- +1
莎普爱思:核心产品滴眼液一致性评价工作或无法按时完成
10月28日晚间,浙江莎普爱思药业股份有限公司(莎普爱思,603168)披露2020第三季度报告,显示今年1月至9月实现营收2.4亿元,同比下降40.61%;归属于上市公司股东的净利润净亏损2805.65万元,同比减少171.65%;归属于上市公司股东的扣除非经常性损益的净利润亏损6233.30万元,同比下降499.93%。
莎普爱思在报告中称,营收和净利润大幅下降的主要是报告期内滴眼液、大输液等产品销售收入下降。
官网资料显示,莎普爱思是一家专业从事药品研发、生产、经营的综合性制药企业,2014年7月2日成功在上海证券交易所A股主板上市。莎普爱思旗下同名滴眼液是莎普爱思的核心产品,根据其2019年年报,滴眼液营收2.32亿元,占比超过45%。
这款滴眼液因为宣称治疗白内障的广告而大受关注,但2017年,有报道直指该产品是涉嫌夸大治疗功效的神药,许多眼科医生也表示该产品无法治疗白内障。随着产品跌下神坛,莎普爱思的营收和净利润也呈现下滑态势。
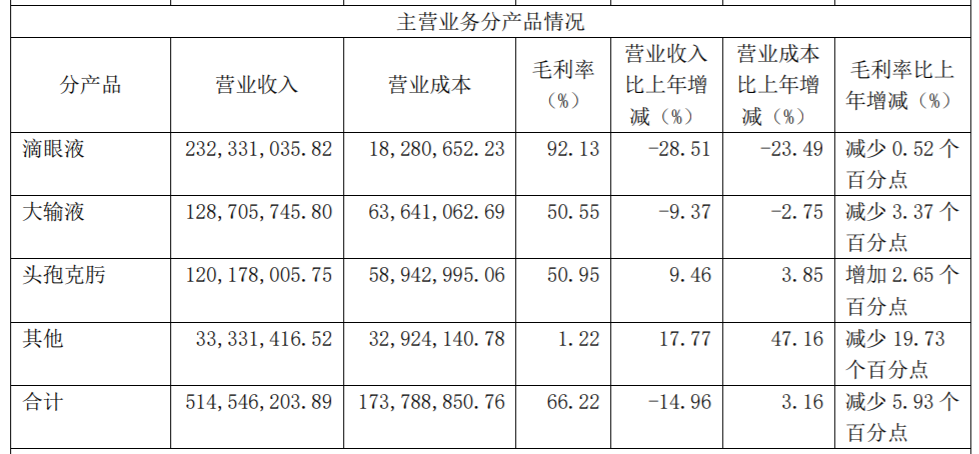
莎普爱思2019年报主营业务分产品情况
2019年年报显示,报告期内,莎普爱思主营业务收入5.15亿元,同比下降14.96%,主要原因就是滴眼液产品销售量同比下降28.51%。到2020年上半年,莎普爱思营收1.38亿元,同比下滑47.93%;净利润亏损1456万元,同比下滑156.66%。
神药风波也让莎普爱思在2017年底收到了浙江省食药监局《转发国家食品药品监督管理总局关于莎普爱思滴眼液有关事宜的通知》,文件要求,滴眼液产品按照《中华人民共和国药品管理法》及仿制药质量和疗效一致性评价的有关规定,尽快启动临床有效性试验,并于三年内将评价结果报国家食品药品监督管理总局药品审评中心。
在最新的第三季度报告中,莎普爱思还提到滴眼液产品一致性评价工作的进展,称苄达赖氨酸滴眼液质量和疗效一致性评价工作存在无法按照国家药监局的要求在三年内完成的可能,该产品药品批准文号或将被注销或到期后不予再注册,导致其不能继续生产销售,对公司生产经营将造成重大影响。
报告中提到,公司已于2016年启动苄达赖氨酸滴眼液的一致性评价工作,委托杭州百诚医药科技股份有限 公司进行苄达赖氨酸滴眼液质量和疗效一致性评价研究。
2018年度,苄达赖氨酸滴眼液(莎普爱思)药品上市后评价工作座谈会、苄达赖氨酸滴眼液 (莎普爱思)上市后临床研究方案讨论会先后召开;公司按照国家有关规定和要求,委托专业CRO 公司组织实施苄达赖氨酸滴眼液(莎普爱思)上市后临床研究,研究方案进一步咨询有关专家意见建议,并上报有关部门。
截至2018年底,已基本完成原研药处方及质量剖析研究、原料药研究、 滴眼液处方筛选、配制工艺优化考察及包材对比研究等相关研究工作,实验室样品的各项质量指标与原研药基本一致,未发现异常状况。
2019年度,浙江大学医学院附属第一医院等全国9个省(市)的9家单位的有关技术人员在广州,参加中山大学中山 眼科中心主办的相关业务培训,以保证各临床研究单位具体操作的一致性。截至本报告披露之日,中山大学中山眼科中心等7家单位已通过伦理委员会的审查。
莎普爱思表示,公司全力以赴推进有关一致性评价工作,但由于新冠疫情影响大,各研究单位有关工作暂停或进展缓慢,各医院伦理审查及合同审核时间较长,试验周期长,公司预计无法在原定期限内将评价结果上报国家药监局药品审评中心。
根据公告,莎普爱思已通过浙江省药品监督管理局向国家药监局申请延期完成一致性评价相关工作。这意味着,苄达赖氨酸滴眼液质量和疗效一致性评价工作存在无法按照国家药监局的要求在三年内完成的可能;或存在公司申请延期完成一致性评价相关工作未予通过的可能;或虽完成苄达赖氨酸滴眼液质量和疗效一致性评价并上报国家药监局药品审评中心,也存在未通过国家药监局的审评审批的风险。
莎普爱思表示,如出现上述情况,如出现上述情况,公司苄达赖氨酸滴眼液药品批准文号将可能被注销或到期后不予再注册,从而导致该产品不能继续生产销售。若公司无法继续生产销售苄达赖氨酸滴眼液对公司生产经营将造成重大影响。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




