- +1
详读全球首例新冠二次感染研究:为何4个月后再中招且无症状
8月24日,中国工程院院士、香港大学李嘉诚医学院微生物学系讲席教授袁国勇(Yuen Kwok-yung)及其团队对外披露香港发现一例新冠肺炎康复者二次感染新案例,该消息迅速引发全球关注。
一天之后,当地时间8月25日,国际权威期刊《临床传染病》(Clinical Infectious Diseases)正式刊发了相关论文。研究指出,即使由于自然感染或接种疫苗而产生了群体免疫力,新冠病毒仍可能继续在人群中传播。研究者们表示,对二次感染患者的进一步研究,会为疫苗设计提供非常重要的保护性相关因素的线索。
该研究题为“COVID-19 re-infection by a phylogenetically distinct SARS-coronavirus-2 strain confirmed by whole genome sequencing”,即“通过全基因组测序确认的、不同系统发育学关系的新冠病毒株导致的新冠肺炎再感染”。研究团队均来自中国香港,所属单位包括香港大学李嘉诚医学院微生物学系、玛丽医院、天水围医院等,研究通讯作者为袁国勇。
论文披露了香港一名33岁男子二度感染新冠病毒(SARS-CoV-2)的案例,该患者系香港第564号个案,为香港居民,曾于3月底确诊新冠肺炎,4月中旬康复出院,并于8月前往英国、西班牙,返港后在香港国际机场进行了例行筛查,8月15日被检测出再次对SARS-CoV-2呈阳性。
在研究背景中,研究团队表示,已有证据表明新冠肺炎的康复患者的免疫力有所下降,但是尚不清楚是否真正会发生再次感染。8月26日,袁国勇在接受澎湃新闻(www.thepaper.cn)记者专访时表示,“这是第一个通过比较基因组测序记录的新冠二次感染。这两次感染的两种病毒株基因组中9种不同病毒蛋白的24个核苷酸的差异和14个氨基酸的变化,强烈表明了患者是再次感染,而不是持续排毒142天。”
基于再次感染发生的可能性,研究者们还强调了以下观点:
第一,群体免疫不可能消除新冠病毒。
第二,疫苗可能无法提供针对COVID-19的终生保护。
第三,患者第二次感染新冠时可能比第一次感染时症状轻,这可能与初次感染期间适应性免疫的启动有关。
以下为澎湃新闻编译的论文(有删减):
引言
迄今为止,新冠肺炎(COVID-19)大流行已经导致约2300万患者感染,影响了200多个国家,超过80万人死亡。新冠大流行严重破坏了全球医疗保健系统,并导致很多社会经济活动停摆。
病毒的家庭传播导致家族聚集病例的发生,由于病原体新型冠状病毒(SARS-CoV-2)的高传播性,其通过空气传播、飞沫传播和接触传播等途径导致餐馆、酒吧、游轮、办公场所和医疗机构疫情大暴发。
除少数地区外,尽管采取了严格的控制措施,COVID-19仍继续在世界范围内流行。此外,许多地区在放宽社会隔离政策后,疫情“卷土重来”。
关于新冠病毒的关键问题之一是,是否发生真正的再次感染。尽管病人在感染后体内会迅速产生中和抗体,但最近的研究表明,抗体滴度最早在急性感染后1至2个月就开始下降。
由于病人康复后仍有长期的一段时间处于低水平的“排毒期”,即病毒水平在RT-PCR检测(逆转录PCR,新冠病毒的检测筛查方法)的检测极限附近,因此检测结果为阴性并出院的新冠患者经常会发生“复阳”的情况。
近期的一个病例报告表明,新冠患者会发生二次感染,但该研究未进行病毒基因组分析,上述有关病例带来了一大争议:新冠康复患者体内再次检测出病毒是由于持续排毒还是由于再次感染?
研究人员分析了一例二次感染的患者,该患者的二次感染发生于第一次感染后4.5个月。团队使用全基因组分析将再感染与长时间排毒期进行了区分,以证明该患者的确发生了再感染,该结论也得到了流行病学、临床和血清学数据的支持。
结果
病例
该患者为一名居住在香港的33岁男性,平时身体较好。在第一次感染新冠病毒时,患者出现3天的咳嗽和痰、喉咙痛、发烧和头痛症状。3月26日,经口咽后唾液SARS-CoV-2的RT-PCR检测确诊为新冠阳性。他于3月29日住院,那时他所有的症状都消失了。该患者于4月14日出院,经鼻咽拭子和咽喉拭子两次RT-PCR检测均为阴性。
8月15日,该患者从西班牙经英国返港,在香港机场进行入境筛查时,采集的口咽部唾液经SARS-CoV-2 RT-PCR检测呈阳性。该患者再次入院,并一直保持无症状。
第二次入院时,他不发烧,体温36.5摄氏度,脉搏频率为每分钟86次,血压为133/94,室内空气中的血氧饱和度为98%。该患者身体检查无异常,住院后口咽后唾液的Ct值为26.69。
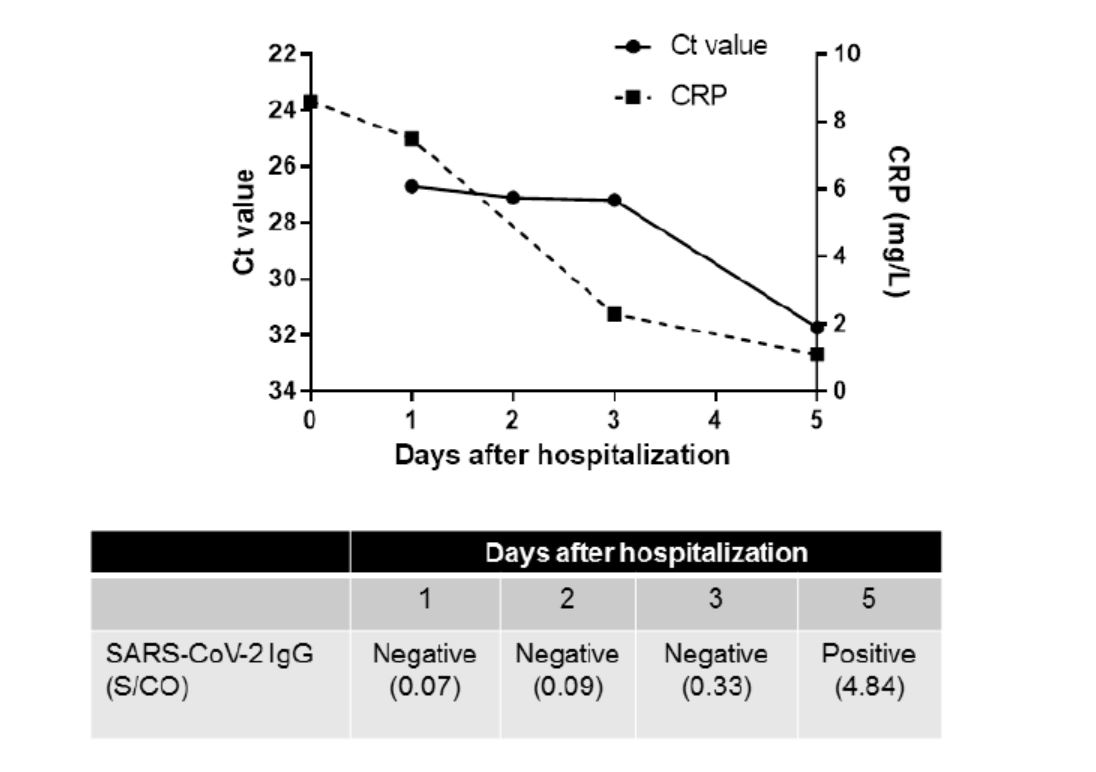
入院时,该患者C反应蛋白(CRP)水平微高,为8.6 mg/L,但在住院期间有所下降。患者也有低血钾症,但其他血液检查结果均正常。患者胸部X光片未发现任何异常。
医院没有给患者进行抗病毒治疗。住院期间,患者口咽后唾液的实时RT-PCR检测Ct值逐渐下降,表明病毒载量减少。
新冠病毒免疫球蛋白G(特异抗体IgG)
患者第一次感染症状发作后第10天和第二次感染住院后第1天收集的血清标本中,针对SARS-CoV-2核蛋白的特异抗体IgG呈阴性。
研究人员还对患者第二次感染期间收集的一系列血清标本进行了新冠病毒IgG的检测,发现住院后1至3天收集的血清标本为阴性,而随后住院后第5天收集的血清标本为阳性。
基因组分析
研究人员对患者3月第一次感染和8月第二次感染期间收集的口咽后唾液标本进行了全基因组测序。
基因组分析结果表明,患者第一次感染和第二次感染的病毒基因组属于不同的进化枝/谱系。第一次感染的病毒基因组属于GISAID进化枝V、Nextstrain进化枝19A、穿山甲谱系B.2(概率为0.99)。而第二次感染的病毒基因组则属于GISAID进化枝G、Nextstrain进化枝20A穿山甲谱系B.1.79(概率为0.70)。

第一次感染的病毒基因组在ORF8(开放阅读框8)64位点有一个终止密码子,导致其58个氨基酸被截断。除此以外,患者第一次感染的病毒组基因与第二次感染的病毒组基因相差23个核苷酸,其中13个是导致氨基酸变化的非同义突变。
两个基因组之间的氨基酸差异位于刺突蛋白、膜蛋白、核蛋白、非结构蛋白和辅助蛋白中。
研究人员对这两个基因组进行了生物大分子序列比对搜索。第一个病毒基因组与2020年3月和4月从美国和英国收集的毒株最相关,而第二个病毒基因组与2020年7月和8月从瑞士和英国收集的毒株最相关。
研究人员还发现,第二个基因组包含nsp6突变,这很少见。
讨论
“我们报告了全球首例再次感染COVID-19的情况。”
研究人员称,有几条证据表明该患者第二次新冠检测阳性是由于再感染,而不是长时间的病毒“排毒期”。
首先,全基因组分析表明,该患者两次感染的SARS-CoV-2毒株属于不同的进化枝/谱系,有24个核苷酸差异,这表明他第二次感染的病毒株与在第一次完全不同。
其次,该患者在第二次感染期间C反应蛋白水平升高,病毒载量相对较高且逐渐下降,并且SARS-CoV-2的特异抗体IgG发生了血清转化,这表明该患者第二次感染是急性感染的一次真正发作。
第三,患者两次感染之间有142天的间隔。先前的研究表明,对于大多数患者而言,在症状发作后一个月就无法检测到病毒RNA了。据报道,很少见病毒的排毒时间持续超过一个月的例子。在一份此前的报告中,一名孕妇在最初新冠测试结果为阳性后104天体内仍检测到病毒。
第四,该患者最近曾前往欧洲,欧洲地区自2020年7月下旬开始再次暴发新冠疫情。患者第二次感染的新冠病毒基因组也与7月和8月在欧洲收集的毒株在系统发育上密切相关。
对于该患者再次感染的确认有几个重要意义。
首先,尽管对于该患者而言,随后的感染可能比初次感染症状轻,但群体免疫不可能消除SARS-CoV-2。与其他人类冠状病毒一样,COVID-19可能会继续在人群中传播。对于“季节性”的冠状病毒229E、OC43、NL63和HKU1,发生再感染是常事。
在某些情况下,尽管体内有一定水平的特异性抗体存在,再次感染仍然会发生。
其次,疫苗可能无法提供针对COVID-19的终生保护。此外,疫苗研究还应包括从已康复的新冠患者。
尽管该患者第二次感染期间CRP升高且血清转化为急性感染,但该患者在第二次感染期间无症状。先前对恒河猴的再感染的研究也显示,再感染时其病情较轻,这可能与初次感染期间患者适应性免疫的启动有关。
在新冠病毒感染期间,大多数患者都会产生中和抗体。在本研究中,尽管在患者第二次感染初期未检测到新冠抗体,但残留的低滴度抗体可能已经部分控制了病毒。
由于中和抗体靶向病毒的刺突蛋白,因此刺突蛋白的变异可能会使病毒对第一次感染时患者体内的中和抗体的敏感性降低。事实上,刺突蛋白受体结合结构域和N端结构域中的几个突变已显示出其对于中和抗体敏感性的降低。
对于本研究中的患者,第一次和第二次感染的病毒刺突蛋白中有4个氨基酸残基不同,即L18F、A222V、D614G和Q780E。
先前的研究已经确定,氨基酸残基222和614都位于B细胞免疫优势表位之内,A222V和D614G可能会影响这些表位的结构。 D614G位于病毒刺突蛋白的亚结构域2,这一突变在大多数SARS-CoV-2毒株中被发现。使用伪病毒的研究表明,D614G可增强SARS-CoV-2的复制能力。
最近一项使用伪病毒的研究表明,大约7%的恢复期新冠患者血清样本显示出对614G假病毒的中和活性比614D降低。我们需要进一步的血清学研究来确定,第一次感染和第二次感染之间SARS-CoV-2毒株刺突蛋白中的这些氨基酸差异是否是造成患者再次感染的原因。
T细胞免疫也可能在改善再次感染的严重程度方面发挥作用。在COVID-19大流行之前对冠状病毒的研究表明,冠状病毒可以诱导持久的T细胞免疫。
T细胞免疫主要针对新冠病毒刺突蛋白,尽管也可以发现CD4或CD8 + T细胞对其他病毒蛋白的反应。Grifoni等人的研究表明,两个CD4 + T细胞都主要靶向结构蛋白(刺突、膜和核蛋白)。
CD4 + T细胞也靶向nsp3、nsp4和ORF8,而CD8 + T细胞靶向nsp6、ORF3a和ORF8。
初次感染新冠数月后,能够在恢复的COVID-19患者中检测到T细胞免疫。患者两次感染的新冠病毒基因组的氨基酸变化之一位于刺突蛋白氨基酸残基222,该残基也是引起CD4 + T细胞反应的潜在位点。
在患者第二次感染后不久,研究人员在收集的血液样本中未检测到针对SARS-CoV-2的特异抗体IgG。抗体水平低可能与该患者首次感染期间的症状较轻有关。多项研究已表明,病情较轻的患者的抗体滴度低于病情较重的患者。
新冠感染后缺乏抗体应答可能会影响再次感染的敏感性和感染的严重性。尽管本次研究中的患者在第二次感染期间无症状,但再次感染有可能导致更严重的感染。
此前对SARS-CoV的研究表明,针对刺突蛋白的抗体可能与更严重的急性肺损伤有关。但是,本研究中的患者在第二次感染期间,直到住院后5天体内才检测到抗新冠病毒的免疫球蛋白G。
一种可能是他在第一次感染后没有发生抗体反应,但是由于研究人员只在他第一次感染症状发作后10天才收集了存档的血清样本,因此无法确定。先前的研究表明,某些患者直到症状发作后2-3周才检测到抗体反应。
另一种可能性是,他确实在第一次感染后引发了抗体反应,但抗体滴度下降到低于检测限度。抗体的这种减弱已被此前的研究充分描述,在一项研究中,有33%的新冠患者在恢复期(症状发作后平均39天)对中和抗体反应呈阴性。
另一项研究表明,在症状发作后的8周内,有40%的无症状新冠患者血清反应阴性。除了缺乏防止再次感染的保护措施外,抗体滴度快速下降的另一个提示是,针对血清阳性率的研究可能低估了真实的感染发生率。
这项研究存在几项局限。
首先,研究人员在患者第一次感染期间仅收集了一个血清样本。由于患者可能无法在10天之内发生抗体反应,因此阴性的抗体测试结果不能排除患者在第一次感染的早期恢复期确实出现抗体反应的可能性。
其次,使用两次感染的上呼吸道标本进行的病毒培养仍在进行,因此无法比较第一次感染和第二次感染中针对病毒的中和抗体效价。
这一病例说明,即使是从第一次感染恢复几个月后,也可能会发生再次感染。研究结果表明,即使患者通过自然感染或通过疫苗接种获得了免疫力,SARS-CoV-2仍可能像其他会带来普通感冒的人类冠状病毒一样在人类体内持续存在。
从SARS-CoV-2感染中恢复,并被同一病毒再次攻击的恒河猴,在支气管肺泡灌洗中,第二次感染期间的病毒载量峰值比第一次感染时降低了超过5 log10,而鼻拭子中的病毒载量峰值仅降低了约2 log10。
同样,在疫苗研究中,仍可以在接种疫苗的动物的上呼吸道中检测到新冠病毒RNA。
有必要对再感染进行进一步的研究,这对于研发更有效的疫苗至关重要。
总之,有症状感染新冠4.5个月后再次感染是可能的。因此,已经感染过一次的患者也应考虑接种疫苗。即使是感染过COVID-19的人,也应遵守流行病控制措施,例如全体佩戴口罩和保持社会距离。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




