- +1
文献解读:晚期实体瘤伴肾损伤患者使用奥拉帕利的药代动力学性质和安全性


奥拉帕利是一种口服PARP抑制剂,早期在美国等国家批准的剂量为400mg胶囊剂型,每日两次(BID),因此患者需要摄入8×50mg胶囊BID。现在使用的片剂可以减少服药负担,300mg奥拉帕利片剂(2×150mg BID)具有相似甚至更优于400mg胶囊制剂的暴露量,因此后来的Ⅲ期研究均使用奥拉帕利片剂,并且片剂也获得批准应用于临床。奥拉帕利片剂已经在欧洲、美国和中国等国家被批准用于治疗卵巢癌,并在美国被批准用于治疗携带gBRCAm的HER-2阴性转移性乳腺癌、HRRm的激素抵抗型转移性前列腺癌和携带gBRCAm的胰腺癌等。
该研究则是旨在探索肾功能损伤患者服用奥拉帕利的药代动力学和安全性。研究分为两个部分:(1)晚期实体瘤伴轻至中度肾损伤患者中单次口服奥拉帕利300mg,以评估奥拉帕利片剂在这类人群中的药代动力学(第一部分);(2)单次(第一部分)和多次300mg BID(第二部分)服药后,比较奥拉帕利在肾损伤者和肾功能正常者中的耐受性。通过这些研究,可评估在肾损伤患者使用奥拉帕利片剂的推荐剂量。
研究设计
该研究分为两部分,为Ⅰ期、干预性、开放标签、PK对比研究(NCT01894256)。研究包括5个欧洲国家(比利时、丹麦、法国、荷兰和英国)的13个中心。第一部分用于评估奥拉帕利单次300mg剂量在轻至中度肾损伤患者中的PK,并与肾功能正常者作比较。第二部分旨在提供额外的安全性数据,允许患者继续使用奥拉帕利300mg BID以评估长期安全性。在这部分研究中没有更深入的PK分析。安全性评估包括患者的不良反应(AE)、生命体征、心电图、实验室数据和体格检查。尽管在研究中没有评估疗效,第二部分中允许有临床获益的患者继续治疗。
入组的患者包括肾功能正常者、轻至中度肾损伤患者(估计肌酐清除率分别为≥81,51-80或31-50Ml/min)。血液标本在给药后96h、尿液标本在给药后24h采集。
主要研究结果
第一部分:44例患者经过评估并接受至少一次奥拉帕利治疗(肾功能正常者和轻度肾损伤者各15例,中度肾损伤者14例)。三组患者人口学和基线特征基本平衡,肾功能降低者年龄稍大。不同肾功能组几何学均数奥拉帕利血浆浓度-时间资料见图1。
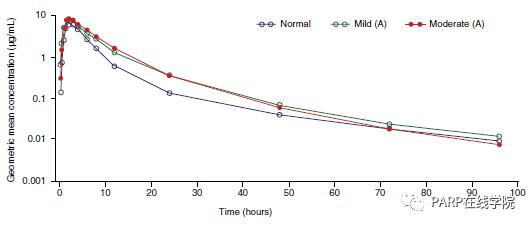
与正常肾功能组相比,轻度肾损伤组AUC GLS均数比1.24(90% CI:1.06-1.47),GLS均数Cmax比1.15(1.04-1.27);中度肾损伤组AUC GLS均数比1.44(1.10-1.89),Cmax 1.26(1.06-1.48,图2)。
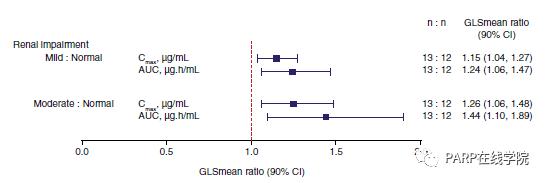
奥拉帕利AUC GLS均数比及GLS均数Cmax比汇总
第二部分:共43例患者(肾功能正常者15例,轻度和中度肾损伤者各14例)进入第二部分研究并继续治疗直至疾病进展/缺乏疗效[40(93.0%)] 。其他导致治疗终止的原因包括:死亡[由于疾病进展,2(4.7%)]和患者意愿[1(2.3%)。] 正常肾功能组平均实际治疗时间为134.2(29-381)天,轻度肾损伤组158.5(18-627)天,但中度肾损伤组显著减少,为60.8(4-247)天。
第二部分研究的详细AE见表1。36起研究者报告的AE被认为与奥拉帕利相关,其中恶心(正常肾功能组、轻度和中度肾损伤组分别为60%、50%和57%)、乏力(53%、57%和57%)、食欲减低(20%、36%和36%)和贫血(20%、36%和36%)最常见。除了食欲减低和贫血,泌尿道感染(7%、0%和21%)在中度肾损伤组更常见。16例患者出现31起≥3级AE,其中7起被研究者评估为与奥拉帕利相关。中度肾损伤组2例患者(14%)报告出现≥3级泌尿道感染和虚弱,正常肾功能组和轻度肾损伤组未出现。9例患者共报告16起严重AE,其中5起被研究者认为与奥拉帕利相关[3起贫血(正常肾功能组、轻度和中度肾损伤组各1起)、1起血小板减少和中性粒细胞减少(均出现在轻度肾损伤组的同一例患者)]。研究报告了2例死亡,经调查均由于肿瘤进展。没有出现AE导致的永久终止奥拉帕利治疗。临床实验室检查显示7例患者出现CTCAE≥3级血红蛋白减低:1例为正常肾功能组,3例为轻度肾损伤组,3例为中度肾损伤组(所有均在AE中被分类为贫血)。
表1 第二部分研究中奥拉帕利长期安全性评估AE汇总
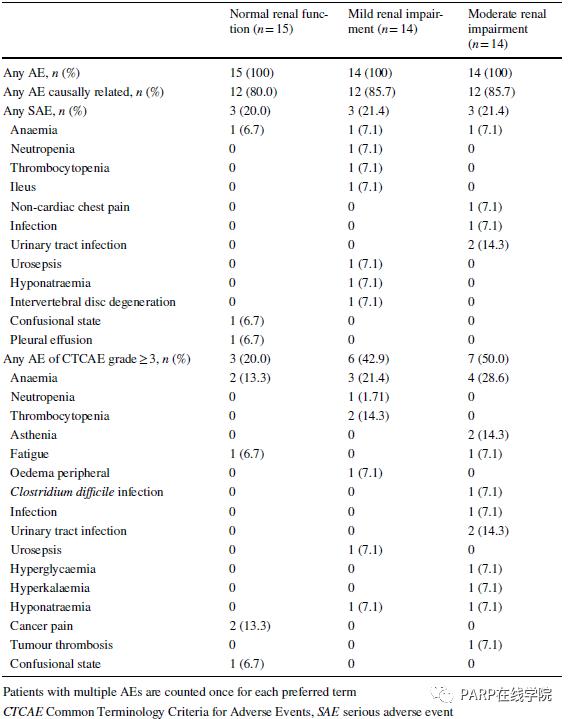
轻度肾损伤患者接受奥拉帕利片剂仅轻微增加奥拉帕利暴露量,不认为会影响到临床治疗,其安全性与肾功能正常者一致。在中度肾损伤患者中未发现新的安全性信号,但是奥拉帕利暴露量(AUC)增加44%。为了应对这种状况,中度肾损伤患者应当进行严密监测,尤其是血液系统毒性,并且将剂量从300mg BID(2×150mg片剂)减少至200mg BID(2×100mg片剂)。不推荐重度肾损伤患者或终末期肾病患者使用奥拉帕利,因为在这类患者中奥拉帕利的安全性和药代动力学未被研究。
本文转自 PARP在线学院
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




