- +1
《科学》子刊:疱疹病毒竟能独立诱导阿尔茨海默病的病理特征
原创 奇点糕 奇点网 来自专辑阿尔茨海默病相关
2020年,阿尔茨海默病依旧扑朔迷离。
深耕几十年的β淀粉样蛋白和tau蛋白领域终点难寻,科学们不得不转而用另一种角度去思考阿尔茨海默病的病因。
2017年,科学家发现β淀粉样蛋白其实是一种抗感染蛋白;2018年,来自中国台湾的队列研究发现疱疹病毒感染竟会增加痴呆风险;同年,科学家揭示了两种人类疱疹病毒(HHV)参与调控阿尔茨海默病相关基因的机制。
这一切似乎都在暗示我们,阿尔茨海默病其实是存在特定病原体的,而这个幕后元凶就是生活中非常常见的疱疹病毒。
近期,《科学进展》杂志上发表了一项新的研究成果,科学家们发现,在人类诱导神经干细胞(hiNSC)构成的3D大脑模型中,1型单纯疱疹病毒(HSV-1)感染竟然能够在完全没有其他因素参与的情况下,诱导淀粉样蛋白沉淀形成、神经胶质增生、神经炎症和神经功能下降——也就是阿尔茨海默病的标志性病理变化![1]
另外,这个3D模型也是第一个阿尔茨海默病的3D大脑模型,而且并不依赖与APP、PSEN1/2等相关基因突变,对未来的研究可以说是非常有力的工具。
其实被认为与阿尔茨海默病有关的病原体并不少,例如肺炎衣原体、伯氏疏螺旋体(Borrelia burgdorferi)、光滑念珠菌( Candida glabrata)等等。最常被提到的则是以1型单纯疱疹病毒(HSV1)和6型人类疱疹病毒(HHV-6)为主的疱疹病毒科。
这些病毒很常见,据估计,90%的人到70岁时都会携带HSV-1,而几乎每个婴儿出生后都会感染HHV-6,这些病毒能够静静地在我们体内潜伏数十年。
今天主要介绍的HSV-1,是一种嗜神经双链DNA病毒,主要存在外周神经中。HSV-1的激活可以没有症状,主要表现为唇部疱疹,极少数情况下也会发生单纯疱疹性脑炎(HSE)——这说明,HSV-1是可以穿透血脑屏障的[2]。
了解了单纯疱疹性脑炎,就不由得人怀疑HSV-1与阿尔茨海默病的关系了。通过对病例的观察,我们可以发现,HSV-1感染脑部的区域与阿尔茨海默病病理发生的脑区基本一致,而且脑炎患者也常常表现出典型的认知和行为障碍[3]。
更进一步的研究发现,阿尔茨海默病患者的脑部存在HSV-1;而超过3万人的中国台湾队列更是明白指出,HSV-1感染会使痴呆风险上涨2.564倍,同时进行抗病毒治疗则能降低九成风险。
如果能够从头揭发HSV-1感染诱导人脑组织产生阿尔茨海默病的过程,那就可以说是彻底实锤了。
但是这却并不容易。
目前,大多数体外的人类阿尔茨海默病模型主要依赖来自早发性阿尔茨海默病患者的细胞——换言之,其实就是靠APP、PSEN1、PSEN2这三种与β淀粉样蛋白产生有关的基因的突变。虽然这确实可以一定程度上重现病理过程,但实际上这些患者只占全部患者的比例不到5%,这意味着很多潜在的环境因素和因果关系都被忽视了。
这就是本次研究提出的模型的优越之处了。
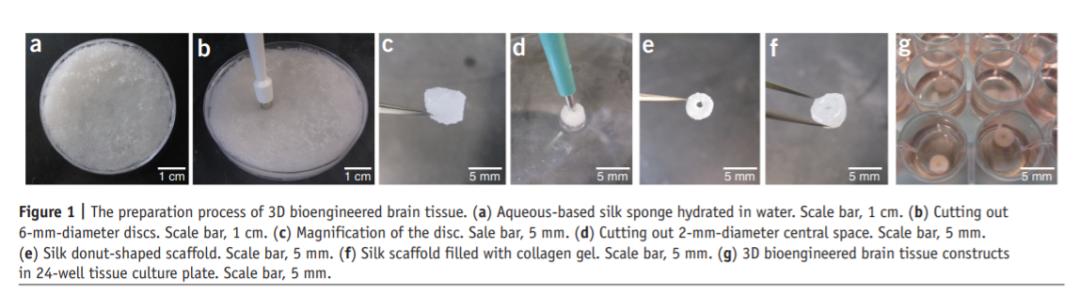
此前,研究团队已经开发出了由真皮成纤维细胞重编程人类诱导神经干细胞(hiNSC)的技术,这种hiNSC可以迅速扩增和分化,在没有复杂分化方案和培养基要求的情况下,短短4天之内就能够自发生成多种神经元和神经胶质细胞,而且它们对各种生长因子、药物都很敏感,也很容易被寨卡病毒等嗜神经病毒感染[4]。
将这种hiNSC植入生物材料制作的支架,并注入胶原蛋白凝胶,就能够生成具有代表性大脑结构的体外3D人类大脑组织模型,观察神经突触、神经元网络、电生理都不成问题。
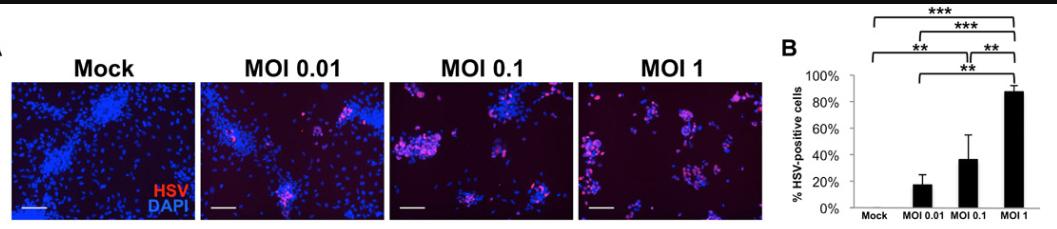
首先,hiNSC是的确可以被HSV-1感染的。在感染复数(MOI)为1的情况下,共培养24小时,几乎100%的hiNSC都感染了HSV-1,病毒水平随培养时间延长而增加。同时,感染细胞也能够分泌HSV-1感染其他细胞。
这表明低水平的病毒感染可以随时间推移导致高水平感染,这也与临床上患者的HSV-1感染再激活很像。
高水平的病毒感染对hiNSC来说是致命的,MOI越高、细胞凋亡就越多,即使MOI为0.01的情况下也会导致大量细胞死亡,所以研究者采取极低MOI 0.0001感染细胞。
有趣的是,研究者观察到hiNSC一些特殊的变化。简单来说,被感染的hiNSC形成了特殊的多细胞结构,与此前研究发现的阿尔茨海默病患者大脑中的合胞体相似[5]。感染时神经元越不成熟,形成的多细胞团块结构就越大。
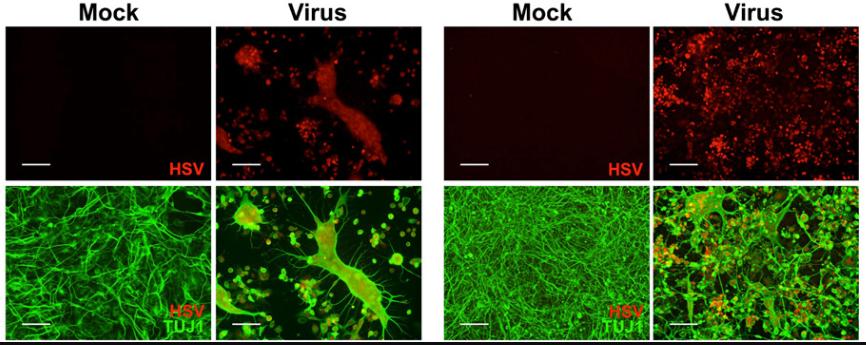
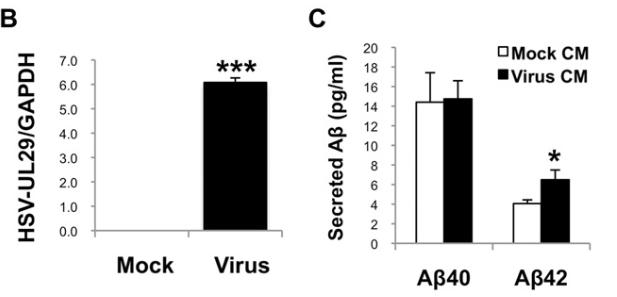
通过特殊的荧光染色和ELISA,研究者发现在这些多细胞结构中存在淀粉样蛋白原纤维,而且其中增加的主要是Aβ1-42,Aβ1-40则没有变化,这也是和阿尔茨海默病的病理表现一致的[6]。
经过qPCR,研究者发现,HSV-1会引起APP和BACE1表达的下调,以及PSEN1/2表达的上调。
考虑到β淀粉样蛋白沉淀并不是阿尔茨海默病唯一的病理特征,研究者还分析了神经纤维缠结(NFT)的存在。结果,在SV-1感染的hiNSC中,淀粉样蛋白原纤维的附近确实存在不少组成NFT的tau蛋白。
既然β淀粉样蛋白沉淀和神经纤维缠结这两大主要特征已经初露端倪,那么阿尔茨海默病的其他病理变化自然也得检查一下。
在HSV-1感染后,hiNSC中多种胶质细胞的标志物表达水平高度上调,而且由HSV-1诱导产生的神经胶质细胞表现出一种特殊的多核球状,这也与阿尔茨海默病患者尸检时发现的星形胶质细胞融合现象一致[7]。
包括肿瘤坏死因子α(TNF-α)、白介素1β(IL-1β)、IL-6和干扰素γ(IFN-γ)在内的多种与阿尔茨海默病有关的炎性细胞因子也都在HSV-1感染之后表达骤升。
作为类器官,HSV-1感染的3D模型也表现出了较弱的电生理活动,与阿尔茨海默病患者的脑功能受损相应。
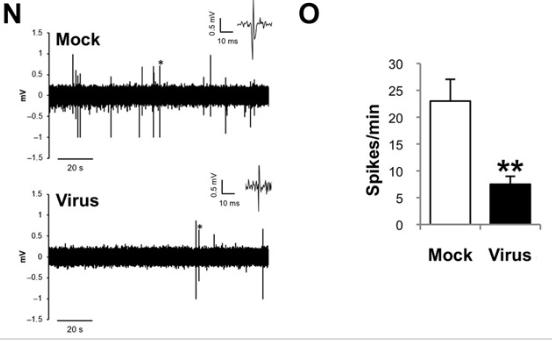
那么,针对HSV-1的抗病毒治疗是否能够挽救“大脑”呢?
研究者选择了常见的抗病毒药物VCV。结果显示VCV能在降低HSV-感染的同时,也大幅度减少相关病理现象。值得注意的是,如果在HSV-感染之前给药,那么几乎可以避免HSV-感染和病理现象的出现,但感染之后给药,就只能逆转一部分了。
由此可见,低水平的HSV-1感染的确与阿尔茨海默病的发生密不可分。不过HSV-1感染其实也相当常见,其中更复杂的过程还需要进一步研究去探索。
参考资料:
[1]https://advances.sciencemag.org/content/6/19/eaay8828
[2] H. Liu, K. Qiu, Q. He, Q. Lei, W. Lu, Mechanisms of blood-brain barrier disruption in herpes simplex encephalitis. J. Neuroimmune Pharmacol. 14, 157–172 (2019).
[3] M. J. Ball, “Limbic predilection in Alzheimer dementia: Is reactivated herpesvirus involved?”. Can. J. Neurol. Sci. 9, 303–306 (1982).
[4] D. M. Cairns, D. S. S. K. Boorgu, M. Levin, D. L. Kaplan, Niclosamide rescues microcephaly in a humanized in vivo model of Zika infection using human induced neural stem cells. Biol. Open 7, bio031807 (2018).
[5] W. Bondareff, Age-related changes in brain extracellular space affect processing of amyloid-β peptides in Alzheimer’s disease. J. Alzheimers Dis. 35, 1–6 (2013).
[6] B. De Strooper, R. Vassar, T. Golde, The secretases: Enzymes with therapeutic potential in Alzheimer disease. Nat. Rev. Neurol. 6, 99–107 (2010).
[7] B. G. Perez-Nievas, A. Serrano-Pozo, Deciphering the astrocyte reaction in Alzheimer’s disease. Front. Aging Neurosci. 10, 114 (2018).


本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




