- +1
世界免疫周,带你了解新冠疫苗
原创 华山感染
世界免疫周 4月24日—4月30日
疫苗的发现是人类发展史上一件具有里程碑意义的事件。1796年英国医生詹纳(Edward Jenner,1749-1823)将正在出牛痘的女孩皮肤上的水泡液,接种到一个8岁健康男孩身上,堪称医学史上最为冒险的一次实验,由此世界上第一支疫苗由此诞生。詹纳的成功不仅使世界摆脱了一种可怕的疾病——天花,也建立了免疫学这门科学,为后人的研究打开了通道,促使后来的科学家巴斯德等人针对其他疾病寻求治疗和免疫的方法,最终开创了人类防治传染病的新时代。

图:1796年詹纳医生给8岁的菲普斯“种痘”
每年4月最后一周(4月24—30日)是特殊的日子——"世界免疫周",其目的是促进接种疫苗以保护各年龄人群免患疾病。今年的世界疫苗周的主题是“疫苗保护人人”。

图:来自世界卫生组织官网
对于传染病,我们人类最有力的武器还是疫苗。凭借疫苗,我们消灭了天花,接近消灭了脊髓灰质炎,每年能够挽救无数生命。疫苗被广泛认为是世界最成功和最具成本效益的卫生干预措施之一。

图:来自世界卫生组织官网
新冠疫苗研发
开历史之先河
新型冠状病毒(SARS-CoV-2)疫情已经持续将近4个多月了,目前仍在全球肆虐,截至到4月24日6时,全球确诊超269万例,死亡超18万例,其波及范围之广、感染及死亡人数之高为过去100年前所未见。并且,有迹象表明本次新冠肺炎有可能在未来相当长时间内会像流感一样“常伴”人类左右在人群中流行。在目前这种的形势下,只有依靠开发出有效的疫苗是才能较好的控制或消除该传染病。
就在日前,全球首个新冠病毒疫苗的临床前试验数据发布了。让我们在这个特殊的日子一起了解下新冠疫苗的研发始末和最新进展,看看新冠疫苗是否能够带领人类安全摆脱这场百年一遇的疫情。
图:来自网络
实际上,研发一个全新的疫苗并不容易。
根据历史经验,新疫苗的研发周期平均为10年。面对来势汹汹的新冠肺炎,为了缩短疫苗研发周期,多国政府、疫苗研发机构与疫苗生产企业通力合作,期望以最快速度研发出有效的新冠病毒疫苗。
在我国,在疫情暴发之初,就已经迅速确立了疫苗研究攻关研究项目,8家国内顶级研究机构,同时通过5条不同技术路线开展疫苗研发,分别是:灭活病毒疫苗、重组蛋白疫苗、腺病毒载体疫苗、核酸疫苗(mRNA疫苗和DNA疫苗)以及减毒流感病毒载体疫苗。
在国际上,1月23日武汉封城开始当天,流行病防范创新联盟(the Coalition for Epidemic Preparedness Innovations, CEPI)就宣布资助多家机构上千万美元资金用于开发新冠病毒疫苗,分别开展DNA、mRNA以及蛋白质疫苗研究。截止4月15日,该机构已向全球8家研究机构投入总计2920万美元用于研发新冠病毒疫苗。
就响应速度而言,此次新冠病毒疫苗研发可谓开历史之先河。第一名新冠疫苗临床试验受试者在3月16日就接受了第一次的免疫接种,距疫情暴发尚不到4个月。这既体现了社会各界对遏止疫情的共同决心,也体现了当代医学科技水平的进步。截止4月8日,全球在研的候选新冠病毒疫苗有115种,其中78种候选疫苗正在快速进展中。开发者中有36家来自北美,14家来自中国、14家来自除中国外的亚太地区,另外14家来自欧洲,并有5种疫苗已经进入I期临床实验[1]。
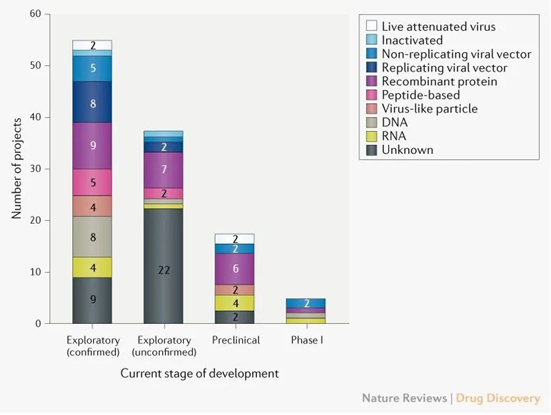
图:不同种类的新冠疫苗及其所处的开发阶段,Exploratory:还在早期研发的项目(分为已确认(confirmed)和未确认(unconfirmed)),没有进行动物模型测试;Preclinical:临床前项目,处于动物模型测试和/或生产临床试验用料的阶段。引用自:Nat Rev Drug Discov. 2020 Apr 9. doi: 10.1038/d41573-020-00073-5.
为了更清晰的展示本次新冠疫苗研发进度,我们将标志性事件按时间顺序整理如下:
01-11
中国科学家公布新冠病毒基因组
01-24
我国成功分离首株新冠病毒毒种
03-04
美国Moderna公司mRNA疫苗mRNA-1273获批开展I期临床试验
03-16
中国腺病毒重组疫苗Ad5-nCoV获批开展I期临床试验;
mRNA-1273招募了第一例受试者
04-03
美国Inovio Pharmaceuticals公司DNA疫苗INO-4800获批进入I期临床试验
04-09
Ad5-nCoV公布I期安全性数据,宣布计划展开II期临床试验
04-12
中国生物武汉生物制品研究所和中国科学院武汉病毒研究院联合申请的新冠病毒灭活疫苗进入I期临床试验
04-13
北京科兴中维生物技术有限公司灭活疫苗进入I期临床试验
下面,我们一起来认识一下在这一次全球“战疫”中备受关注的明星候选疫苗:
01
mRNA-1273
全球第一个获批进入临床试验的候选疫苗为美国Moderna公司的mRNA疫苗。早在1月13日,美国国立卫生院(NIH)和Moderna就完成新冠病毒疫苗序列的设计,起名为 mRNA-1273。由CEPI出资后Moderna启动临床生产,2月7日第一批临床生产的疫苗完成,耗时25天。3月4日,美国食品药品监管局(FDA)批准了mRNA-1273进入临床试验,3月16日,第一位志愿者接受了第一剂疫苗的接种。
02
Ad5-nCoV
中国第一个获批进入临床试验的候选疫苗重组腺病毒载体疫苗Ad5-nCoV。该疫苗由军事科学院军事医学研究院的陈薇院士团队与康希诺公司联合开发,以复制缺陷型人5型腺病毒为载体,表达新型冠状病毒S抗原,其工作原理是能免疫刺激人体产生针对新冠病毒的抗体。3月16日获国家药品监督局批准展开I期临床试验,并于4月9日公布I期临床试验共108名志愿者的初步安全数据,并宣布进入临床II期。
03
INO-4800
全球第三款进入临床试验阶段的新冠疫苗,也是第一个DNA候选疫苗,是来自Inovio Pharmaceuticals公司的INO-4800。在获得病毒基因序列后,Inovio在三个小时内就完成了疫苗设计。1月30日,Inovio公司宣布与国内企业艾棣维欣达成合作协议,共同推进INO-4800在中国的研发工作。4月7日,FDA接受该公司为新冠病毒候选DNA疫苗递交的新药临床试验(IND)申请。
04
灭活病毒疫苗
全球第一个灭活病毒疫苗由国药集团中国生物武汉生物制品研究所有限责任公司与中科院武汉病毒所研发。2月1日,项目获得科技部国家重点研发计划“公共安全风险防控与应急技术装备”重点专项“2019-nCoV灭活疫苗”紧急立项。短短2个多月,完成疫苗株筛选、毒种库建立、抗体制备及鉴定、检测方法建立、生产工艺研究、配伍及配方筛选,迅速开展并完成动物体内有效性及安全性评价等工作,于4月12日获得国家药品监督管理局临床试验许可,开展随机、双盲、安慰剂平行对照I/II期临床试验。
另一个被批准进入临床研究的新型冠状病毒灭活疫苗(PiCoVacc),由北京科兴中维生物技术有限公司联合中国医学科学院、中国科学院、浙江省疾病预防控制中心、中国疾病预防控制中心、军事医学科学院及国家食品药品监督管理局共同研制。在临床前验证中,PiCoVacc在小鼠、大鼠及恒河猴体内均成功诱导产生了保护性抗体[2]。
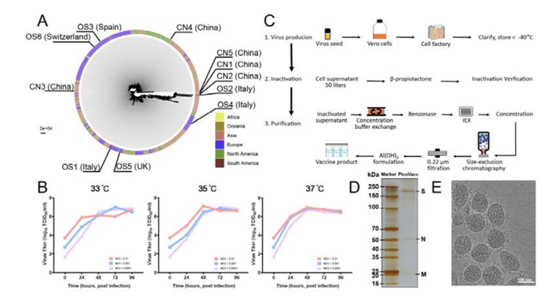
图:PiCoVacc的特性(A)SARS-CoV-2系统发育树。(B)PiCoVacc(CN2)P5菌种在Vero细胞中的生长曲线。(C)PiCoVacc制备流程图。(D)PiCoVacc的蛋白组成和纯度。(E)PiCoVacc电子显微照。[2]
以上四种疫苗的设计目标均为通过诱导人体产生抗新冠病毒抗体来实现免疫保护,但是各自的技术原理并不相同:前三种疫苗是运用基因合成与克隆技术将新冠病毒基因以核酸或者重组病毒的形式导入人体细胞,激发人体产生免疫应答;而灭活病毒疫苗则是通过化学灭活病毒的方法制备疫苗,属于传统疫苗制备方案。不同疫苗制备方案各有特点,实际保护效果需通过后续临床试验来进行评价和比较。

图:来自网络。
目前几乎全球所有从事疫苗研发机构都在投入研发新冠疫苗,中国也是走在了新冠疫苗研发的前列,但是也面临量产、临床试验资源等问题,应该加强各个机构间合作和交流,汇集各方优势共同攻关,全球合作才能大幅缩短疫苗研发周期。
虽然全世界都是以极大的资源和人力全力投入新冠疫苗研发,审批流程大大加速,但是从研发到获得一款安全有效可以在人群中推广接种的疫苗并不容易,花费的时间要好几年。
此外,本周末我们有关于全球的新冠疫情与疫苗未来的学术研讨会,届时将汇聚中美华裔专家共同探讨疫苗能否成为解决新冠威胁的“破局之剑” ?

其实,在世界疫苗周这样的日子,特别注意的是除了新冠肺炎,这个世界还有很多需要防范的传染病。Gavi首席执行官塞斯·伯克利(SethBerkley)提醒到:“世界曾关注埃博拉,但实际上死于麻疹的人数是死于埃博拉的2.5倍。现在全球关注新冠疫情,也会有其他传染病大规模暴发,这可能使卫生系统被完全压垮,我们该如何应对?”
许多传染病已经有非常成熟的疫苗,我们仍应该重视这些已有的有效疫苗合适人群的接种,特别是儿童的计划免疫接种,请家长们一定要重视,及时带小朋友完成接种,特别是因为疫情耽误接种的疫苗应该及时补种。此外,每年的秋冬季也是流感大流行的季节,这里再次提倡大家记得在每年流感季到来前接种流感疫苗。
参考文献:
1. Thanh Le T, Andreadakis Z, Kumar A, et al. The COVID-19 vaccine development landscape.Nat Rev Drug Discov 2020.
2. Gao Q, Bao L, Mao H, et al. Rapid development of an inactivated vaccine for SARS-CoV-2. bioRxiv 2020: 2020.2004.2017.046375.
供稿:吴晶 阮巧玲 万延民 王新宇
编辑:刘其会
审核:张文宏
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




