- +1
狗是新冠中间宿主?研究称病毒在狗肠道进化后传人,引发质疑
自从新冠肺炎COVID-19暴发以来,全世界越来越多的实验团队加入溯源队伍,试图了解引发这次疫情的新型冠状病毒如何从动物宿主传染给人类。截至目前,该疫情已造成全球确诊患者超过190万人,累计死亡超过12万人。
目前普遍认可的是,新冠病毒或来源于蝙蝠,其和中科院武汉病毒所石正丽研究员团队2013年在中国云南采集的RaTG13样本的相似性为96.2%。然而,科学家们仍一直在寻找介于蝙蝠和首次将新冠病毒病毒引入人类之间的中间宿主,蛇、穿山甲此前都被纳入“疑似名单”。
最新的一份研究将该名单再补充一员——狗。当地时间4月14日,国际权威期刊《分子生物学和进化》(Molecular Biology and Evolution,其2018/2019影响因子为14.797)杂志在线发表了一项研究,给出一种全新的推测:狗或许是将新冠传染给人类的中间宿主,病毒可能在狗的肠道中进化,从而获得了感染人的能力。

夏旭华总结,他这项研究的结果为新冠病毒的起源和最初传播提供了假设。首先,新冠病毒和蝙蝠来源冠状病毒RaTG13的祖先感染了一种哺乳动物的肠道(例如犬科动物或人类食用的蝙蝠肉)。第二,犬类肠病毒RNA基因组对CpG的强选择性可能导致病毒的快速进化,大量CpG到UpG 的突变导致基因组ICpG和GC%的减少。第三,犬类在交配和其他情况下会舔舐肛门区域,帮助病毒从消化系统传播到呼吸系统。最后,减少的病毒基因组ICpG使病毒逃避人类ZAP介导的免疫应答,成为一种严重的人类病原体。
他强调,这表明,在与新冠病毒的斗争中,监测野狗体内SARS样冠状病毒的重要性。
不过,夏旭华的这份推论目前已引发了多名学者公开质疑。
抗病毒前哨蛋白:ZAP
包括蝙蝠在内的野生哺乳动物物种构成了冠状病毒(包括SARS、MERS和致命的新冠病毒)的天然宿主。论文中提到,不同的宿主或宿主组织提供不同的细胞环境,特别是不同的抗病毒和RNA修饰活动,这些可以改变病毒RNA基因组中观察到的RNA修饰特征。
其中,锌指抗病毒蛋白(ZAP)是哺乳动物干扰素介导免疫应答的关键成分,其RNA结合域与病毒RNA基因组中的CpG二核苷酸特异性结合。ZAP可抑制病毒复制,并介导病毒基因组降解。因此,ZAP的作用就类似于抗病毒前哨蛋白。
ZAP不仅可以对抗HIV-1这样的逆转录病毒,还可以对抗埃柯病毒7型和寨卡病毒等,后两种病毒都是正义单链RNA病毒,类似冠状病毒。特别是,在ZAP缺陷细胞中,针对病毒RNA中CpG的选择消失了。论文中提到,这表明ZAP可能是唯一针对病毒RNA基因组中CpG的细胞因子。
实际上,许多哺乳动物RNA病毒已经进化出CpG缺陷。此前的研究显示,在ZAP存在的情况下,在这些低CpG病毒基因组中增加CpG二核苷酸始终会导致病毒复制和毒力下降。这也促使提出了涉及增加CpG以减弱致病性RNA病毒的疫苗开发策略。
作者引用了此前的一些认为,病毒RNA基因组中CpG的减少与毒性增强之间存在关联。在RNA病毒中,CpG下降与毒力增强之间的联系主要是由于干扰素诱导的ZAP蛋白通过其RNA结合域与病毒RNA基因组中的CpG二核苷酸结合,抑制病毒复制,促进病毒基因组降解。
基于此,作者提到,病毒病原体中ICpG的减少意味着对公共卫生的威胁增加,但ICpG的增加减少了这种威胁,因为这类病毒病原体,随着ICpG的增加和毒力的降低,将类似于自然疫苗。“事实上,许多病毒研究人员已经提出通过增加病毒RNA基因组中的CpG来开发疫苗。”
鉴于ZAP表现出组织特异性表达,因此感染不同组织的病毒可能具有不同的CpG信号,“这为识别病毒宿主组织转换提供了一种方法。”
新冠病毒及其最接近的RaTG13的ICpG水平在其谱系中最低
在这项研究中,夏旭华检测了存入GenBank 中的1252个β冠状病毒全长基因组。GenBank是美国国家生物技术信息中心(NCBI)建立的DNA序列数据库,包含了来自所有可获得的公共来源的DNA序列。
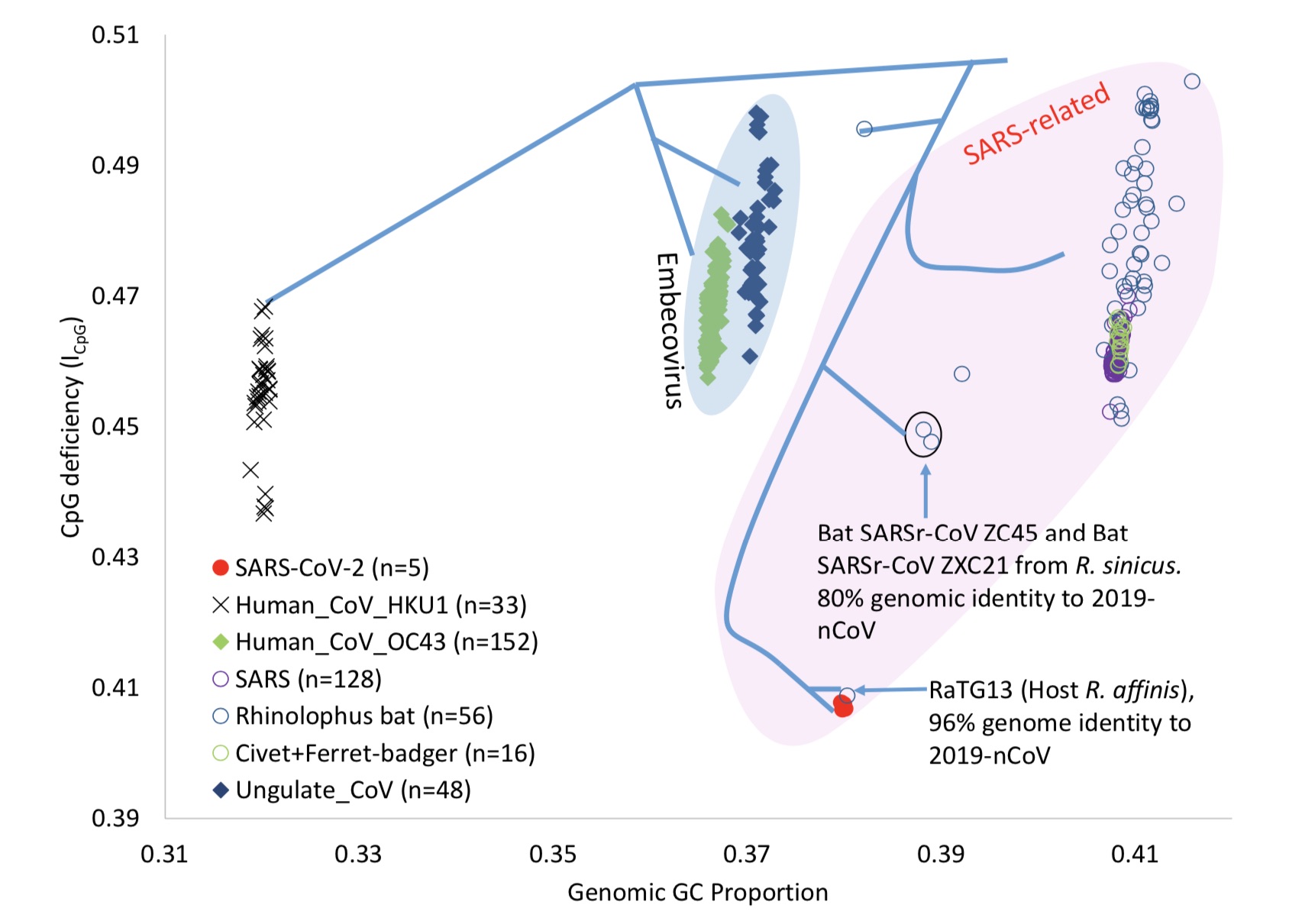
作者表示,可以看出,在同一宿主的不同病毒谱系之间,或在同一病毒谱系的不同宿主之间,基因组GC%和ICpG都存在差异。
作者认为,最引人注目的是,RaTG13 谱系中的病毒基因组CpG产生了一个孤立且急剧的下降。在此次疫情暴发之后,石正丽团队研究显示,RaTG13和新冠病毒的序列相似性为96.2%。
作者在论文写道:不幸的是,RaTG13在2013年没有被测序,否则ICpG的下降可能是一个警告,因为有两个非常重要的含义。
首先,该病毒可能是在一个ZAP高表达的组织中进化而来,ZAP高表达有利于ICpG低的病毒基因组。第二,更重要的是,病毒的存活表明它已经成功地避开了ZAP介导的抗病毒防御。“换句话说,这种病毒已经变得鬼鬼祟祟,对人类很危险。”
此次检测得出,RaTG13基因组的ICpG值为0.40875,远低于从菊头蝠属蝙蝠物种采集的所有其他β冠状病毒基因组中观察到的ICpG值。在不同的病毒谱系基因组ICpG会有波动,但只有RaTG13 ICpG被观察到有一个非常低的值。
作者提到,这表明RaTG13和新冠病毒的祖先可能在有高表达ZAP的哺乳动物组织中进化,从而产生异常低的ICpG。这种哺乳动物组织可能不在菊头蝠体内,因为在其他蝙蝠家族中没有发现ICpG含量较低的情况。
他认为,如果能鉴定出ICpG含量相对较低的病毒,就意味着候选宿主物种的组织细胞环境对病毒基因组中的CpG有很强的选择性。
犬冠状病毒:新冠病毒或来源于狗?
截至2020年2月3日,GenBank提供的所有β冠状病毒中,有1127个独特基因组,其中927个基因组有明确的宿主名称。但作者提到,令人惊讶的是,不同自然宿主中没有可用的β冠状病毒基因组具有与新冠病毒和RaTG13相近的基因组ICpG和GC%组合。
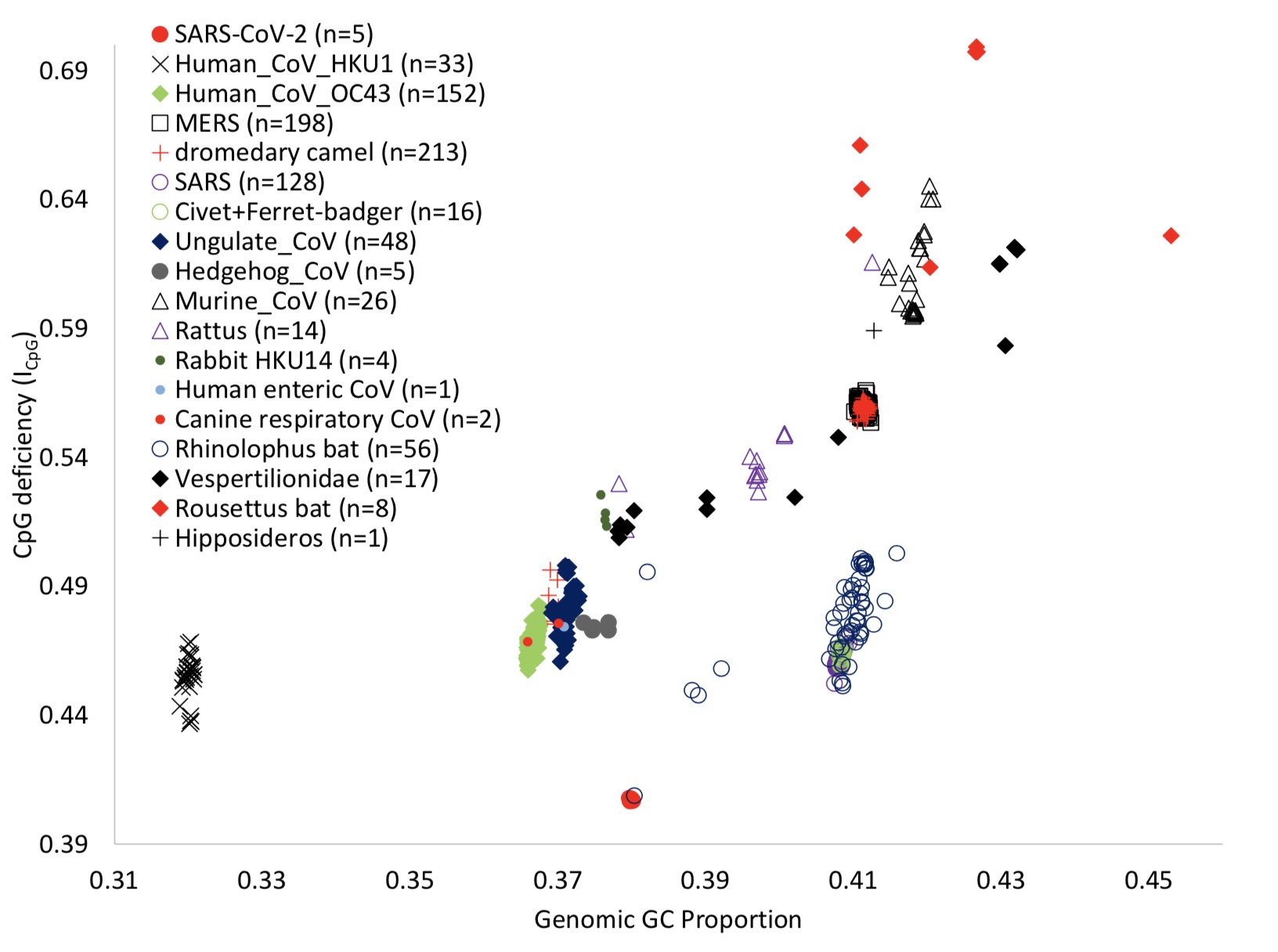
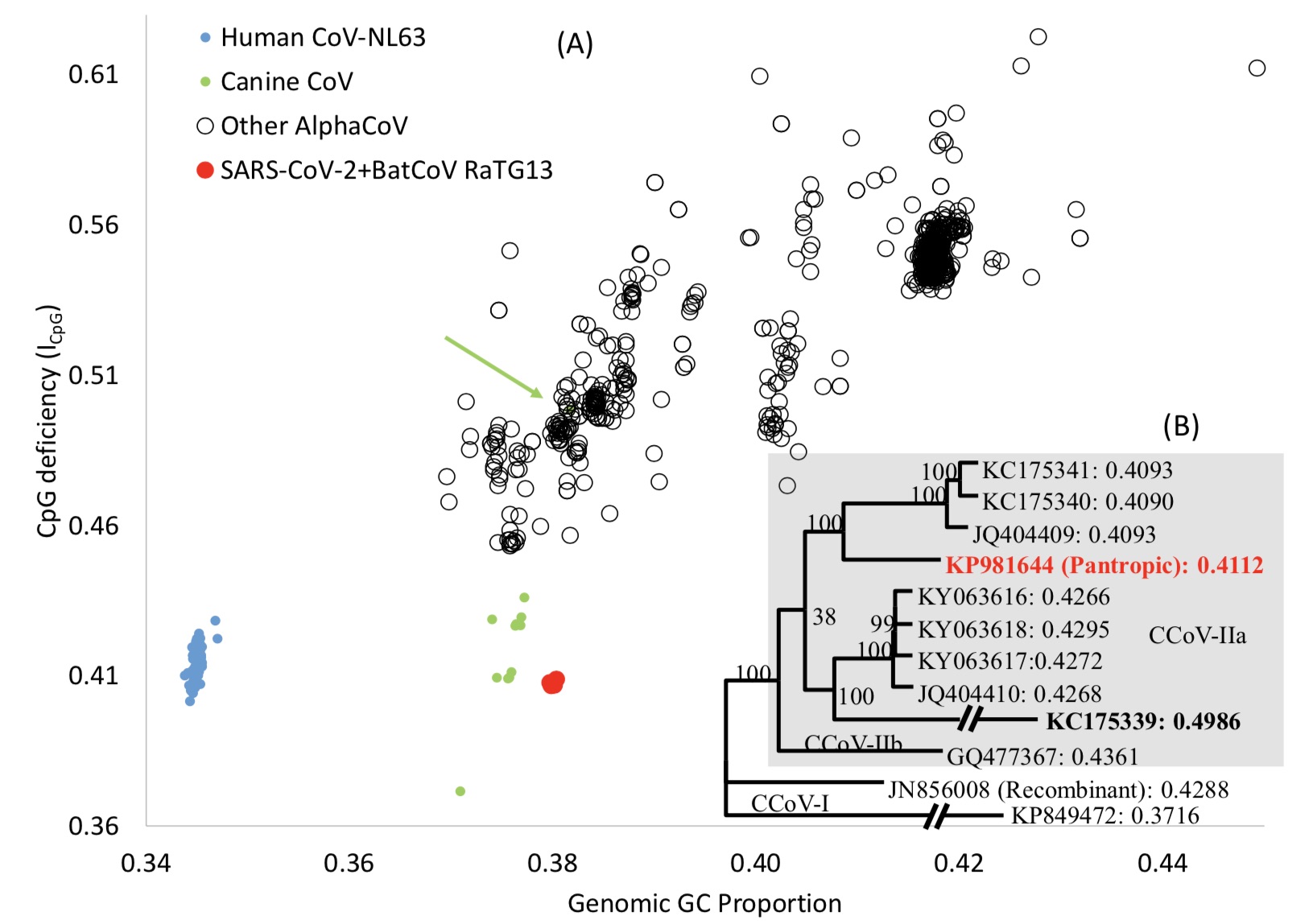
作者认为需要强调的是,犬科动物,像骆驼一样,也有冠状病毒感染它们的呼吸系统。CRCoV有两个基因组序列,它们的基因组ICpG值分别为0.4756和0.4684,显著高于感染消化系统的CCoVs(图3A)。因此,与感染骆驼的冠状病毒相似,感染犬消化系统的CCoVs的ICpG含量远低于感染犬呼吸系统的CRCoVs。
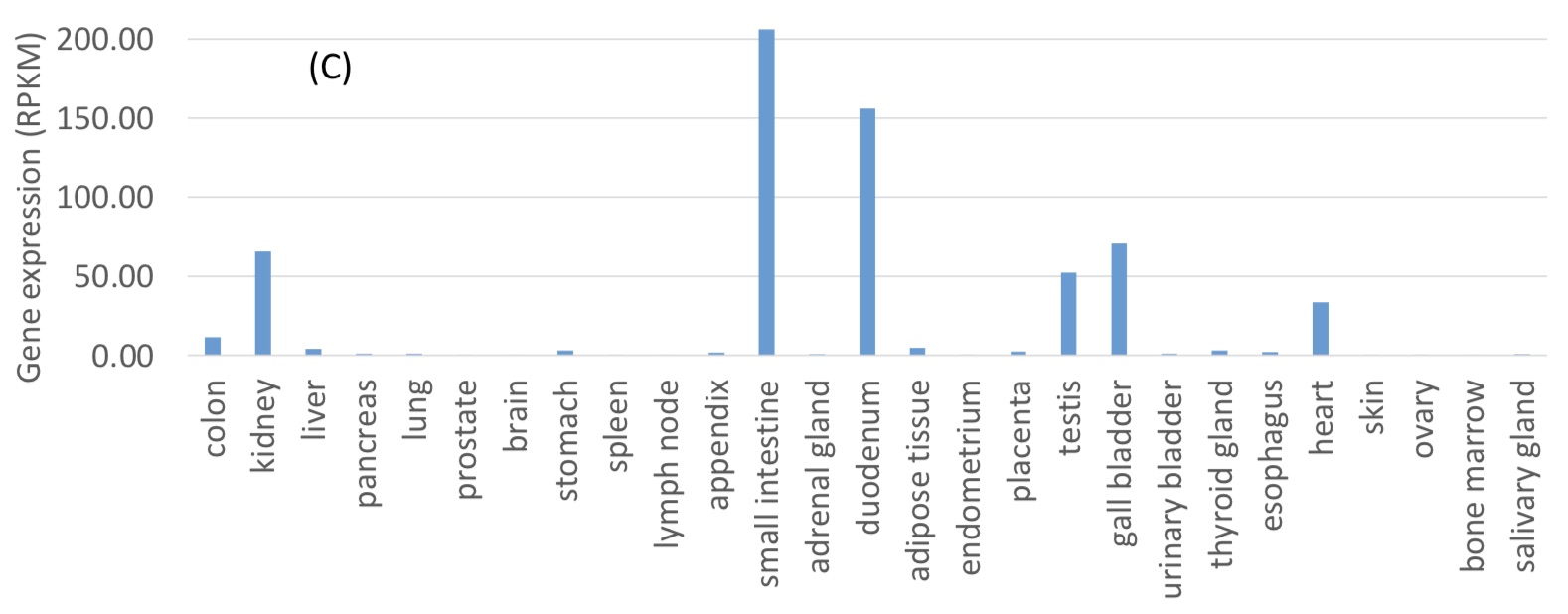
作者认为,最近的一份报告进一步证实了这一解释,即大部分COVID-19患者也有消化不适。
作者在论文中总结道,这些观察结果为新冠病毒的起源和最初传播提供了假设。首先,新冠病毒和蝙蝠来源冠状病毒RaTG13的祖先感染了一种哺乳动物的肠道(例如犬科动物或人类食用的蝙蝠肉)。第二,犬类肠病毒RNA基因组对CpG的强选择性可能导致病毒的快速进化,大量CpG到UpG 的突变导致基因组ICpG和GC%的减少。第三,犬类在交配和其他情况下会舔舐肛门区域,帮助病毒从消化系统传播到呼吸系统。最后,减少的病毒基因组ICpG使病毒逃避人类ZAP介导的免疫应答,成为一种严重的人类病原体。
他强调,这表明,在与新冠病毒的斗争中,监测野狗体内SARS样冠状病毒的重要性。
学界质疑
然而,该论文虽经过同行评议正式刊发,但却引来诸多质疑。质疑声普遍认为,这仅仅是一种假设,基于对各种冠状病毒基因组的计算机分析,一种尚未被任何既定事实证明的理论。英国剑桥大学兽医学系主任James Wood教授说,“我不认为任何狗主人会因为这项研究而感到担忧。”他认为,没有在这篇论文中看到任何支持这一假设的东西,“有太多的推论和太少的直接数据。”
美国范德比尔特大学医学院的预防医学和传染病教授、传染病专家William Schaffner不禁提问,“我们是应该担心从我们的狗身上感染病毒,还是应该担心把病毒传染给我们的狗?”他认为,这两个问题的答案都是否定的。
“这项研究是在没有任何新数据的情况下对旧数据进行重新分析的基础上进行的。”得克萨斯农工大学生物科学系主任Ben Neuman补充说,这项研究与之前一篇错误地将蛇认为是新冠病毒起源的论文有相似之处,“需要一些新的数据来最终解开新冠病毒的起源之谜,猫或狗是新冠病毒的中间宿主的结论是高度推测性的,不应该作为事实提出。”
同样,来自美国旧金山州立大学生态学和进化学专家Pleuni Pennings也认为夏旭华这篇论文中的一些数据和结论并不能成立。Pennings的团队已经检测了许多病毒的CpG水平,她认为这项研究的逻辑有弱点。
Pennings于2018年发表在PLOS Genetics杂志上的一项研究中调查了HIV病毒的CpG水平,并研究了这种病原体在人体内的进化过程。她也领导了类似的研究,研究其他几种病毒,包括登革热病毒、流感病毒、乙型和丙型肝炎病毒,了解这些病毒通过突变失去或获得CpG位点的频率。
Pennings说,产生CpG突变对病毒来说可能代价高昂,因为它们会提醒身体受到感染,所以随着时间的推移,进化力量会使它们最小化。“有许多病毒的CpG值低于新冠病毒,”她说,“当你观察所有的病毒时,CpG值一点也不奇怪。”
她补充说,夏旭华的这项研究确实发现了新冠病毒比其他动物传播的冠状病毒含有更少的CpG位点,并且假设这一发现是正确的,那么这就提出了为什么会出现这种情况的问题。Pennings说,即使有进化上的原因可以解释为什么新冠病毒失去了CpG位点,进化上的原因也不能使这种病毒在感染人类方面具有特殊优势。
针对夏旭华在论文中指出,“研究显示出病毒RNA基因组中CpG的减少与毒性增强之间的联系”,这意味着低CpG病毒似乎与更严重的感染有关。然而,Pennings提醒,CpG位点数量少的病毒一定更致命。她举例说,BK病毒含有很少的CpG位点,大约60%到80%的成年人的肾脏中都有这种病毒,但通常只会在免疫抑制的人身上引发症状。
另外还有值得注意的是,目前已有的一些研究也似乎并不支持狗在这场疫情中发挥重要作用。此前的当地时间4月8日,顶级学术期刊《科学》(Science)在线发表了中国科学院院士、中国农科院哈尔滨兽医研究所动物流感基础与防控研究创新团队首席科学家陈化兰,以及中国农业科学院哈尔滨兽医研究所所长、国家动物疫病防控高级别生物安全实验室主任步志高等人的一项研究,他们通过在P4(生物安全等级四级)实验室中进行的一系列新冠病毒感染试验发现,新冠病毒在狗、猪、鸡和鸭子身上复制效果不佳,但在雪貂和猫身上却很有效。他们还发现病毒可以通过呼吸道飞沫在猫之间传播。
实际上,新冠疫情以来,从事病毒溯源工作的一些实验团队陆续将蛇、穿山甲、猫等动物纳入了新冠病毒的疑似中间宿主名单。然而,截至目前,仍然没有一种令人信服的结论得出。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




