- +1
二甲双胍“跨界”风湿领域,靠不靠谱?
原创 小火炉 医学界风湿与肾病频道

“老药新用”?没那么简单!
二甲双胍是治疗2型糖尿病的一线药物,通过抑制肝脏中的葡萄糖生成来降低血糖水平,是目前全球控制糖尿病的核心药物。
AMPK是二甲双胍发挥作用的重要分子靶点。在体外环境中,二甲双胍可逆转糖皮质激素对AMPK的作用;在接受糖皮质激素治疗的非糖尿病患者中防止血糖恶化。在过往的一些研究中,二甲双胍治疗可能对体重、血压、血脂、凝血、炎症以及内皮细胞的代谢有益处。
身为降糖“神药”的二甲双胍,不仅在糖尿病领域地位崇高,在其他疾病领域,如肿瘤领域、感染相关领域、心血管领域等也都有它的光辉传说:二甲双胍或可提高神经胶质瘤患者生存期[1]、或可降低皮肤相关癌症风险[2]、减少糖尿病患者结核感染[3]……凭借其在多系统多领域研究的“全面开花”,着实大火了一把。
那么,二甲双胍在自身免疫性疾病中是否也能“老药新用”?
1
二甲双胍有望改善慢性炎症患者的代谢健康
在风湿免疫疾病的常规治疗中,糖皮质激素因其有效地抗炎和免疫抑制作用,成为治疗的基础用药。但是,长期过量摄入糖皮质激素会引起发育性躯干肥胖、高血压、高血糖、血脂异常、感染和血栓形成风险增高等并发症,并可能导致患者出现库欣综合征,大大增加发病率和死亡率。
为探究二甲双胍是否能逆转大量使用糖皮质激素所带来的副作用的同时,不影响激素抗炎活性,在一项发表于柳叶刀子刊的随机、双盲、安慰剂对照的II期临床研究中[4],研究人员在英国的4所医院开展试验,纳入年龄在18-75岁间、患有炎症性疾病、未被诊断为糖尿病、已持续接受剂量≥20 mg/d的泼尼松龙治疗4周或更长时间,能够在接下来12周中维持≥10 mg/d的泼尼松龙治疗的53名受试者(最终MITT 40人),随机地按照1:1分组后进行二甲双胍(n=19)或安慰剂(n=21)治疗,研究检测周期为12周。
在研究中,患者接受口服形式的二甲双胍或安慰剂片剂治疗,剂量逐渐递增,以减少胃肠道不良反应:最初5天,每天1次,每次850 mg;接下来5天,每天两次,每次850 mg;随后,每天三次,每次850 mg,一直坚持至试验结束。试验期间,每四周对受试者进行一次体检、视觉模拟评分(评估食欲、身体活动、内在疾病活动等)、采集空腹血样、检测各方面安全性和不良事件的产生。在第0和第12周,进行影像学检查和碳水化合物挑战。
研究结果显示,此次试验的主要终点,反映代谢风险的替代指标—内脏脂肪与皮下脂肪面积比,在组间未有变化[0.11 (95% CI –0.02~0.24); p=0.09]。但相较于安慰剂组,二甲双胍组患者的皮下脂肪显著减少[–3835 mm⊃2; (95% CI –6781~–888); p=0.01],内脏脂肪影响不大。次要终点,如碳水化合物、脂质、肝脏和骨代谢指标,有所改善。
此外,二甲双胍组患者的纤维蛋白溶解、颈动脉内膜中层厚度、炎症参数以及疾病活动的临床指标都得到了相应改善。在二甲双胍组,肺炎、中度至重度感染、由于不良事件导致住院的总发生率较安慰剂组低。但二甲双胍组的腹泻发生率高于安慰剂组。
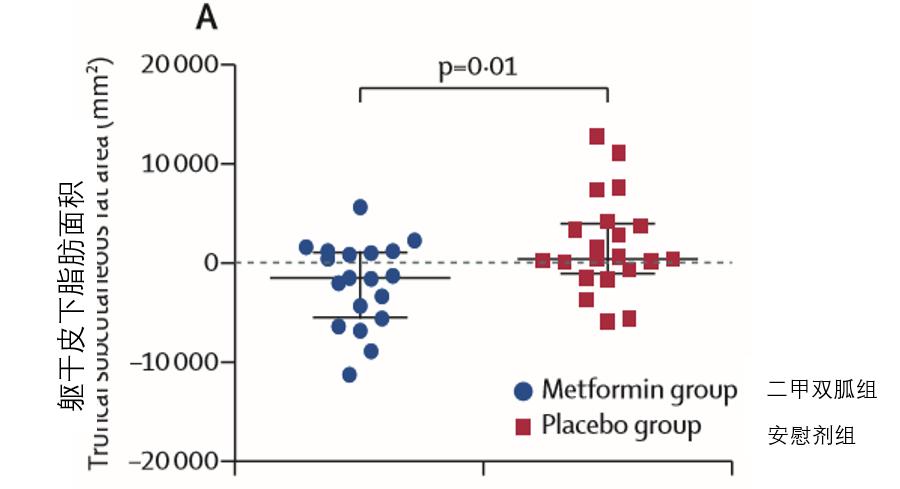
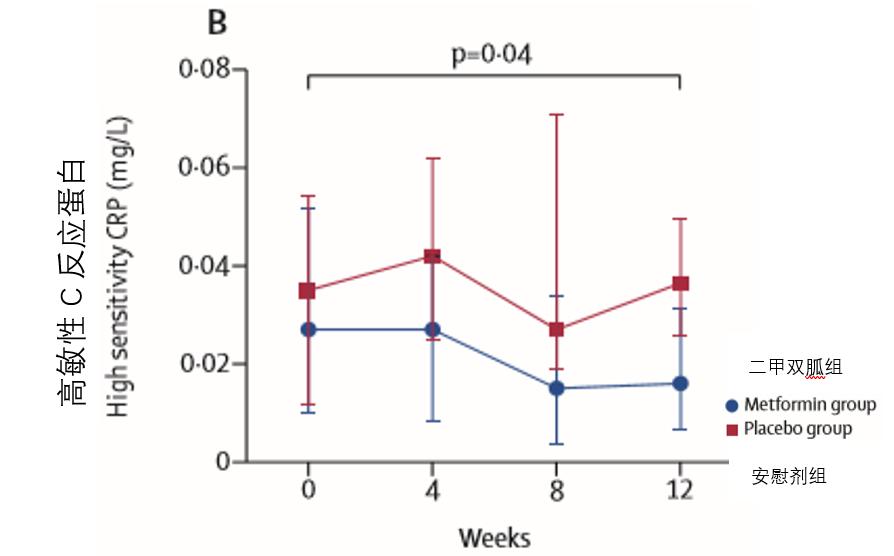
因此,二甲双胍有望改善长期使用激素治疗患者的代谢健康,减少激素过量带来的代谢并发症。
2
二甲双胍在SLE患者中的疗效与安全性
系统性红斑狼疮(SLE)是风湿性疾病中的一种,是炎性全身性自身免疫性疾病。免疫代谢参与了SLE的发病机制,二甲双胍对于治疗SLE是否有一定的疗效?
在此前的一项开放性、概念证明的试验中发现,在轻度至中度疾病活性的SLE患者的常规治疗中辅以二甲双胍,可减少疾病复发、激素用量及患者体重[5]。
接下来,该研究团队为了进一步评估二甲双胍在轻中度SLE疾病活动、无糖尿病的中国患者中的疗效和安全性,在上海的3所医院开展了多中心、随机、双盲、安慰剂对照的临床试验[6]。此次研究纳入成年SLE患者[SELENA-SLEDAI(SS)评分≤6、BILAG评分没有A或者不超过一个B]140例,他们至少发生过一次狼疮活动、在过去的12个月内接受剂量≥20 mg/d泼尼松治疗。受试者被随机地以1:1的比例分配到二甲双胍组(n=67)和安慰剂组(n=73)。
受试者在接受常规治疗的同时,随餐服用二甲双胍或安慰剂片剂:第一周服用0.5 g/d,随后每周剂量在前一周的基础上增加0.5 g,直到最大剂量为1.5 g/d(分2-3次服用)。保持服用最大剂量直至研究结束。研究周期为12个月。研究的主要终点是第12个月时的SS评分,次要终点为使用泼尼松剂量、BMI、SS评分的变化及不良事件发生率。
结果显示,研究没有达到其主要终点---两组的狼疮活动情况并未有显著差异。二甲双胍组和安慰剂组分别有14例和25例患者发生疾病活动(21% vs 34%, HR0.68, 95%CI 0.42–1.04,p=0.078)。
在次要终点的评估中,二甲双胍组患者的激素用量净变化、SS评分变化虽较安慰剂组都有所好转,但未有显著差异;而二甲双胍组患者的BMI较安慰剂组显著降低。
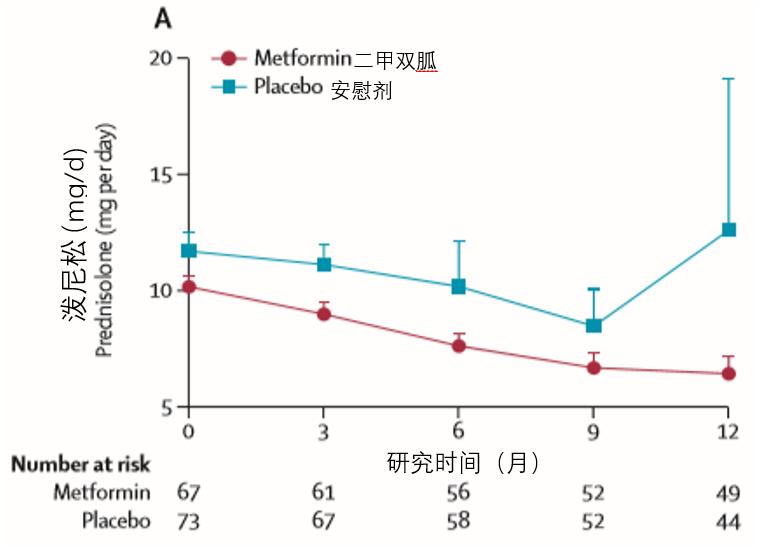
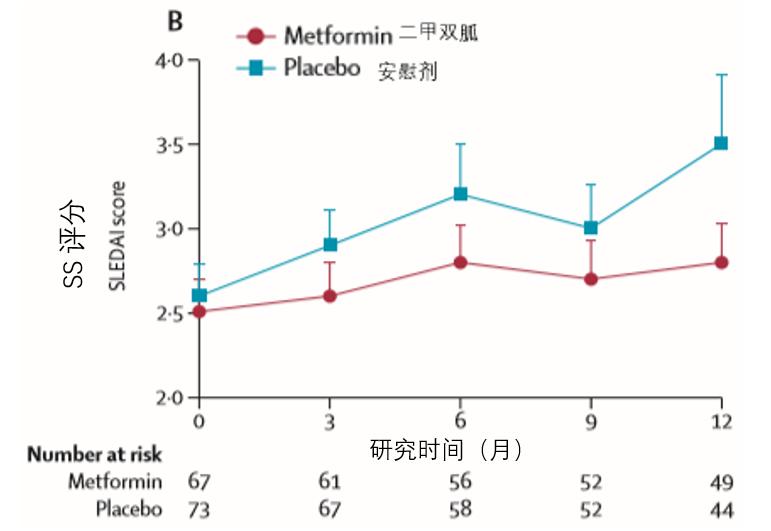
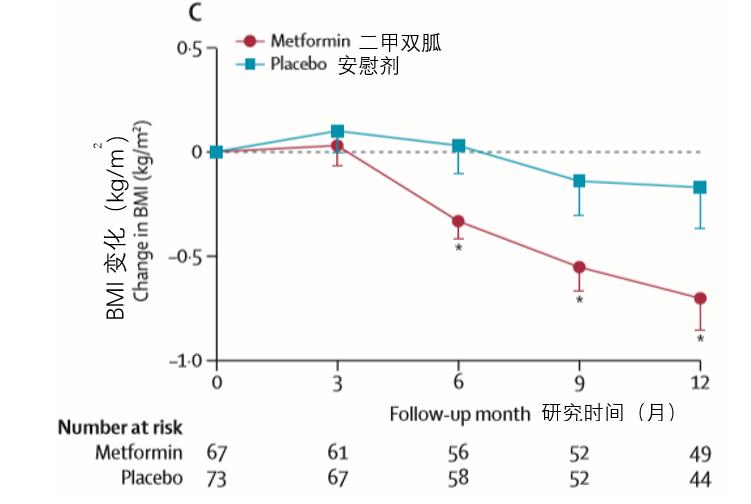
两组不良事件发生率相当,但二甲双胍组患者发生严重不良事件的次数比安慰剂组显著减少。接受二甲双胍组的患者胃肠道不良事件的发生率更高(39% vs 15%, p=0.0015)、感染率更低(25% vs 44%, p=0.022)。
此次临床研究实验未能有力证明二甲双胍,作为标准治疗的附加治疗方案,降低SLE疾病活动性的有效性。但二甲双胍的安全性良好,同时,试验也为未来更大型的相关临床研究提供了基础。
结 语
虽然目前的临床研究未能得到关于二甲双胍治疗SLE疾病的肯定疗效,但作为附加治疗,其安全性和改善激素治疗副作用的效果得到了验证。以上介绍的两项临床研究都各有其局限性,如两者有效样本量都比较少、第一项研究的次要终点检测项多、第二项研究仅选取了轻中度SLE疾病活动的患者作为受试者且局限于上海地区,结果可适性不明确等,所以应谨慎看待研究结果,期待更大规模的临床实践。
除了SLE,在治疗其他类风湿免疫疾病中,二甲双胍的研究结果也充满 “曙光”:如改善实验性类风湿关节炎、可能对骨组织起到保护作用、降低痛风患者尿酸[7]……尽管如此,不能“神化”二甲双胍的疗效,很多效果依然处于体外研究阶段或是动物实验阶段,而缺少直接的证据证明二甲双胍对于治疗自身免疫性风湿性疾病的有效性。这需要未来进一步对机制深入的研究和临床疗效的证实。
Reference:
[1] Corinna Seliger, et al. Int J Cancer. 2019; 144(2): 273–280.
[2] Tseng CH, et al. J Am Acad Dermatol. 2018; 78(4):694-700.
[3] Tseng CH, et al. J Clin Med. 2018;7(9): 264.
[4] Pernicova I, et al. Lancet Diabetes Endocrinol. 2020; DOI: 10.1016/S2213-8587(20)30021-8.
[5] Wang H, et al. ARTHRITIS & RHEUMATOLOGY. 2015; 67(12):3190-3200.
[6] Sun F, et al. Lancet Rheumatol. 2020; DOI: 10.1016/S2665-9913(20)30004-7.
[7] 陈鹏路, 等. 医学综述. 2019, 25(9): 1811-1815.
本文首发:医学界风湿与肾病频道
本文作者:小火炉
本文审核:陈新鹏 副主任医师
责任编辑:风禾
版权声明
本文原创 欢迎转发朋友圈
原标题:《二甲双胍“跨界”风湿领域,靠不靠谱?》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




