- +1
脑声常谈|觉醒与睡眠的神经环路
哺乳动物睡眠觉醒状态的神经回路调控、昼夜节律计时机制及相关睡眠障碍的病理基础。睡眠对认知、免疫功能和整体健康至关重要,睡眠障碍是常见临床问题,解析其神经调控机制具有科学和临床价值。
睡眠-觉醒状态的分类与特征
| 状态 | 心理特征 | 生理特征 | EEG 模式 | 发育变化 |
| 觉醒 | 警觉性、注意力可变 | 交感神经张力可变;肌肉活动存在 | 低振幅、快频率 | 婴儿和幼儿觉醒周期短 |
| NREM 睡眠 | 无意识或平淡思绪 | 交感神经张力低;浅 NREM 睡眠有漫游眼动 | 慢波主导(δ 波:04Hz;θ 波:47Hz) | 儿童深 NREM 睡眠丰富,成年后逐渐减少 |
| REM 睡眠 | 生动、故事性梦境 | 交感神经张力可变;快速眼动爆发;肌肉强烈抑制 | 低振幅、快活动(人类含少量 θ 波;啮齿类含大量 θ 波) | 婴儿期丰富,成年后稳定;婴儿 NREM、REM周期短 |
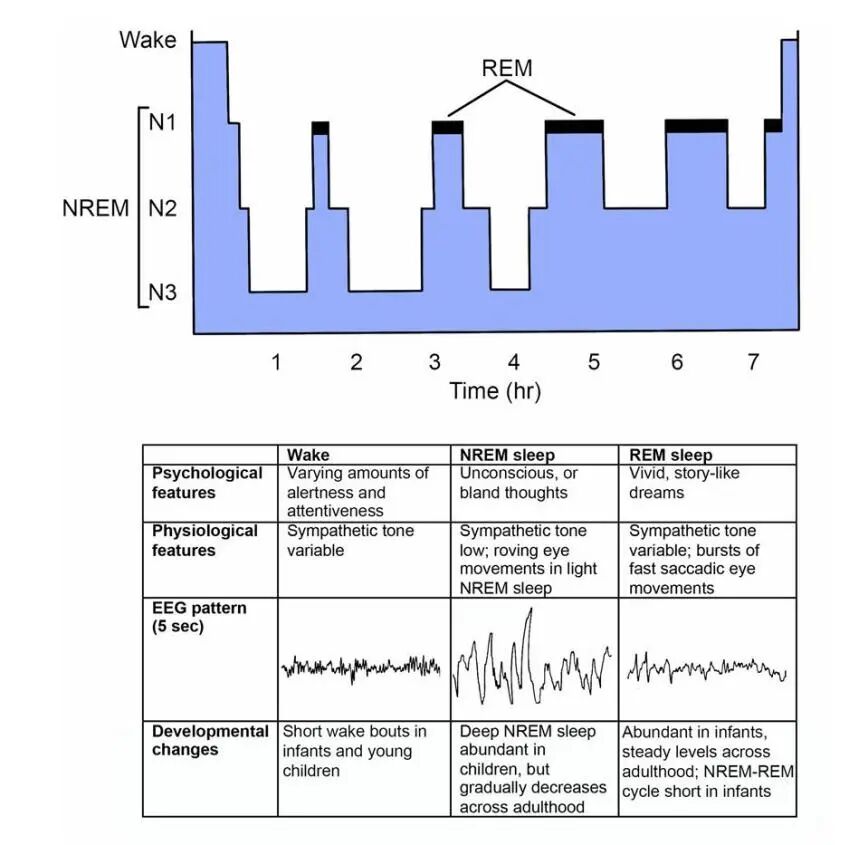
状态检测的核心生物标志物
EEG(脑电图):反映脑电活动,是区分状态的关键。觉醒时低幅快频,NREM 时慢波主导,REM 时类觉醒模式。
EMG(肌电图):反映肌肉活动,觉醒时肌肉活动可变,NREM 时保持一定肌肉张力,REM 时肌肉活动显著抑制。
生物标志物的局限性:EEG 仅为状态的间接反映并非绝对对应。例如,代谢紊乱(如肝性脑病)患者觉醒时 δ 波可能升高,苯二氮䓬类药物诱导的睡眠中 δ 波可能降低。
状态内的觉醒水平差异:觉醒状态中,觉醒程度与瞳孔直径、眼睑位置等相关;NREM 睡眠分浅(N1)、深(N3)阶段,深睡眠需更强刺激才能唤醒。
单胺类物质是调控睡眠-觉醒状态的核心神经递质家族,其功能和作用机制是理解睡眠调控的关键。
单胺类物质的分类与具体功能:
1. 去甲肾上腺素(NE)
分泌脑区:蓝斑核(LC),是前脑 NE 的主要来源。
核心功能:促进整体觉醒,尤其在响应显著刺激(如压力、新奇事物、奖励或威胁信号)时增强觉醒水平。
调控证据:激活 LC 神经元可快速唤醒睡眠中的小鼠;减少 NE 释放的药物(如 α2 激动剂)会导致镇静;LC 损伤的大鼠在复杂环境中觉醒时间显著减少。
2. 血清素(5-HT)
分泌脑区:中缝背核(DR)和正中中缝核。
核心功能:促进觉醒,直接兴奋其他觉醒促进神经元;同时参与体温调节、情绪、奖励等调控。
关键澄清:早期研究认为 5-HT 可能促眠,但后续发现,之前观察到的 “5-HT 耗竭导致失眠” 是因体温过低(5-HT 对产热至关重要),在温暖环境中该现象消失;激活 5-HT 神经元可使觉醒时间翻倍,碎片化 NREM 睡眠。
3. 多巴胺(DA)
分泌脑区:主要来自腹侧被盖区(VTA),少量来自腹侧导水管周围灰质。
核心功能:强促觉醒作用,尤其在高动机场景(如寻求美味食物、潜在配偶)中;药物(如安非他明、莫达非尼)通过增加 DA 浓度显著促醒,而 DA 拮抗剂(如抗精神病药)会导致镇静。
特殊点:VTA 的 DA 神经元没有典型 “觉醒时高放电” 模式,其觉醒调控更多依赖多巴胺转运体(DAT)活性和动机相关的通路激活。
4. 组胺(Histamine)
分泌脑区:结节乳头核(TMN),是脑内组胺的唯一神经元来源。
核心功能:促进全身性觉醒,兴奋皮层、丘脑等觉醒相关脑区;参与注意力、认知功能调控。
调控证据:组胺 H1 受体拮抗剂(抗组胺药)会导致嗜睡;缺乏组胺或 H1 受体的小鼠,黑暗期初期觉醒减少,对新环境应激的觉醒反应减弱;激活 TMN 神经元可增加运动活动,增强觉醒。
单胺类物质的共同特征与作用模式:
放电节律一致:均遵循 “觉醒(尤其主动觉醒)时高放电→NREM 睡眠时慢放电→REM 睡眠时几乎停止放电” 的规律,是区分睡眠-觉醒状态的重要神经活动标志。
投射广泛:均弥散性投射至大脑皮层、基底前脑、下丘脑等多个区域,通过调节丘脑-皮层信号传递,实现全身性觉醒调控。
功能协同且多元:除核心的觉醒调控外,还参与注意力、情绪、奖励、运动等多种生理过程,因此其对睡眠的影响可能是直接调控与间接作用(如通过动机、情绪介导)的结合。
单胺类物质是一类含单胺基团的神经递质,包括去甲肾上腺素(NE)、血清素(5-HT)、多巴胺(DA)、组胺(Histamine),主要由脑干和下丘脑的特定神经元分泌,通过广泛投射调控觉醒、注意力、情绪等功能,核心特征是觉醒时高放电、NREM 睡眠时慢放电、REM 睡眠时几乎停止放电。
睡眠相关脑区
基底前脑(Basal Forebrain, BF)
是睡眠-觉醒调控的核心脑区之一,兼具促进觉醒和调控睡眠的双重功能且通过分区、分神经元类型实现精准调控。
基底前脑是位于大脑半球腹侧、从内侧隔核延伸至无名质的脑区集合,包含胆碱能、γ 氨基丁酸(GABA)能、谷氨酸能三类核心神经元,通过广泛投射至皮层、丘脑等区域,调控皮层激活、注意力、记忆及睡眠-觉醒状态转换,是连接下丘脑、脑干与皮层的关键 “中继站”。
基底前脑的核心组成与功能:
1. 神经元类型与分布
胆碱能神经元:核心功能区从内侧隔核延伸至无名质,是 BF 最具代表性的神经元群体,直接投射至整个皮层、杏仁核、海马体。
GABA 能神经元:数量最多,占 BF 神经元的大部分,按分子标志物(生长抑素等)可分为多个亚群,投射至皮层、丘脑中线核及其他觉醒/睡眠调控脑区。
谷氨酸能神经元:数量较少,投射至皮层和下丘脑、脑干等觉醒相关亚皮层区域,功能研究相对有限。
2. 各神经元亚群的睡眠-觉醒调控作用
2.1 胆碱能神经元:皮层激活的 “加速器”
核心功能:促进皮层快节律活动(类似觉醒和 REM 睡眠时的脑电模式),调控注意力、感觉处理、记忆和皮层可塑性。
放电特征:觉醒和 REM 睡眠时高放电,NREM 睡眠时低放电,与皮层快波活动同步。
调控表现:
抑制或损伤这类神经元:增加 NREM 睡眠的慢波活动,减少从 NREM 睡眠的觉醒次数,但不减少总觉醒时间。
激活这类神经元:抑制 NREM 睡眠的慢波活动,光激活可快速唤醒 NREM 睡眠中的小鼠,并延长后续觉醒时间。
2.2 GABA能神经元:觉醒的 “核心促进者” 与睡眠的 “调控者”
核心功能:通过不同亚群实现双向调控,是 BF 调控睡眠 觉醒的 “主力”。
关键亚群与作用:
PV阳性 GABA 能神经元:激活后显著增加觉醒时间和皮层快波活动,直接促进觉醒。
生长抑素阳性 GABA 能神经元:激活后轻度增加 NREM 睡眠,通过抑制 BF 内的觉醒相关神经元(如胆碱能神经元)间接调控睡眠。
调控表现:化学遗传激活 BF GABA 能神经元可使觉醒时间大幅延长数小时;抑制则增加 NREM 睡眠约 3 小时。
2.3 谷氨酸能神经元:睡眠-觉醒转换的 “触发器”
核心功能:促进皮层激活,参与觉醒启动,尤其在从 NREM 睡眠唤醒的过程中起作用。
放电特征:觉醒和 REM 睡眠时中度放电,与皮层快波活动相关。
调控表现:光激活可快速唤醒 NREM 睡眠中的小鼠;但化学遗传激活仅轻微减少慢波活动,不增加总觉醒时间(可能与激活方式导致的神经元放电模式差异有关)。
3. 基底前脑的核心作用机制
直接调控皮层:三类神经元均直接投射至皮层,通过释放神经递质(乙酰胆碱、GABA、谷氨酸)调节皮层神经元兴奋性,进而影响脑电节律(快波/慢波)和意识状态。
间接整合信号:通过接收下丘脑(如食欲素神经元)、脑干(如单胺能神经元)的输入信号,整合觉醒促进和睡眠促进信号,实现状态转换的精准调控。
局部环路交互:BF 内部神经元间存在广泛连接(如 GABA 能神经元抑制胆碱能神经元),形成局部调控网络,精细调节觉醒水平和睡眠质量。
脚桥被盖核(PPT)和背外侧被盖核(LDT)
是位于脑桥与中脑交界处的相邻核团,合称 PPT/LDT,核心由胆碱能、γ-氨基丁酸(GABA)能、谷氨酸能三类神经元组成,主要功能是调控 REM 睡眠启动与维持、抑制皮层慢波活动,同时参与觉醒状态的皮层激活,是连接脑干与前脑的重要 “信号中继站”。
1. 解剖学定位
位于脑桥和中脑的交界区域,是脑干上部的核心核团,与蓝斑核(LC)、中缝背核(DR)等觉醒相关核团相邻且存在广泛神经连接。两者在解剖结构上紧密相连,功能高度协同,因此常被合称为 PPT/LDT 复合体。
2. 神经元类型(三类核心亚群)
胆碱能神经元:最具代表性的亚群,是脑内重要的乙酰胆碱分泌源之一,投射范围广泛。
GABA 能神经元:抑制性神经元,参与局部环路调控和远端靶区的抑制性信号传递。
谷氨酸能神经元:兴奋性神经元,近年被证实是调控睡眠-觉醒状态的关键亚群,功能研究逐渐深入。
核心功能:睡眠-觉醒调控的关键作用
1. 调控 REM 睡眠(核心功能)
触发 REM 睡眠转换:胆碱能神经元在 REM 睡眠启动前开始高放电,光激活 PPT/LDT 胆碱能神经元可促进从 NREM 睡眠向 REM 睡眠转换。
调制 REM 睡眠特征:参与调控 REM 睡眠时的皮层快波活动(类似觉醒时的脑电模式),同时与脑桥背外侧被盖核(SLD)协同,间接影响 REM 睡眠时的肌肉失张力和快速眼动。
放电节律:胆碱能和谷氨酸能神经元在 REM 睡眠和觉醒时高放电,NREM 睡眠时低放电,与 REM 睡眠的启动和维持同步。
2. 抑制皮层慢波活动,促进皮层激活
PPT/LDT 的胆碱能神经元通过投射至丘脑,兴奋丘脑-皮层神经元,抑制 NREM 睡眠时的慢波(δ 波)活动,增强皮层兴奋性。
光激活 PPT/LDT 胆碱能神经元可减少癫痫发作时的慢波活动,化学遗传激活则能强烈抑制 NREM 睡眠的慢波,体现其对皮层节律的调控作用。
3. 参与觉醒状态的调制
虽然核心功能聚焦 REM 睡眠,但 PPT/LDT 的谷氨酸能神经元被化学遗传激活后,可显著延长觉醒时间,说明其在觉醒维持中也发挥辅助作用。
与基底前脑、丘脑等区域形成通路,整合觉醒促进信号,参与注意力、感觉处理等觉醒相关功能的调控。
关键调控通路与机制:
1. 输入通路(接收信号)
接收来自下丘脑食欲素神经元的兴奋性输入:食欲素可激活 PPT/LDT 的胆碱能和谷氨酸能神经元,增强其调控睡眠 觉醒转换的功能。
接收来自单胺能核团(LC、DR)的抑制性输入:觉醒时,LC 的去甲肾上腺素(NE)、DR 的血清素(5HT)抑制 PPT/LDT 神经元,避免 REM 睡眠在觉醒时启动;REM 睡眠时,单胺能神经元放电停止,这种抑制解除,PPT/LDT 神经元激活。
2. 输出通路(传递信号)
上行投射:至丘脑、基底前脑、皮层,调控皮层节律和意识状态。
下行投射:至脑桥 SLD(REM 睡眠核心核团),通过乙酰胆碱兴奋 SLD 的谷氨酸能神经元,间接介导 REM 睡眠的肌肉失张力和脑电特征。
臂旁核(PB)
是睡眠-觉醒调控与感觉信号整合的核心枢纽,其功能直接关联意识维持和睡眠障碍相关机制。臂旁核是位于脑桥的关键核团,核心由谷氨酸能神经元组成,主要功能是传递感觉信号、调控觉醒状态,同时参与呼吸、疼痛等内感受刺激的唤醒反应,损伤会导致昏迷或持续性植物状态,是维持意识和正常睡眠-觉醒转换的必需脑区。
位于脑桥上部,与中脑、延髓相邻,是连接脑干、下丘脑与前脑的重要 “中继站”。紧密连接觉醒调控核心脑区(如基底前脑、下丘脑)和感觉处理通路,兼具信号传递和状态调控双重作用。以谷氨酸能神经元为主,是其发挥觉醒调控和信号传递功能的核心。按亚区可分为内侧臂旁核(mPB)和外侧臂旁核(lPB),亚区功能存在分工,分别参与不同类型的信号调控。
核心功能:觉醒调控与感觉整合
1. 强觉醒促进作用(核心功能)
内侧臂旁核(mPB):通过密集投射至基底前脑(BF),释放谷氨酸激活觉醒促进神经元,直接增强觉醒;破坏 mPB 神经元或阻断其谷氨酸信号,会导致觉醒时间减少,NREM 睡眠的 δ 波功率增加(睡眠加深)。
维持意识必需:动物或人类的 PB 区域损伤,会引发昏迷或持续性植物状态(清醒但无反应),证明其对意识维持和觉醒启动的关键作用。
2. 响应内感受刺激,触发针对性觉醒
外侧臂旁核(lPB):被高碳酸血症(血液中二氧化碳升高)、疼痛、寒冷、恶心等内感受刺激激活。
临床关联:在阻塞性睡眠呼吸暂停模型中,lPB 的谷氨酸信号受损会延迟高碳酸血症引发的觉醒,导致睡眠中呼吸暂停时间延长,凸显其在睡眠中危险信号唤醒的重要性。
3. 整合感觉与睡眠-觉醒信号
作为感觉信号(尤其是痛觉、呼吸相关信号)向中枢传递的关键节点,将外周刺激转化为觉醒信号,确保机体在面临危险或生理失衡时能及时从睡眠中唤醒。与下丘脑、基底前脑等睡眠-觉醒核心区形成双向通路,实现信号整合与状态调控的协同。
关键调控通路
1. 输入通路(接收信号)
接收来自外周的感觉信号:包括呼吸、疼痛、温度、代谢状态等内感受信息。
接收来自脑干其他核团的调控信号:与睡眠 觉醒相关的单胺能核团、食欲素神经元等存在功能连接,整合觉醒促进与抑制信号。
2. 输出通路(传递信号)
上行投射:至基底前脑(BF)、下丘脑等觉醒调控区,通过谷氨酸能信号激活觉醒相关神经元,启动或维持觉醒。
参与全身生理调控:投射至下丘脑室旁核(PVN)等区域,同时调控自主神经功能(如呼吸、心率)与睡眠-觉醒状态,实现生理功能与意识状态的协同。
食欲素(Orexins)
是调控睡眠-觉醒平衡的核心神经肽,其功能异常直接关联重大睡眠障碍,是理解觉醒维持机制的关键。食欲素是由外侧下丘脑(LH)神经元分泌的两种神经肽通过结合OX1R和 OX2R受体,广泛激活所有觉醒促进脑区,核心功能是维持长时间觉醒、稳定睡眠-觉醒周期,同时参与应激、奖励寻求等动机相关行为调控,其神经元选择性缺失会导致发作性睡病。
1. 分泌部位与神经元分布
仅由LH 的特定神经元分泌,这些神经元散在于外侧下丘脑区域,数量虽少,但投射范围极其广泛。
除分泌食欲素外,还共同释放谷氨酸(兴奋性神经递质)和强啡肽(抑制性神经肽),通过协同作用调控靶区神经元活性。
2. 分子类型与受体
两种亚型:食欲素A(OrexinA)和食欲素B(OrexinB),均为小分子多肽,其中食欲素A的生物学活性更强、作用更持久。
两类受体:OX1R(主要结合食欲素A)和OX2R(可结合两种食欲素),广泛表达于皮层、丘脑、脑干觉醒相关核团(蓝斑核、结节乳头核等)。
核心功能:睡眠-觉醒调控的 “稳定剂”
1. 维持长时间觉醒(核心功能)
食欲素神经元在觉醒期(尤其主动觉醒)高放电,REM 睡眠时几乎停止放电,与觉醒状态高度同步。
作用机制:通过兴奋性信号激活所有觉醒促进系统(单胺能、胆碱能、谷氨酸能神经元),增强其放电活性,避免觉醒状态快速消退。
实验证据:侧脑室注射食欲素A可显著延长觉醒时间、抑制REM睡眠数小时;光激活或化学遗传激活食欲素神经元,能快速唤醒睡眠中的小鼠,并维持长时间觉醒。
2. 稳定睡眠-觉醒周期,防止异常转换
避免觉醒向 REM 睡眠突然切换:食欲素通过持续抑制 REM 睡眠促进通路(如脑桥 SLD 核团),阻止觉醒状态下突然进入 REM 睡眠(发作性睡病的典型症状)。
调控觉醒质量:增强觉醒状态的稳定性,减少碎片化觉醒,使机体能维持持续的认知、运动功能。
3. 参与动机与应激相关的觉醒调控
应激与奖励寻求:在面临应激、寻求食物/配偶等高动机场景时,食欲素神经元活性显著增强,通过提升觉醒水平支持目标导向行为。
稳态挑战应对:如食物剥夺时,食欲素介导的觉醒增加,鼓励动物主动觅食;缺乏食欲素的小鼠,饥饿时几乎无觉醒增强反应。
关键调控通路与机制:
1. 输入通路(接收调控信号)
接收来自下丘脑、脑干的多重信号:包括能量代谢信号(如瘦素、饥饿信号)、应激信号、昼夜节律信号(来自视交叉上核 SCN),整合机体状态与环境信息,精准调控食欲素释放。
睡眠压力信号:长时间觉醒后,腺苷等促眠因子会间接抑制食欲素神经元活性,为睡眠启动做准备。
2. 输出通路(作用靶区)
广泛投射至所有觉醒促进脑区:包括蓝斑核(NE)、结节乳头核(组胺)、中缝背核、腹侧被盖区(DA)、基底前脑(胆碱能)、臂旁核(谷氨酸能)等,形成 “一源多靶” 的调控网络。
核心作用模式:通过谷氨酸快速激活靶区神经元,同时通过食欲素的长效兴奋作用,维持靶区持续放电,实现觉醒的稳定维持。
临床关联:与睡眠障碍的核心联系
发作性睡病的直接病因:人类发作性睡病患者(尤其是伴猝倒型),其食欲素神经元会选择性缺失(可能与自身免疫相关),导致食欲素水平显著降低或检测不到。
症状对应机制:患者表现为慢性严重嗜睡(觉醒维持能力丧失)、REM 睡眠紊乱(觉醒时突然进入 REM 睡眠、睡眠中 REM 片段混入觉醒),与食欲素的功能缺失完全吻合。
治疗靶点:OX2R 激动剂可改善发作性睡病患者的嗜睡症状;食欲素拮抗剂则可用于治疗失眠(通过抑制觉醒促进信号,促进睡眠)。
LH和后下丘脑(PH)是睡眠-觉醒与动机行为整合的核心枢纽,不仅直接调控觉醒维持,还通过与多个脑区协同,实现生理需求与意识状态的精准匹配。
外侧下丘脑(LH)和后下丘脑(PH)
是下丘脑的关键功能区,主要通过 GABA 能神经元、食欲素神经元(仅 LH 含)等亚群,直接促进觉醒、调控睡眠-觉醒转换,同时整合饥饿、奖励等动机信号,损伤会导致严重嗜睡;两者功能协同,是连接觉醒调控、动机行为与生理稳态的核心脑区。
外侧下丘脑(LH):位于下丘脑外侧部,与基底前脑、脑桥等觉醒调控区相邻,是食欲素神经元的唯一分布区,也是动机行为(如觅食、奖励寻求)的重要调控位点。
后下丘脑(PH):位于下丘脑后部,与中脑、丘脑相连,与 LH 解剖结构连续,功能高度协同。
1. 核心神经元类型
LH 关键神经元:
食欲素神经元:分泌食欲素 A/B和谷氨酸,是LH调控觉醒的核心亚群。
GABA 能神经元:多个亚群,分别投射至丘脑网状核、睡眠促进脑区(如 VLPO),通过抑制睡眠通路或激活觉醒相关环路直接促醒。
PH 关键神经元:以GABA能神经元为主,与LH的GABA能神经元形成功能网络,共同参与觉醒维持和动机相关的觉醒调控。
核心功能:觉醒调控与动机整合
1. 强觉醒促进作用(核心功能)
直接促醒机制:
LH 的 GABA 能神经元:光激活可快速唤醒 NREM 睡眠中的小鼠;化学遗传激活能延长觉醒数小时;抑制则增加 NREM 睡眠慢波活动(睡眠加深)。
PH 与 LH 协同:临床观察显示,LH/PH 区域损伤会导致患者每日睡眠 1520 小时,唤醒后冷漠且快速复睡,证明其对觉醒维持的必需性。
与食欲素的协同:LH 的 GABA 能神经元与食欲素神经元共同投射至觉醒促进脑区(如 LC、TMN),形成 “兴奋性 + 抑制性” 协同调控,增强觉醒稳定性。
2. 整合动机与生理需求,调控针对性觉醒
饥饿与觅食:LH/PH 的 GABA 能神经元被饥饿信号激活,通过促进觉醒鼓励动物主动觅食;缺乏 LH 神经元的小鼠,饥饿时无法产生觉醒增强反应。
奖励寻求:LH/PH 神经元与腹侧被盖核(VTA,多巴胺能核团)形成通路,在寻求美味食物、潜在配偶等高动机场景中,激活觉醒通路,提升觉醒水平以支持目标行为。
稳态挑战应对:如应激、代谢失衡时,LH/PH 整合信号并增强觉醒,帮助机体应对危机。
3. 调控睡眠-觉醒转换的稳定性
通过抑制睡眠促进通路:LH 的 GABA 能神经元投射至视前区(VLPO,NREM 睡眠核心促进区),通过释放 GABA 抑制 VLPO 神经元,阻止睡眠过度延长。
避免觉醒碎片化:与食欲素神经元协同,维持长时间连续觉醒,减少觉醒与睡眠的频繁切换。
关键调控通路:
1. 输入通路(接收信号)
生理需求信号:接收饥饿(如瘦素、 ghrelin 信号)、能量代谢、应激等稳态信息。
动机与奖励信号:接收来自 VTA、伏隔核等奖励通路的信号,整合 “需求-奖励” 关联。
昼夜节律信号:接收来自视交叉上核(SCN)的节律信号,同步觉醒-睡眠与光照周期。
2. 输出通路(传递信号)
觉醒促进通路:投射至LC、TMN、BF等觉醒核心区,通过 GABA 或谷氨酸信号激活靶区神经元,直接促醒。
睡眠抑制通路:投射至 VLPO、 脑干面神经旁核(PZ)等睡眠促进区,通过 GABA 抑制睡眠通路,间接增强觉醒。
动机-觉醒整合通路:投射至 VTA、纹状体等,将动机信号转化为觉醒驱动,实现 “需求-觉醒” 联动。
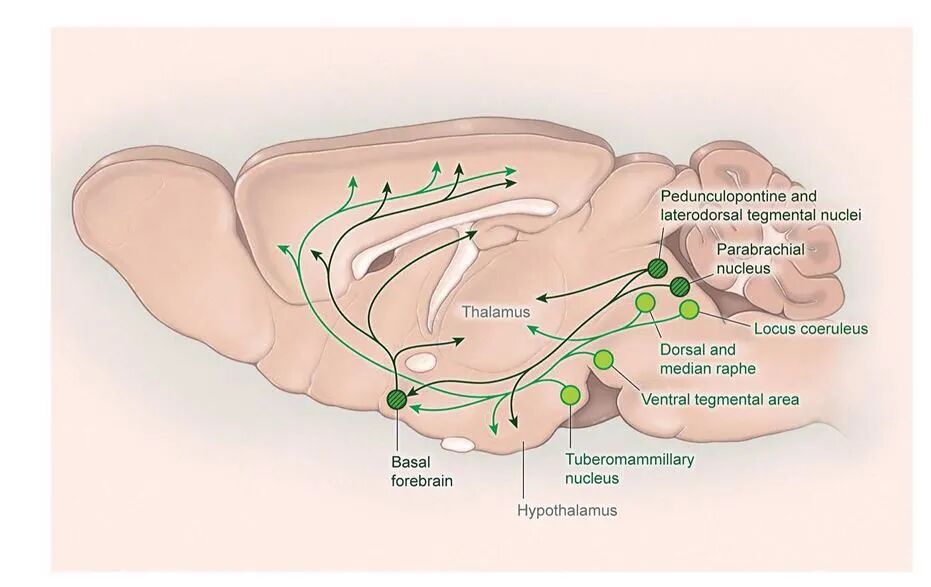
图一 睡眠生理学特征
多种神经化学系统促进觉醒,并引发觉醒状态下典型的快速皮层活动。位于脑干前端和下丘脑后部的单胺能神经元直接投射至大脑皮层,同时也广泛支配包括下丘脑和丘脑在内的多个皮层下区域。这些单胺能系统包括:蓝斑核的去甲肾上腺素能神经元,背侧缝核和中缝核的5-羟色胺能(血清素能)神经元,腹侧被盖区的多巴胺能神经元,结节乳头体核的组胺能神经元。
此外,促觉醒信号还来源于臂旁核以及胆碱能区域,包括脚桥被盖核、背外和基底前脑等。
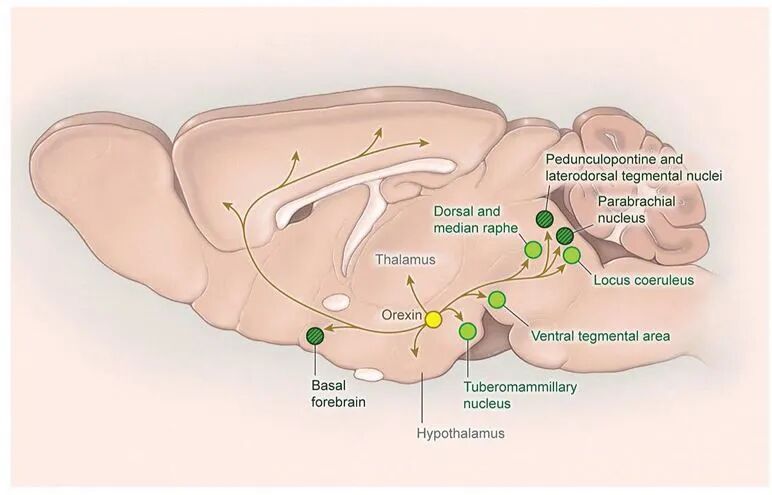
图二 食欲素神经元的投射
食欲素神经肽由外侧下丘脑的神经元产生,可兴奋大脑皮层、中线丘脑以及所有促觉醒脑区的神经元。
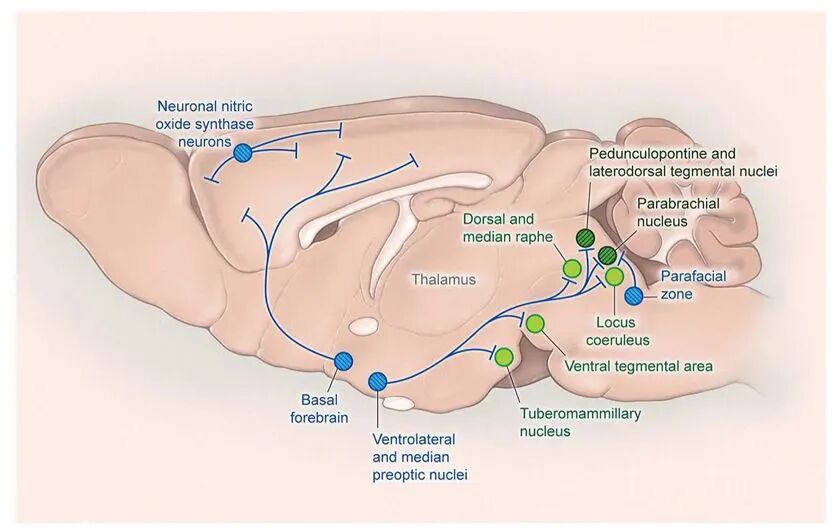
图三 NREM睡眠促进通路
腹外侧视前区(VLPO)和正中视前核(MnPO)中的GABA能神经元通过抑制位于下丘脑后部和脑干的促觉醒神经元来促进睡眠。
BF也包含在睡眠期间活跃的神经元,它们可能通过基底前脑内部的投射以及直接投射至皮层来促进睡眠。NREM 睡眠由多个脑区协同调控,形成以“相互抑制”和“促眠信号整合”为核心的动态回路。视前区(POA)是睡眠“启动器”,其 VLPO 和 MnPO 的 GABA/galanin 能神经元直接抑制蓝斑核、结节乳头体核等觉醒中枢并受腺苷激活,与觉醒系统构成双稳态开关;基底前脑作为“皮层调控器”,通过生长抑素阳性 GABA 能神经元抑制局部觉醒信号并投射至皮层,促进 δ 慢波同步;PZ是脑干“促眠中枢”,其 GABA/甘氨酸能神经元在 NREM 期特异性活跃,通过抑制臂旁核阻断觉醒上行通路对深度睡眠至关重要;皮层则含nNOS阳性GABA能中间神经元,通过释放GABA和一氧化氮同步局部慢波,其活性随睡眠压力增强,缺失 nNOS 会削弱 NREM 时长与反弹能力。整体上,POA 启动睡眠,PZ 维持稳定性,BF与皮层精细调控慢波质量,共同保障 NREM 睡眠的时长、深度与恢复功能。
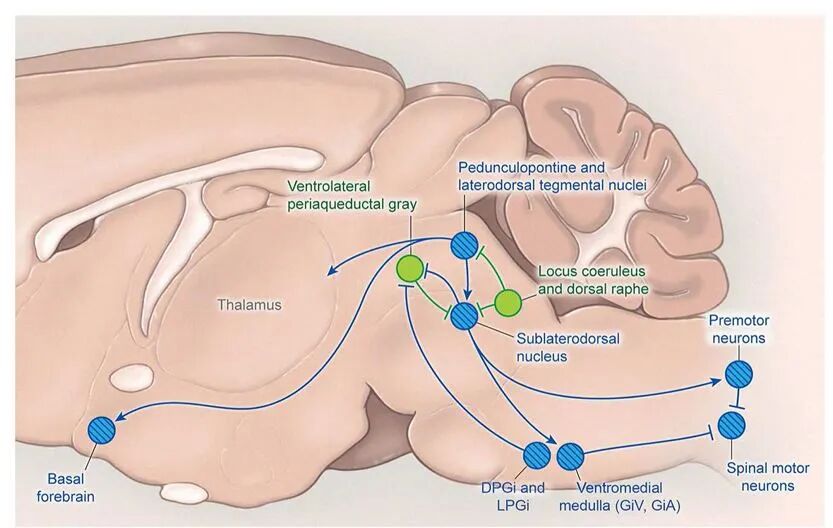
图四 REM睡眠促进通路
SLD在调控REM睡眠中起核心作用。SLD中的谷氨酸能神经元通过兴奋延髓腹内侧和脊髓中的GABA能/甘氨酸能神经元,使运动神经元超极化,从而引发REM睡眠特征性的肌肉麻痹(肌张力缺失)。
此外,PPT和LDT的胆碱能神经元也促进REM睡眠,并可能驱动REM期典型的快速脑电活动(低幅快波EEG)。
在觉醒和NREM睡眠期间,SLD受到以下区域的抑制:
导水管周围灰质腹外侧部(vlPAG)及邻近的外侧脑桥被盖的GABA能神经元以及蓝斑核和缝核的单胺能神经元。而在REM睡眠期间,vlPAG很可能被SLD和延髓中的GABA能神经元反过来抑制从而解除对SLD的抑制,形成REM睡眠的“去抑制”启动机制。
REM睡眠的调控依赖于一系列复杂且相互作用的神经回路,核心是SLD的谷氨酸能神经元。这些神经元通过与多个脑区形成“相互抑制回路”,协同延髓、下丘脑等区域,实现REM睡眠的启动、维持及特征调控。
通过上述多层次、多脑区的协同调控,REM睡眠得以精确启动、维持并表现出其特有的生理特征。
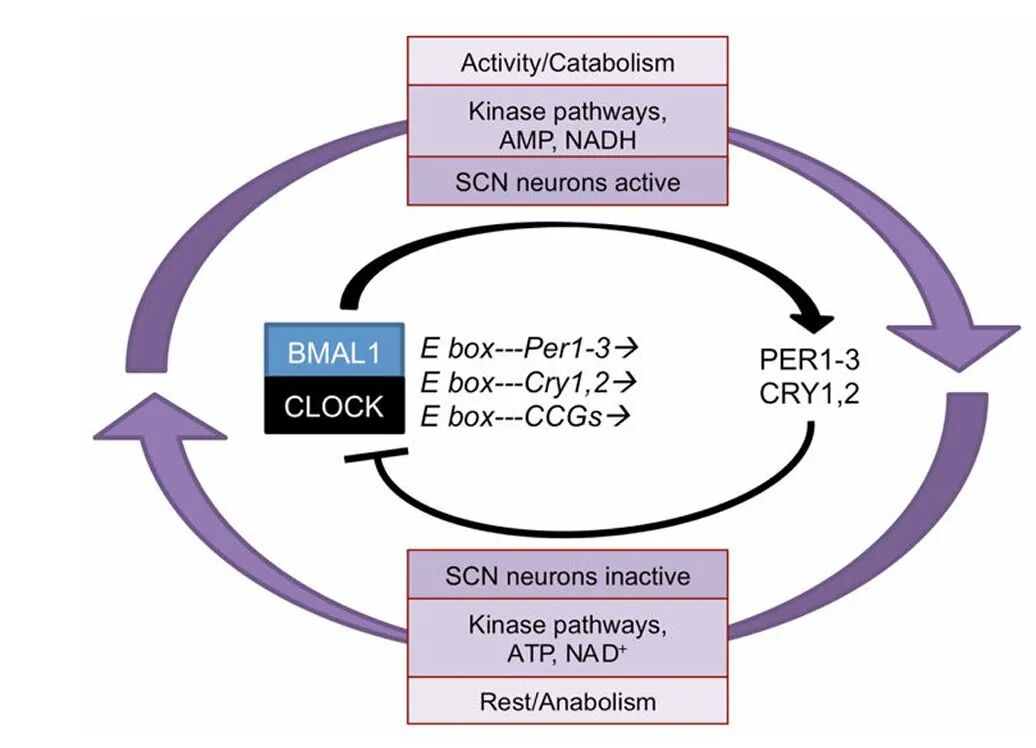
图五 细胞内的昼夜节律由转录翻译反馈环路和翻译后调控机制共同协调
昼夜节律的核心是BMAL1/CLOCK–Per/Cry负反馈环路:BMAL1与CLOCK激PerCry转录,其蛋白产物积累后回核抑制BMAL1/CLOCK活性,形成约24小时振荡。该分子钟受激酶活性、AMP/ATP及NAD⁺/NADH等代谢信号微调,耦合细胞生理与时间调控。
在系统层面,SCN作为“主生物钟”接收视网膜光信号(经RHT),通过VIP/AVP实现内部同步,并驱动节律输出。光照(由ipRGCs感知蓝光)校准SCN相位,褪黑素夜间反馈抑制SCN以促进睡眠。
SCN通过SCN→SPZ→DMH通路调控睡眠-觉醒时序:白天DMH兴奋食欲素神经元和蓝斑核促进觉醒,夜间解除对VLPO的抑制以启动睡眠,确保行为与环境光暗周期精准同步。得注意的是,昼夜节律系统决定“何时睡”,而睡眠稳态系统(如腺苷积累)决定“睡多深、多久”,二者协同维持健康睡眠结构。
节律紊乱(如熬夜、倒班、跨时区)可导致失眠、代谢异常、情绪障碍甚至神经退行性疾病。临床干预如光照疗法和褪黑素补充,正是通过重置SCN节律来改善睡眠时相障碍。
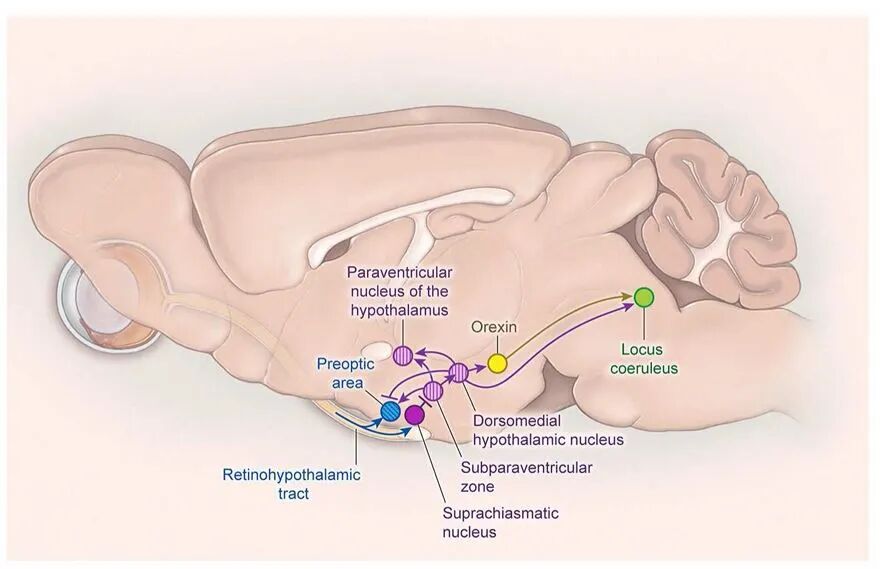
图六 调控睡眠及其他节律昼夜时间的神经通路
SCN神经元能自主产生昼夜节律,并通过视网膜下丘脑束(RHT)接收视网膜的直接光输入,与外界光-暗周期同步;RHT还发出少量投射,可能直接调节视前区促睡神经元的活动。SCN的大部分输出经由SPZ中继至DMH,后者作为关键整合中枢:白天通过兴奋性投射激活外侧下丘脑的食欲素神经元和脑干蓝斑核以促进觉醒,同时通过抑制性投射抑制视前区,防止睡眠过早发生,从而精准调控觉醒时序。此外,SPZ和DMH还协调心率、血压、体温、运动和摄食等生理功能的昼夜节律;而SCN另经PVN调控松果体褪黑激素的昼夜分泌,同步外周生物钟。
综上,SCN作为中央起搏器,通过多级下游通路统筹睡眠-觉醒与其他生理节律,实现机体与地球24小时环境周期的精准同步。
总结
系统解析睡眠觉醒调控环路的多层次机制,有助于了解从分子、细胞到神经网络水平的动态互作如何共同塑造复杂的睡眠行为。这些发现为理解失眠、嗜睡等睡眠障碍的神经基础提供了关键线索,也为开发靶向特定环路或细胞类型的精准干预策略奠定了理论基础。
文章来源:
Scammell TE, Arrigoni E, Lipton JO. Neural Circuitry of Wakefulness and Sleep. Neuron. 2017 Feb 22;93(4):747765. doi: 10.1016/j.neuron.2017.01.014. PMID: 28231463; PMCID: PMC5325713.
原标题:《脑声常谈|觉醒与睡眠的神经环路》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




