- +1
为何紧张时会心跳加速、呼吸急促?河北医科大学王升团队揭示中央杏仁核GABA能神经元分路调控焦虑与呼吸
焦虑的特征是对情绪刺激的呼吸反应失调。中央杏仁核(CeA)是处理情绪变化的关键结构,但其在协调类焦虑行为和特定呼吸模式中的作用仍未被充分探索。
基于此,2025年4月14日,河北医科大学神经生物学系王升研究团队在Nature communications杂志发表了“GABAergic neurons in central amygdala contribute to orchestrating anxiety-like behaviors and breathing patterns”揭示了中央杏仁核中的GABA能神经元有助于协调类焦虑行为和呼吸模式。

作者的研究发现,急性束缚应激(ARS)会诱导小鼠表现出类焦虑行为,表现为长时间的梳理行为和更快的呼吸频率(RF)。相反,沉默CeA中的GABA能神经元可减少ARS后的类焦虑行为,并降低相关的梳理时间延长和呼吸频率增加。在主动活动的小鼠中,激活CeA的GABA能神经元会引发类焦虑行为,同时延长梳理时间,并通过CeA-丘脑室旁核(PVT)环路加速呼吸频率。而在行为静止或麻醉的小鼠中,激活这些神经元会显著增加呼吸频率,但不会通过CeA-外侧臂旁核(LPBN)环路诱导类焦虑行为。总体而言,CeA的GABA能神经元主要通过CeA-PVT和CeA-LPBN环路分别在协调类焦虑行为和呼吸模式中发挥重要作用。
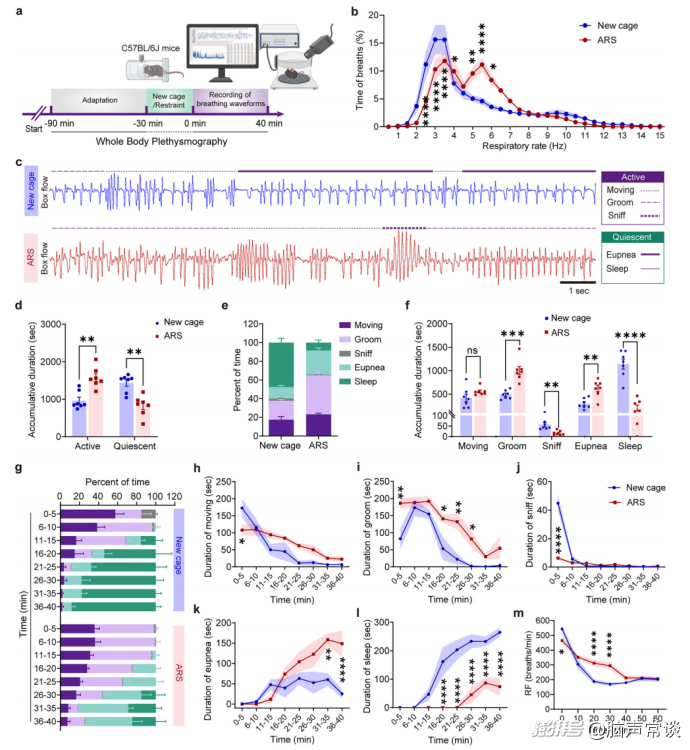
图一 急性束缚应激后小鼠的呼吸和行为变化
研究使用急性束缚应激(ARS)模型评估类焦虑行为及其相关的呼吸模式变化。C57BL/6J小鼠被分为三组:家笼对照组、新笼对照组(在行为测试前30分钟从小鼠的家笼转移到新笼中),以及经历30分钟ARS处理的ARS组,并随后进行了一系列时间点的行为评估。ARS处理的小鼠在旷场测试(OFT)中花费在中心区域的时间显著减少,休息时间延长,总体移动距离减少。在高架十字迷宫(EPM)测试中,这些小鼠进入开放臂的次数更少,停留时间更短,移动距离也缩短。这些行为差异在ARS后0至40分钟最为明显,但在50和60分钟后与新笼组相比不再明显。使用全身体描记术(WBP)分析自由活动小鼠在应激后的40分钟内的行为和呼吸变化,发现ARS小鼠的呼吸频率(RF)分布曲线向右偏移,显示出高频呼吸事件的增加。根据特定的呼吸波形和视频记录,将行为分类为活跃状态(包括移动、梳理毛发、嗅探)和静息状态(包括正常呼吸和睡眠)。结果显示,ARS小鼠的累计活跃时间显著增加,而静息时间减少,主要是由于梳理毛发时间大幅增加,嗅探时间减少且移动时间没有显著变化。睡眠时间显著减少,而正常呼吸时间延长。相关性分析显示,呼吸频率与梳理毛发时间之间存在显著正相关,表明增加的呼吸频率与焦虑水平升高有关,这通过增加的梳理行为得到体现。综上所述,本研究表明ARS诱导的小鼠表现出类焦虑行为和升高的呼吸频率,尤其是在ARS处理后的20到30分钟内。
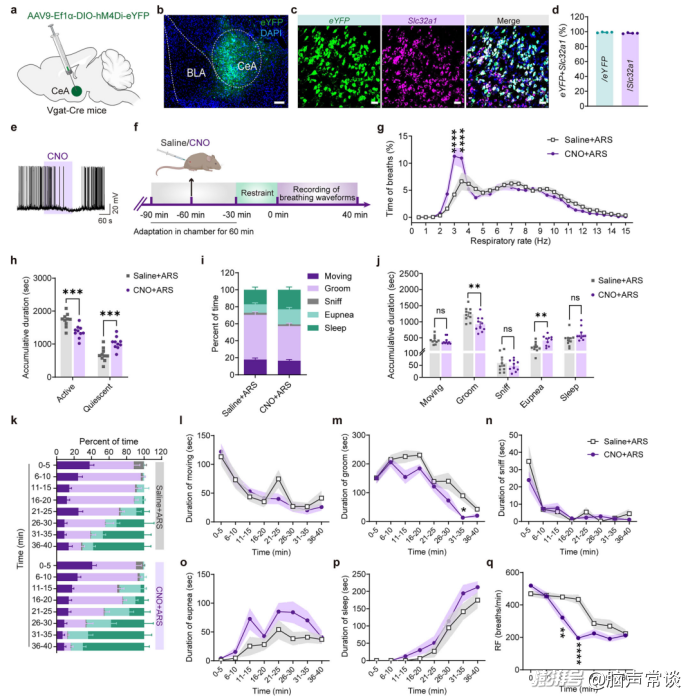
图二 沉默CeAGABA神经元可减少ARS诱导的呼吸和行为变化
研究旨在探讨中央杏仁核(CeA)中的GABA能神经元(CeAGABA)在调节ARS诱导的类焦虑行为中的作用。使用光纤记录检测了Vgat-Cre小鼠在ARS条件下CeAGABA神经元的钙离子(Ca2+)水平,反映了神经元的激活状态。结果显示,与新笼对照组相比,束缚条件下观察到明显增强的Ca2+信号,表明CeAGABA神经元的激活水平显著升高。采用化学遗传学来抑制这些神经元,结果表明,CeAGABA神经元的抑制显著增加了OFT中心区域的时间,减少了ARS组中的休息时间,并增加了EPM开放臂进入次数和停留时间。进一步分析显示,在ARS后,CeAGABA神经元的化学遗传学抑制导致呼吸频率降低,表现为低频呼吸模式(3–3.5 Hz)的增加,以及活跃时间减少、静息时间增加,特别是减少了压力相关的梳理毛发时间和增加了正常呼吸时间。利用光遗传学方法结合膈神经放电(PND)记录评估了CeAGABA神经元对中枢呼吸驱动的影响,但未观察到明显变化,这表明CeAGABA神经元的抑制对中枢呼吸驱动没有显著影响。综上所述,该研究表明,CeAGABA神经元的抑制能够显著缓解ARS诱导的类焦虑行为,同时减少压力相关的长时间梳理行为和高频呼吸事件。然而,这种抑制并不影响中枢呼吸驱动,提示CeAGABA神经元在调控情绪反应而非直接控制呼吸方面具有特定作用。
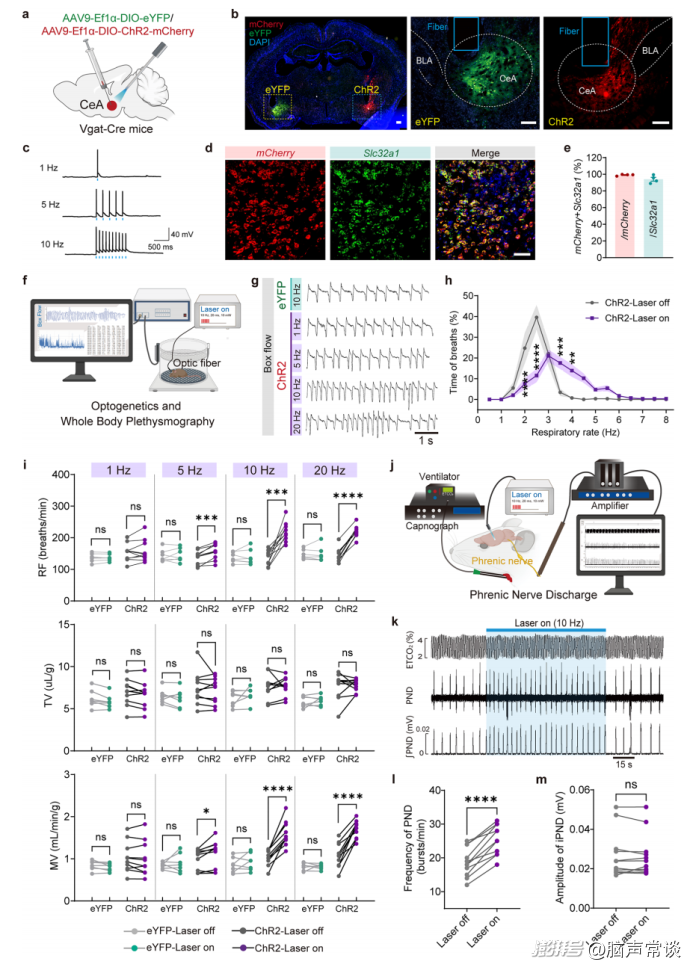
图三 光刺激CeAGABA神经元在安静和麻醉状态下激活呼吸
虽然证明了CeAGABA神经元的激活引发了更多的梳理行为以及随之而来的高频呼吸频率,但尚不清楚这种刺激是否在行为静止和麻醉状态下都会引发类似的呼吸表型。作者采用上述光遗传学方法,将AAV9-Ef1α-DIO-ChR2-mCherry(以AAV9-Ef1α-DIO-eYFP作为对照病毒)注射到Vgat-Cre小鼠的CeA区域。电生理实验进一步证实,在脑片中对表达ChR2的神经元进行光刺激能够诱发动作电位。RNAscope-FISH分析显示,ChR2-mCherry特异性表达于CeA中的GABA能神经元。随后,作者在动物行为静止的情况下使用全身体描术(WBP)记录,研究了CeAGABA神经元光刺激对通气的影响。1分钟内的呼吸频率分布曲线显示,光刺激主要增加了高频呼吸事件。此外,与仅表达eYFP的小鼠相比,≥5 Hz的光刺激显著增加了表达ChR2的小鼠的RF和每分钟通气量(MV),而潮气量(TV)无显著变化。为了进一步阐明CeAGABA神经元激活对中枢呼吸驱动的影响,在双侧迷走神经切断、机械通气、注射ChR2且麻醉的小鼠中研究了光刺激对PND的影响。观察结果显示,CeA区域的光照引起了PND频率快速、可逆且适度的增加,但未影响其振幅。总体而言,CeAGABA神经元的光刺激在行为静止和麻醉条件下均显著增强了静息通气。
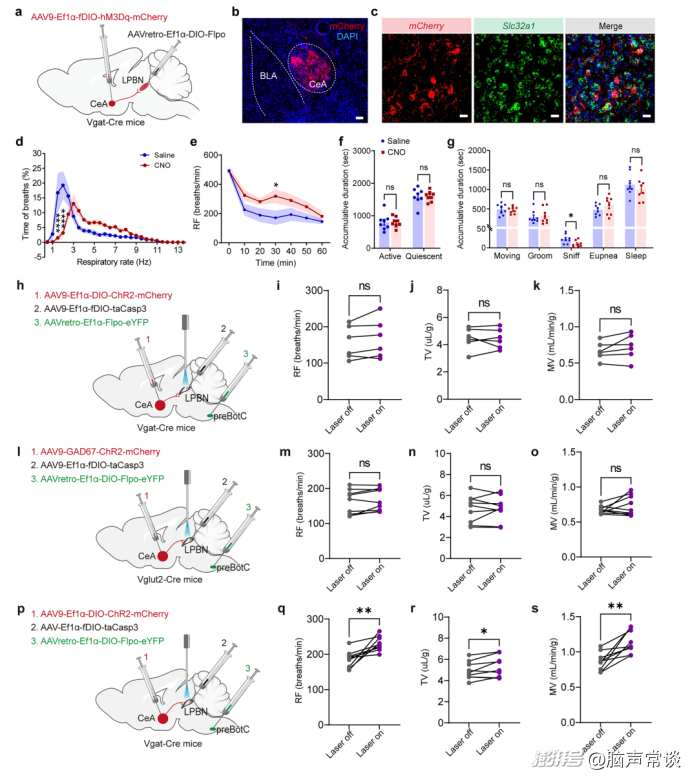
图四 CeA-LPBN环路主要在行为静止状态下调节呼吸模式
研究探讨了CeA到LPBN再到preBötC(前包钦格尔复合体)这一神经环路在调节呼吸模式中的作用,尤其是在行为静止状态下。使用化学遗传学方法特异性地操纵从CeAGABA神经元投射到LPBN的神经元表达hM3Dq,并通过注射CNO激活这些神经元。结果显示,与盐水注射相比,给予CNO后显著增加了高频呼吸事件的发生率,特别是在注射后30分钟观察到了明显升高。行为分析表明,无论是盐水还是CNO注射,对活跃期和静息期以及移动、梳理毛发、嗅探、正常呼吸和睡眠的持续时间的影响相似,这表明CeA-LPBN环路主要调节呼吸模式而不影响行为变化。进一步实验显示,刺激CeAGABA神经元轴突末端位于左侧或右侧LPBN均明显增加了自由活动小鼠的呼吸频率和每分钟通气量,但左右侧之间没有显著差异,说明没有明显的侧向效应影响呼吸功能。作者选择性地损毁了投射至preBötC的LPBN神经元。结果表明,光刺激CeA-LPBN环路未引起呼吸参数的显著变化。损毁LPBNGlu神经元后,由CeAGABA神经元光刺激引起的呼吸参数增加消失,而损毁LPBNGABA神经元则未能阻止这种增加。这表明CeAGABA神经元光刺激引发的呼吸变化最有可能是由投射至preBötC的LPBNGlu神经元的激活介导的。综上所述,CeA-LPBN环路主要在行为静止状态下调节呼吸模式,尤其是通过激活投射至preBötC的LPBNGlu神经元来实现这一点,而非直接影响焦虑样行为。
总结
作者的研究表明,ARS不仅会诱导小鼠的类焦虑行为,还会延长其活跃时间(主要由梳理毛发时间增加引起),同时减少静息时间。在这些行为变化的同时,经ARS处理的小鼠表现出高频呼吸事件的发生率显著增加。通过化学遗传学方法抑制CeAGABA神经元能够显著减轻ARS引起的行为和呼吸变化。相反,刺激CeAGABA神经元则会产生与ARS处理小鼠相似的行为和呼吸变化,表现为梳理毛发时间延长以及高频呼吸事件增加。在行为静止或麻醉状态下,刺激CeAGABA神经元也会增强中枢呼吸驱动和呼吸频率。此外,激活CeA-PVT环路会显著增加梳理毛发时间和高频呼吸事件,而刺激CeA-LPBN-preBötC环路则显著增强通气功能且不会引发类焦虑行为。综上所述,CeAGABA神经元作为一个中枢调控枢纽,通过不同的神经环路机制协调类焦虑行为和呼吸模式。
文章来源:https://doi.org/10.1038/s41467-025-58791-6
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




