- +1
我国学者开发基于自噬的细胞膜蛋白靶向降解新技术
撰文丨王聪
编辑丨王多鱼
排版丨水成文
靶向蛋白降解(TPD)利用细胞自身的降解机制(例如泛素-蛋白酶体系统、溶酶体途径)来选择性清除目标蛋白,已成为一种新兴治疗策略,TPD 为传统药物的不可成药靶点带来了巨大希望。例如,目前已有十多项基于蛋白靶向降解嵌合体(PROTAC)的药物进入人体临床试验,用于治疗癌症等疾病。
细胞表面的细胞膜蛋白,广泛参与细胞识别、物质运输、信号转导等生命活动,是重要的药物研发靶点。近年来,研究人员开发了一系列针对细胞膜蛋白的靶向降解技术,例如 LYTAC、AbTAC 等。这些技术通过构建双功能分子,实现靶蛋白与细胞膜表面溶酶体穿梭受体或 E3 连接酶之间的物理绑定,借助这些受体或酶的生物学活性,促进靶蛋白内吞至溶酶体并降解。
然而,由于双功能分子的合成较为复杂,且依赖于特定的溶酶体穿梭受体或 E3 泛素连接酶,其应用受到了限制。
2025年1月9日,中国科学院深圳先进技术研究院医药所纳米医疗技术研究中心李红昌研究员、房丽晶研究员、蔡林涛研究员及邵喜明副研究员等人,在 Nature 子刊 Nature Chemical Biology 上发表了题为:Chemically Engineered Antibodies for Autophagy-based Receptor Degradation 的研究论文。
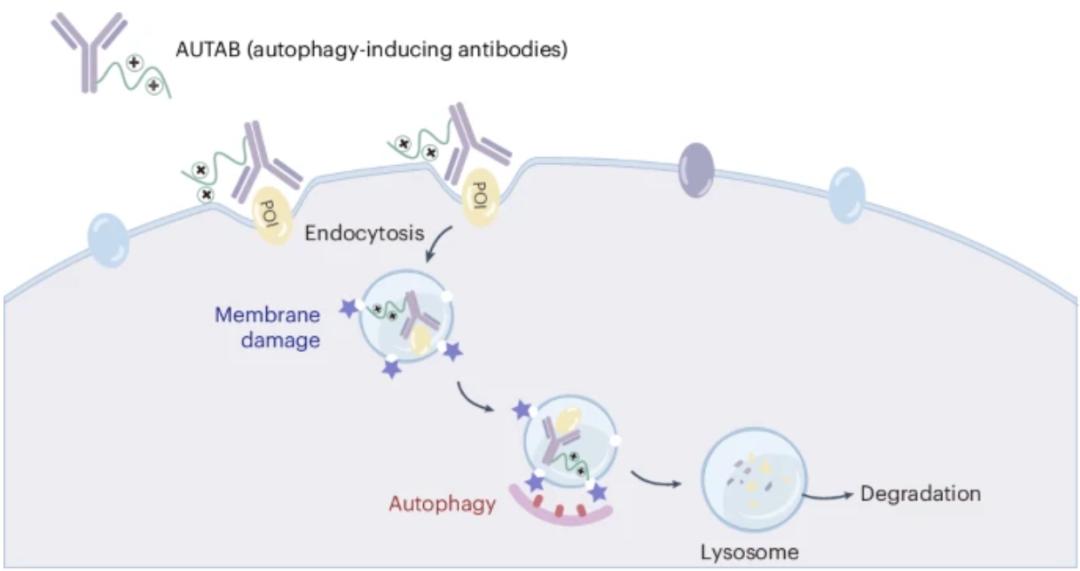
该研究开发了一种全新的基于自噬机制的细胞膜蛋白靶向降解技术——AUTAB(autophagy-inducing antibody)。该技术通过将细胞自噬诱导分子与细胞膜蛋白靶点抗体进行共价偶联,实现了在不依赖额外细胞表面蛋白的情况下,精确触发靶点蛋白通过自噬-溶酶体路径降解。该研究为以细胞膜蛋白为靶点的药物研发提供了一种新的广谱适用策略。

为了解决当前细胞膜蛋白靶向降解技术的局限性,研究团队开发了一种基于细胞自噬的质膜蛋白降解平台,研究团队将其称为 AUTAB(autophagy-inducing antibody,自噬诱导抗体)。该工程抗体通过与聚乙烯亚胺(PEI)共价结合,通过自噬降解靶受体。AUTAB 的蛋白降解活性是自给自足的,无需溶酶体穿梭受体或 E3 泛素连接酶的参与。
接下来,研究团队通过靶向各种临床上重要的受体,展示了该平台的广泛适用性,不仅能够在多种细胞类型中降解靶蛋白,而且能够实现对包括膜锚定蛋白 CD73 在内的各种膜蛋白的高效靶向降解。
为了进一步提高 AUTAB 技术的可及性和便利性,研究团队进一步开发了一种模块化的 纳米 AUTAB 系统,将特定的一抗与带有聚乙烯亚胺(PEI)标签的二抗纳米抗体相结合,获得了一种通用的 AUTAB 分子,只需在使用时搭配不同的细胞膜蛋白抗体,即可实现对各种细胞膜蛋白的靶向降解。
总的来说,该研究开发出了一种质膜蛋白靶向自噬降解的新策略,该策略具有易于生成、不受细胞类型限制以及适用范围广等优点。
中国科学院深圳先进院博士生程冰华、副研究员李梅青、研究助理郑纪维为该论文的共同第一作者;李红昌研究员、房丽晶研究员、蔡林涛研究员、邵喜明副研究员为论文共同通讯作者。
论文链接:
https://www.nature.com/articles/s41589-024-01803-1
原标题:《Nature子刊:我国学者开发基于自噬的细胞膜蛋白靶向降解新技术——AUTAB》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




