- +1
Immunity:万伟/刘伟/许银丰团队发现cGAS-STING通路新功能——溶酶体生物发生
原创 生物世界 生物世界
撰文丨王聪
编辑丨王多鱼
排版丨水成文
固有免疫是宿主抵御病原体的第一道防线。在哺乳动物细胞中,模式识别受体(PRR)检测微生物成分并触发固有免疫应答。作为细胞内的PRR, cGAS识别细胞质中的微生物或宿主来源的DNA并产生cGAMP, cGAMP与STING结合并导致STING从内质网输出。
诱导自噬是cGAS-STING通路的一个古老功能,通过该通路,自噬货物被运送到溶酶体降解。然而,溶酶体本身的功能是否也受到cGAS-STING通路的调节,目前尚不清楚。
2024年12月16日,浙江大学医学院附属邵逸夫医院万伟研究员、浙江大学国际健康研究院刘伟教授及湖南第一师范学院许银丰副教授等,在 Immunity 期刊发表了题为:The cGAS-STING pathway activates transcription factor TFEB to stimulate lysosome biogenesis and pathogen clearance 的研究论文。
该研究表明,cGAS-STING通路激活转录因子TFEB,刺激溶酶体生物发生和病原体清除,从而揭示了cGAS-STING通路的一个新的重要功能——诱导溶酶体生物发生。

在这项最新研究中,研究团队发现,cGAS-STING通路通过独立于其下游蛋白激酶TANK结合激酶1(TBK1)的溶酶体生物发生过程,来上调溶酶体活性。
STING的激活通过诱导转录因子EB(TFEB)及其同源转录因子TFE3和MITF的核转位,来增强溶酶体的生物发生。STING的诱导GABA A型受体相关蛋白(GABARAP)脂质化,这是一种自噬相关蛋白,位于STING囊泡上,负责TFEB的激活。
膜结合的GABARAP隔离了GTP酶激活蛋白卵巢滤泡激素(FLCN)和FLCN相互作用蛋白(FNIP)复合体,以阻止其对RagC和RagD的功能,解除了mTORC1依赖的磷酸化和TFEB失活。
在功能上,STING诱导的细胞内溶酶体生物发生促进了胞质DNA和入侵病原体的清除。因此,这些发现揭示了诱导溶酶体生物发生是cGAS-STING通路的另一个重要功能。
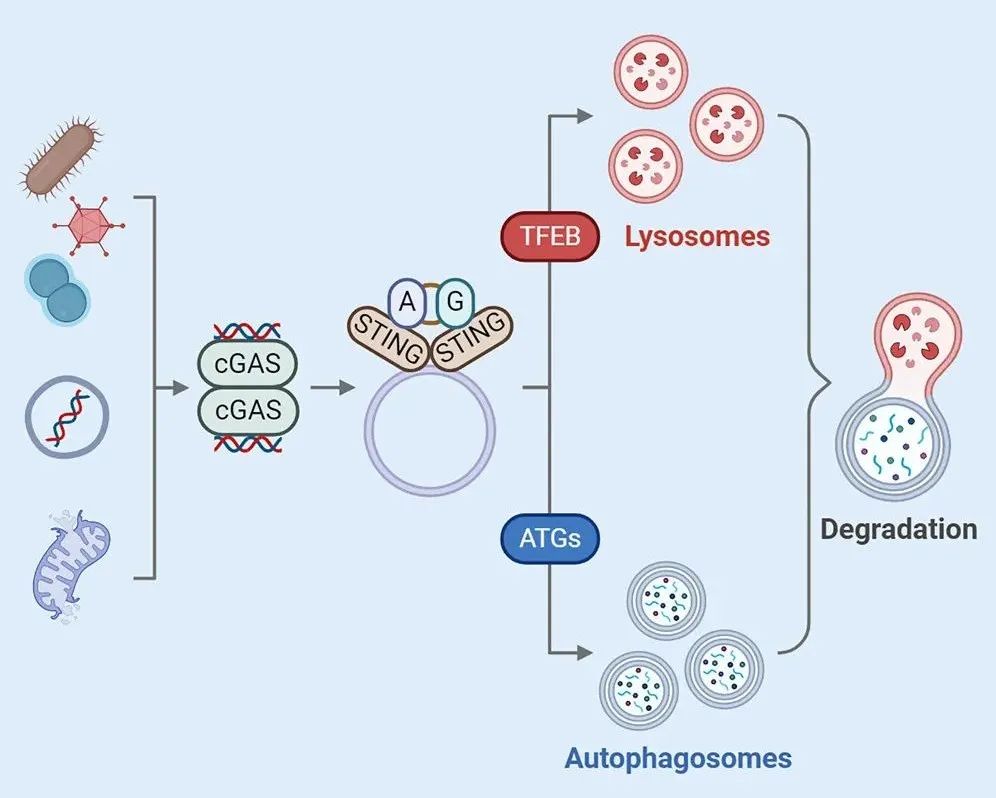
该研究的核心发现:
cGAS-STING通路可增强溶酶体活性;
STING的激活足以激活TFEB,从而刺激溶酶体的生物发生;
STING诱导的GABARAP脂质化介导TFEB激活;
STING诱导的溶酶体生物发生有助于病原体的清除;
论文链接:
https://www.cell.com/immunity/abstract/S1074-7613(24)00532-6

设置星标,不错过精彩推文
开放转载
欢迎转发到朋友圈和微信群
微信加群
为促进前沿研究的传播和交流,我们组建了多个专业交流群,长按下方二维码,即可添加小编微信进群,由于申请人数较多,添加微信时请备注:学校/专业/姓名,如果是PI/教授,还请注明。
点在看,传递你的品味素材来源官方媒体/网络新闻继续滑动看下一个轻触阅读原文

生物世界向上滑动看下一个
原标题:《Immunity:万伟/刘伟/许银丰团队发现cGAS-STING通路新功能——溶酶体生物发生》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




