- +1
【科学普及】心脏澎湃动力之源——心磷脂
作者:张悦健 闫岩 冯静雯 刘佳 滕洁英
指导老师:胡劲松
作者单位:西安交通大学医学部基础医学院细胞生物学与遗传学系
作为第一个发挥功能的器官,心脏的发育生物学令人着迷[1]。
人类胚胎发育第10天左右,胚胎开始出现外胚层、中胚层、内胚层的分化。到第16天左右,中胚层的头侧部分增厚,形成一条中央管并发育成心脏和大血管。第20天左右,心脏开始泵血工作。
胎儿时期处于低氧环境,此时心脏发育尚不完全,会选择糖酵解与乳酸氧化作为能量来源。出生标志着心脏代谢方式的重大转变,随着心脏内脂质成分的改变,线粒体数量增加,心脏氧化磷酸化能力大幅增强,此时对能量底物利用倾向为脂肪酸[2]。心脏的早期发育不全通常与代谢异常有着密切的联系,因此,了解心脏内与代谢相关脂质的合成对于疾病的早期监控与预防有着重要意义。
心肌作为人体内最“强壮”的永久细胞,无时无刻不在工作。为了适应长期高强度的活动,心肌细胞内有大量的“能量工厂”——线粒体为其供能。而存在于线粒体内膜上ATP合酶(又称为F0F1-ATP酶),则是线粒体内最重要的负责生成ATP的分子机器。此外,一种富含于心脏细胞线粒体内膜中的心磷脂(cardiolipin)对能量产生有着极其重要的作用。在几种遗传性心脏疾病如Barth综合征、Sengers综合征、扩张型共济失调性心肌病(dilated cardiomyopathy with ataxia syndrome,DCMA)背后,都存在心磷脂的生物合成的异常;而其他心血管疾病,如缺血/再灌注损伤和心力衰竭,也与心磷脂的变化密切相关。
01 心磷脂的诞生之旅

心磷脂,亦称双磷脂酰甘油,具有二聚体结构和四个对称的脂肪酰基侧链,主要存在于动物细胞中线粒体的内膜,其中15%的心磷脂存在于心肌。20世纪40年代,科学家从新鲜的牛心肌中分离出心磷脂,故得此名。
心磷脂的合成殊不简单,是细胞内错综复杂的生化反应的典型代表[3]。它从一个简单的分子开始,经过多种酶的协作,一步步被“修饰”成最终的功能性分子,这过程就如同雕刻家将一块石头慢慢雕琢为完美的艺术品。
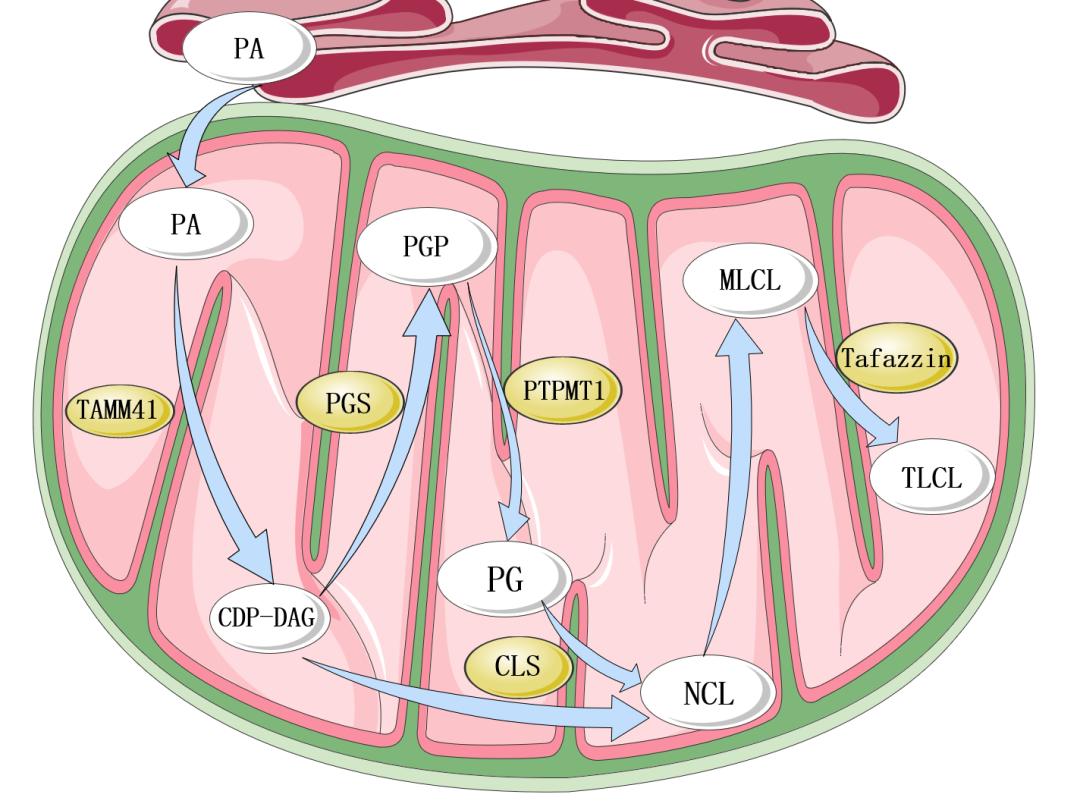
(一)磷脂酸的转运——启动旅程

一切都从一个叫磷脂酸(phosphatidic acid,PA)的分子开始。
PA首先在内质网中合成,在线粒体相关内质网膜中,PA借助液泡蛋白分选13蛋白家族(vesicle protein sorting 13,VPS13)与微管动力学调节器蛋白家族(microtubule dynamics regulator protein, MDRP)的帮助被转运至线粒体外膜。
想要进一步到达线粒体内膜,PA还需要穿过线粒体外膜的疏水屏障,此时就需要线粒体内膜和外膜之间的“桥梁”—线粒体接触位点和嵴组织系统(mitochondrial contact site and cristae organizing system,MICOS)来协助转运。MICOS由蛋白质复合物组成,在线粒体内、外膜之间形成连接,对于脂质和蛋白质的运输至关重要。在MICOS附近,一种名为Prelid 1的蛋白可以介导PA的运输。有趣的是,MICOS的组装还需依赖PA的终产物心磷脂。在这一步,PA就像是被运送到工厂中的原材料,等待进一步加工。
(二)TAMM41——起始的催化

一旦PA进入线粒体内膜,一种关键的酶——TAMM41就会对其进行加工。TAMM41负责将磷脂酸(PA)转化为CDP-二酰甘油(cytidine diphosphate-diacylglycerol,CDP-DAG)。CDP-DAG可以被看作是构建心磷脂的基础材料。它的形成标志着心磷脂合成的重要起点,就像是建筑工人已经将地基打好。
(三)PGS和PTPMT1——构建骨架

CDP-DAG还需要进一步的加工。磷脂甘油磷酸合成酶(phosphatidylglycerol synthase,PGS)会将CDP-DAG转化为磷脂甘油磷酸(phosphatidylglycerophosphate,PGP)。PGP像是心磷脂的雏形,具备了基本的骨架,但还需要更多的修饰。接着,另一种酶PTPMT1接过接力棒,将PGP去磷酸化,生成磷脂甘油(phosphatidylglycerol,PG)。这个过程类似于将大体轮廓塑造完成,但还未达到最终的形态。
(四)心磷脂合成酶——拼图大师的收尾工作

到这个阶段,构建心磷脂的关键材料已经准备就绪。现在,轮到心磷脂合成酶(cardiolipin synthase, CLS)进行“拼图”了。CLS将PG与CDP-DAG结合,生成了初生的心磷脂(nascent cardiolipin,NCL)。这一步至关重要,心磷脂合成酶就像是这场合成旅程的总指挥,负责将之前准备的各种原料最终组合成心磷脂的雏形。这一步生成的新生心磷脂具备了一定的功能,但还远未达到成熟的状态。
(五)去酰基酶与Tafazzin——雕刻家的精细修饰

新生心磷脂其实还只是一个“半成品”,还需要经过进一步的修饰才能达到功能上的最佳状态。新生心磷脂首先由去酰基酶脱乙酰化形成单溶血心磷脂 (monolysocardiolipin,MLCL)。接下来,转酰基酶Tafazzin将完成最终的修饰。它的工作就像是雕刻家精细打磨雕像的过程,通过一系列的转酰基反应,把MLCL转化为最终成熟的心磷脂,即四亚油酰心磷脂(tetralinoleoyl cardiolipin,TLCL)。
最终的修饰决定了心磷脂的功能特性。在心磷脂的修饰过程中,Tafazzin等酶负责将脂肪酸链转移到心磷脂分子上,使它变得更稳定、功能更强。这一步骤是心磷脂合成的“点睛之笔”,使其能够在细胞中真正发挥重要的生理作用。
02 可怕的心肌病——Barth综合征

有一种罕见的 X 连锁遗传性疾病叫作Barth综合征(barth syndrome,BTHS),它由编码转酰基酶 Tafazzin的基因突变引起。在男性患者中表现为心肌病、中性粒细胞减少症、骨骼肌病、青春期前生长迟缓和独特的面部形态(婴儿期最为明显)。尽管Barth综合征是一种多系统疾病,但心肌病对于该综合征的进展具有重要意义。心肌病总是在五岁前出现,通常是扩张型心肌病,伴或不伴有心内膜弹力纤维增生症或左心室致密化不全,也可能出现肥厚型心肌病。心力衰竭是Barth综合征死亡的重要原因[4]。
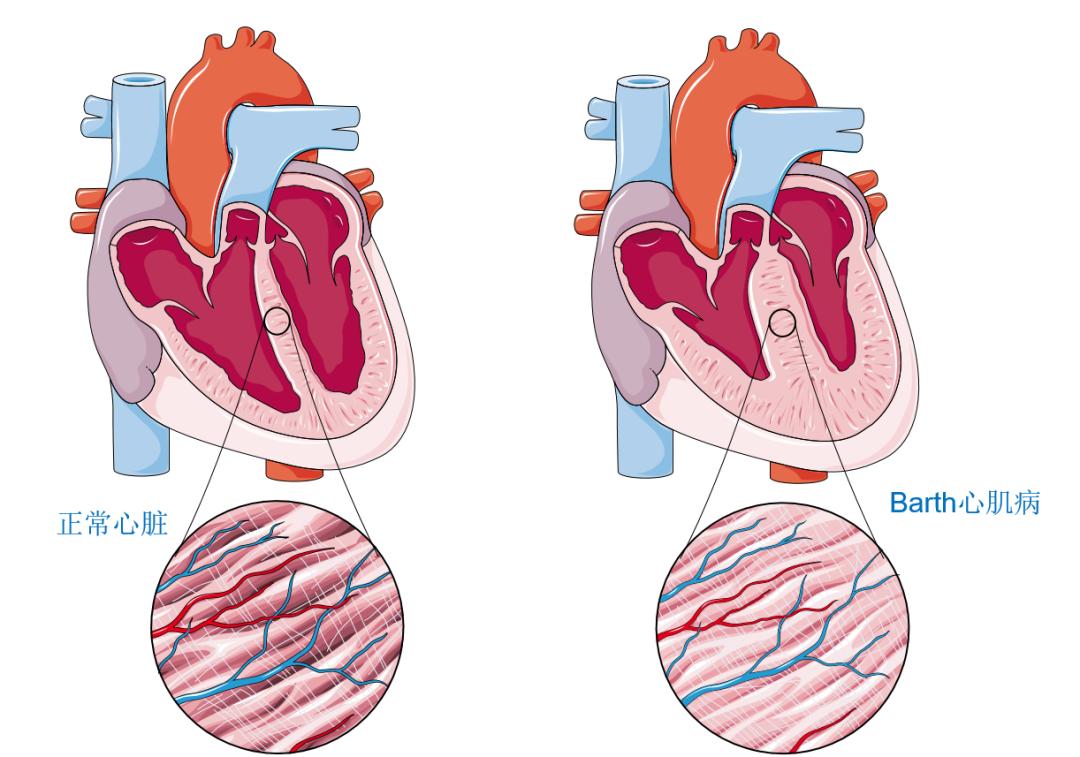
Barth综合征的发生与编码Tafazzin的基因突变有关。Tafazzin的功能缺失,会导致成熟心磷脂量减少、心磷脂酰基链异质性增加和单溶血心磷脂水平增加。以上变化会使线粒体嵴形态显著改变,导致氧化磷酸化功能受损[5],最终导致这种可怕的疾病。
近年,随着对疾病早期监控的重视,Barth综合征患者的预期寿命不断得到延长。医生常采用多学科管理方法来解决Barth综合征造成的多器官损伤问题。虽然目前尚无针对Barth综合征原发性分子机制的药品应用于临床,但有两种正处于实验阶段且颇有前景的药品:[6]
(1)苯扎贝特(Bezafibrate)
苯扎贝特是一种 PPAR 激动剂,最初用作降脂剂,现已证明可通过激活过氧化物酶体增殖激活受体-γ(PPAR-γ)的辅激活因子 1-α(PGC-1α)信号来促进那些参与氧化代谢的基因转录。在敲低Tafazzin的 Barth 综合征模型小鼠中,苯扎贝特被证明可在异丙肾上腺素应激环境下改善左心室收缩功能障碍。
(2)Elamipretide
Elamipretide 是一种具有交替芳香族阳离子结构的细胞渗透肽,它定位于线粒体内膜并与心磷脂结合。Elamipretide 被推测可以维持嵴结构并改善生物能量功能障碍。研究表明,Elamipretide可用于治疗线粒体疾病和心力衰竭。
总而言之,心磷脂是一位神秘而无私的守护者,是每一次心跳的幕后推手,使得那些持久澎湃的强健心脏能够为人们热烈的人生提供功力。
参考文献

[1] Asp, M., Giacomello, S., Larsson, L., Wu, C., Fürth, D., Qian, X., ... & Lundeberg, J. (2019). A spatiotemporal organ-wide gene expression and cell atlas of the developing human heart. Cell, 179(7), 1647-1660.
[2] Miao, H., Li, B., Wang, Z., Mu, J., Tian, Y., Jiang, B., ... & Lam, S. M. (2022). Lipidome atlas of the developing heart uncovers dynamic membrane lipid attributes underlying cardiac structural and metabolic maturation. Research, 2022, 0006.
[3] Decker, S. T., & Funai, K. (2024). Mitochondrial membrane lipids in the regulation of bioenergetic flux. Cell Metabolism.
[4] Ferreira C, Pierre G, Thompson R, Vernon H. (2020). "Barth Syndrome." GeneReviews® [Internet].
[5] Ikon N, Ryan RO. (2017). "Cardiolipin and mitochondrial cristae organization." Biochim Biophys Acta Biomembr, 1859(6), 1156-1163.
[6] Thompson R, Jefferies J, Wang S, Pu WT, Takemoto C, Hornby B, Heyman A, Chin MT, Vernon HJ. (2022). "Current and future treatment approaches for Barth syndrome." J Inherit Metab Dis, 45(1), 17-28.
原标题:《【科学普及】心脏澎湃动力之源——心磷脂》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




