- +1
【科普课堂】有趣的糖科学史:唾液酸的发现史(之一)
以下文章来源于谢然课题组 ,作者XR
谢然课题组.
课题组文献阅读共享及科普平台
有趣的糖科学史
唾液酸的发现史(之一)
“
燕巢虽小,心怀天下;
人居其室,内有乾坤。
”
“层出不穷”唾液酸
在1973年第二届国际糖复合物研讨会上,阿尔弗雷德·戈特沙尔克(Alfred Gottschalk)应邀讨论了糖蛋白研究的现状,他说:“我们尚未走到尽头,一切仅仅刚刚开始,我们只是到达了一片未知大陆的海岸有待登陆。”这些话可能恰巧最适用于他毕生喜爱的课题:关于唾液酸(sialic acid)的相关研究。戈特沙尔克鼓励对科学研究感兴趣的学生从事糖生物学领域的工作,而这一领域在 20世纪70年代得以迅速发展。自彼时以降,许多关于唾液酸的化学、分析、生物化学和生物学的问题都得到了解答,这一糖分子家族对我们生活的重要影响,也已广泛出现在大量的学术出版物中。
唾液酸在自然界中以多种分子形式存在,自20世纪60年代以来已有各种详细的描述。这些化合物通常存在于高等动物中,如棘皮动物门、半索动物门、头索动物门和脊椎动物门,偶尔也可以在其他动物类群的一些成员中发现,如头足纲、扁形动物门中的涡虫和甲壳纲中的螯龙虾。唾液酸还存在于某些病毒、各种细菌、原生动物和致病真菌中。它们不存在于植物和进化树中低于棘皮动物门的大多数动物中。各种研究表明,唾液酸在进化过程中出现得相对较晚,这导致人们假设获得这些单糖会加速高等动物的分化。在天然存在的含唾液酸结构中,唾液酸单元通过碳水化合物-蛋白质相互作用在许多生理和病理过程中发挥重要作用,包括细胞识别和通讯、细胞聚集和发育、控制生物体中糖复合物的寿命、介导细菌和病毒感染、参与肿瘤生长和转移、在免疫学、微生物组生物学、细胞信号传递、生殖生物学和神经生物学中发挥了重要作用。唾液酸主要存在于许多糖复合物(糖蛋白;糖脂)和碳水化合物链(寡糖、荚膜和组织多聚唾液酸、细菌脂寡糖/多糖)的末端,并且以各种化学形式存在(图1)。它实际上是更为古老的α-酮酸(α-keto acid)单糖家族的一个子集,该家族具有九碳骨架,被称为壬酮糖酸(nonulosonic acid, NulO),在一些真细菌和古菌中也有发现(图2)。本期及余下的几期中,我们将抽丝剥茧,回顾这些糖生物学中令人着迷的分子,以及它的发现史。
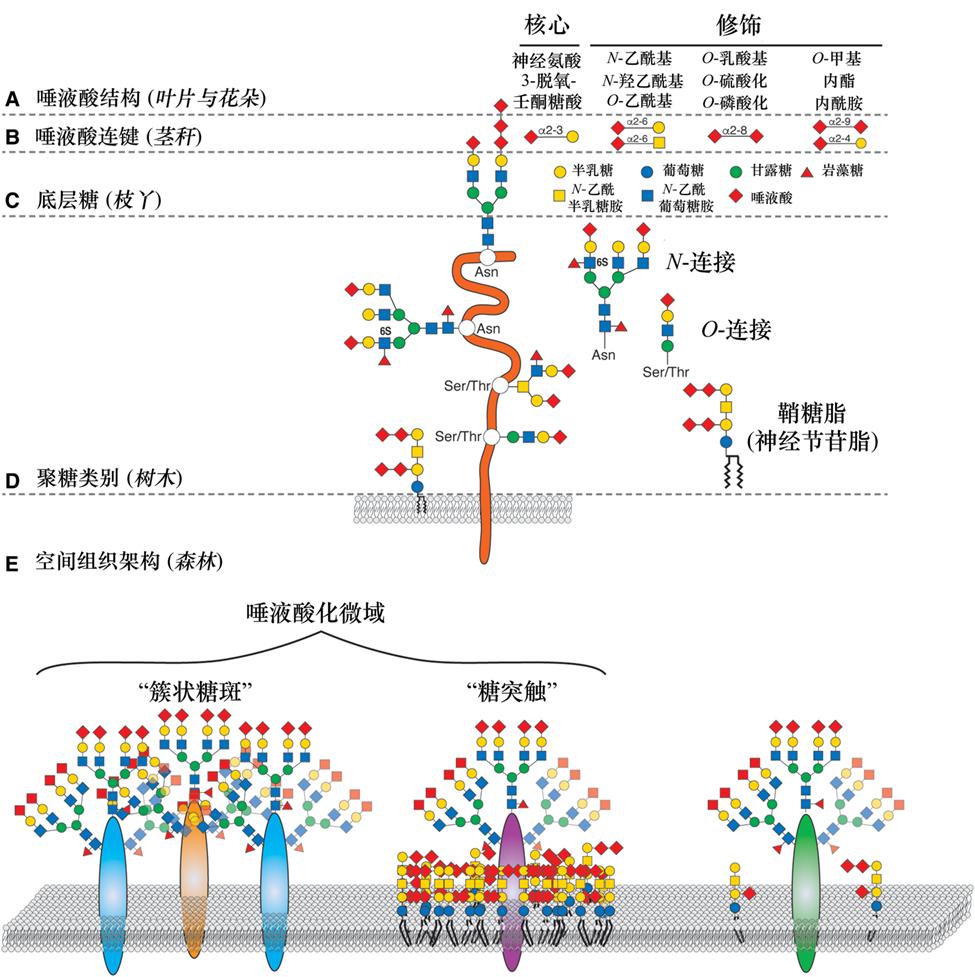
图1 唾液酸的复杂性具有不同的层级结构。唾液酸组的复杂程度至少存在着以下几个层级 (A)唾液酸核心及核心修饰:与各种基团的酯化,O-甲基化,内酯化或内酰胺化,产生逾80种不同的结构; (B)与表层下的糖之间的、不同的连键类型。包括四种主要连键类型和许多次要连键类型; (C)表层下糖链的特性和排列,还可以通过岩藻糖基化或硫酸化获得进一步的修饰;(D)聚糖类别的不同(N-连接或O-连接的糖蛋白,鞘糖脂);(E) 唾液酸在唾液酸化微域中的空间组织,即被称为 "簇状糖斑 "或 "糖突触 "的唾液酸化微域。
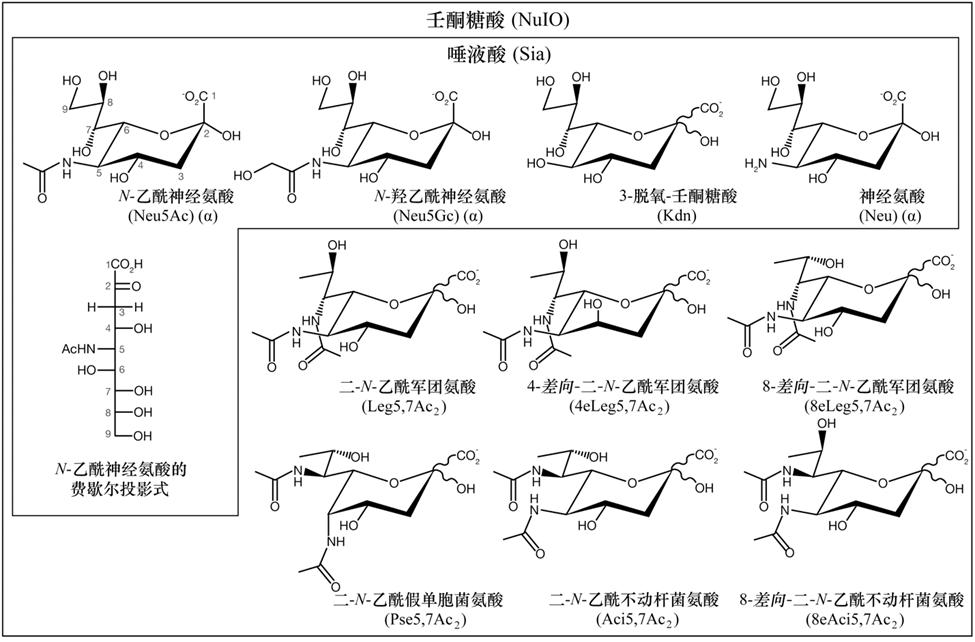
图2 唾液酸和其他壬酮糖酸。如图所见,唾液酸是壬酮糖酸的一个子集。
埃尔利希,比亚尔与一盆滋味
距今140多年前的1877年,德国科学家菲利克斯·霍普-塞勒(Felix Hoppe-Seyler)描述了一种物质,它是经过高温弱酸处理后从上皮粘蛋白中释放出来的一种酸性化合物,酸性强于碳酸。在碱性条件下加热时溶液可变成棕色。该化合物含有氮元素,可还原氧化铜、氧化铋或硫酸靛蓝,但无法被啤酒酵母发酵。如何纯化这一物质是长期困扰科学家的问题之一。除了霍普-塞勒外,格林(J.R.Green)、克鲁根博格(C. Fr. W. Krukenberg)和泽勒(H.Zeller)在研究亚洲金丝燕时观察到了类似的弱酸性物质,这些鸟类使用它们的唾液腺分泌黏蛋白来筑巢。燕窝可以食用,并有一定的营养和药用价值。
“有趣的是,格林声称从释放的物质中观察到了糖的结晶,而泽勒却无法佐证这一说法:“显然,格林认为所观测到的无机物质其实就是糖”。
风趣的是,多年之后,从燕窝中的黏蛋白反而成为了分离克级唾液酸的绝佳来源,因为研究者只需将磨碎的燕窝在回流状态下下煮沸5个小时即可获得大量的唾液酸。
时间来到1898年,德国的保罗·埃利希(Paul Ehrlich)发现将这些黏蛋白和对二甲氨基苯甲醛(p-dimethylaminobenzaldehyde)在酸性溶液中共同加热可形成紫色物质。同年,德国的穆勒(F.Muller)描述将这些粘液物质在碱性条件下稍微加热后,随后在较高温度下与酸性的对二甲氨基苯甲醛一起孵育,会形成鲜艳的红色。现在对二甲氨基苯甲醛和50%的盐酸混合物被称为埃利希试剂(Ehrlich’s reagent), 经常用于检测吲哚、吡咯和致幻剂LSD,但该反应在揭示唾液酸结构方面发挥了重要作用。1927年,德国的沃尔兹(E. Walz)和美国的莱文(P. Levene)与兰德施泰纳 (K. Landsteiner)报道,将源自牛脾/马肾/牛肾/牛脑中的脂类物质与苔黑素(orcinol)在含有氯化铁或醋酸铜的盐酸溶液中加色后会形成红紫色,该试剂后来被称为比亚尔试剂(Bial’s reagent),已经成为了碳水化合物存在的通用测试方法。戊糖会呈现出蓝绿色,而己糖则呈现黄褐色。因此,实验中所观察到的红紫色其实非常耐人寻味。

图3 菲利克斯·霍普-塞勒,爪哇金丝燕以及西方关于燕窝的第一例系统性研究。保罗·埃利希因对免疫学的贡献获得了1908年诺贝尔生理学与医学奖,殊不知他还是一个功夫了得的化学家,埃利希试剂至今仍被用于致幻剂麦角酸二乙基酰胺(LSD)的快速化学检测。比亚尔试剂的检测效果因碳水化合物的类型不同而各异。
千人千面,同归殊途
究竟是哪个研究小组率先发现和分离了唾液酸?这个问题的答案众说纷纭且分布在世界各地:瑞典乌普萨拉大学的贡纳·布利克斯(Gunnar Blix)?德国图宾根大学和科隆大学的厄内斯特·克伦克(Ernst Klenk)?还是澳大利亚墨尔本沃尔特和伊丽莎霍尔研究所和德国图宾根马克斯普朗克病毒研究所的阿尔弗雷德·戈特沙尔克?有趣的是,以完全不同生物来源的材料作为检测源,在他们的探索之旅中发挥了重要的作用。
1936年,布利克斯及同事以沸水作为溶液,从牛颌下腺黏蛋白中抽提分离出了一种强酸性化合物,他称之为“1号碳水化合物”(Kohlenhydrat I)。该化合物通过自发的水解过程得以生成,并且能够以晶体形式获得,具有还原性。元素分析得出的化学式为C14H24NO11。微量化的乙酰测定表明,该化合物的单个分子中存在着两个乙酰基,而作为阴性测试的茚三酮反应则推测出存在一个N-乙酰基结构。产物的熔点为140-150°C (分解温度)。紫外光谱检测表明化合物不存在不饱和的乙烯键。该化合物对稀无机酸加热非常敏感,导致形成深色的腐殖质(humin)。与埃利希试剂一起加热时,无论是否经过碱的预处理,都会形成深红紫色的焰色反应。综合考虑以上观察结果,布利克斯认为:该化合物应该具有软骨胺(chondrosamine)部分和具有六个碳原子的多羟基酸部分共同组成的二糖结构,而不是以己糖醛酸的形式存在(需要注意的是,布来克斯并未从该物质中成功分离出己糖胺结构)。最初有人提出。己糖胺部分应该是半乳糖胺结构,但随后因为软骨胺的成功分离而被证伪。有人指出,这两种化合物“可能以极其易断裂的化学键两相结合”。另一个早期观点是期中的多羟基酸可能是脱氧己糖醛酸。由于“1号碳水化合物”来源于唾液(希腊语σíαλoν),布利克斯将该化合物称为“唾液酸”。
在后续的工作中,布利克斯发现牛脑组织中所谓的“初磷脂“(protagon)组分也能产生埃利希试剂和比亚尔颜色反应。而几年前,厄内斯特·克伦克已经提出了用比亚尔试剂将人脑的脂质”变成”红色物质。该团队在1941年成功分离出一种结晶形式的含氮有机酸,并因来源于神经元相关,将其称为“神经氨酸”(neuraminic acid)。由于在酸性介质中进行实验,通常会因化合物的不稳定性导致形成黑色的腐殖质,他们选择了甲醇-盐酸处理脂质材料,随后通过其钡盐将释放的物质转化为游离酸。元素分析获得的化学式为:首选化学式为C11H21NO9。茚三酮反应呈阳性,表明化合物中存在着游离氨基,但并未表现出还原性。比亚尔和埃利希反应则均呈现强阳性。检测“神经氨酰酸”中己糖胺部分的方案最终未能成功,因此他们认为该化合物具有脂肪族聚氧氨基二羧酸结构。当克伦克意识到分离获得的物质经过甲醇-盐酸处理过程时会引入甲氧基时(后于20世纪50年代使用14C标记的甲醇予以证明),他将“神经氨酰酸”重新命名为“甲氧基神经氨酸”,并保留了化学式为 C10H19NO9(即C11H21NO9 去掉亚甲基)作为代表“神经氨酸”的名称。据此,“神经氨酸”可能含有活性羰基,从而能够与其他单糖形成糖苷键。在随后的一项研究中,他们将含有“神经氨酸”的脑糖脂称之为“神经节苷脂”(ganglioside),该名称也延续至今。
除了黏蛋白和脑糖脂研究领域对这些全新但未知的化合物展现出科学兴趣外,一个有趣的新角度来自于病毒学领域。20世纪40年代末,博耐特(F.M. Burnet)团队报道,各种黏蛋白(即血清黏蛋白、卵巢囊肿黏块、绒毛膜促性腺激素)在用活性病毒预处理后,失去了作为加热失活的流感病毒B血液凝集的竞争性抑制剂的能力。随后阿尔弗雷德·戈特沙尔克发现,将甲型流感病毒的墨尔本株与卵黏蛋白(ovomucin)(一种含有强效病毒血凝素抑制剂的蛋白质组分)一起孵育,产生了一种具有还原形的、水溶性的含氮化合物,经过埃利希试剂碱处理后呈现紫色;此外,采用莫利希碳水化合物试验(Molisch carbohydrate test),即浓硫酸和α-萘酚的混合试剂检测,可呈现强阳性。酸处理最终导致黑色的不溶性腐殖质形成。将卵黏蛋白与霍乱弧菌的滤液一起孵育,可产生具有类似性质的物质。长久以来,致病菌滤液中的酶样组分,被称为“受体破坏酶”(receptor-destroying enzyme,RDE)。根据迄今为止的结果,有研究者提出酶促过程释放了一种“碳水化合物-肽复合物”,并指出碳水化合物的部分应该是“一种寡糖,含有一个或多个 N-乙酰基(乙酰基)己糖胺残基,并且通过碱不稳定的糖苷键与非氨基糖相连”。两年后,戈特沙尔克重复了人类尿液黏蛋白与乙型流感病毒的孵育实验,提出释放出的化合物应为“N-取代的异葡萄糖胺”,即果糖胺;N-1-脱氧-1-酮糖氨基酸或肽。有趣的是,通过谢里瓦诺夫试验(Seliwanoff reagent),即间苯二酚/浓盐酸试验表明,该物质中确实存在酮。
1975年,布利克斯在写给克劳斯·斯托里克(Klaus Storiko)的一封信中,描述了他与戈特沙尔克的第一次接触:
“...我记得1949年在剑桥举行的第一届国际生物化学家大会上,我与斯泰西和戈特沙尔克交谈,当时后者描述了抑制病毒血凝的黏蛋白中碳水化合物成分的一般特性,并向斯泰西征求意见。我立刻意识到,戈特沙尔克提到的一些特性,使我强烈地回忆起了唾液酸。回到家后,我把我们写的关于唾液酸的文章寄给了戈特沙尔克,并告诉他我们打算对这个问题进行更为深入的验证。戈特沙尔克当时显然还不了解唾液酸,除了科隆和乌普萨拉之外,人们对这东西的兴趣仍然不大。而我对博耐特的研究也是知之甚少。我们后来同意在各自的实验室中明确地研究的塔姆-霍斯福尔糖蛋白(Tamm-Horsfall glycoprotein)中的碳水化合物成分,并于1952年同时在《自然》杂志上发表了我们的研究结果...”

图4 三个和尚有口水吃…贡纳·布利克斯,厄内斯特·克伦克和阿尔弗雷德·戈特沙尔克
未完待续
本文转载自公众号:“谢然课题组”
中国生物物理学会官方订阅号,为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科普课堂】有趣的糖科学史:唾液酸的发现史(之一)》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




