- +1
Sci Adv丨帕金森病治疗新曙光:M4受体的潜力与前景
帕金森病(PD)是一种神经退行性运动障碍,其特征是黑质致密部(substantia nigra pars compacta, SNc)的多巴胺(dopamine, DA)神经元逐渐丧失,导致背侧纹状体(dorsal striatum, DSt)中的多巴胺水平下降。这种多巴胺的缺失通过改变纹状体回路引起运动障碍,最终导致直接和间接通路的输出失衡,这些通路分别由表达D1受体(dMSNs)或D2受体(iMSNs)的中型棘状神经元组成。多巴胺的耗竭还被认为会增加主要来自局部胆碱能中间神经元(cholinergic interneurons, ChIs)的纹状体乙酰胆碱(acetylcholine, ACh)。根据DA-ACh平衡假说,多巴胺的丧失和乙酰胆碱的增加是导致帕金森运动功能障碍的主要病理因素。然而,尽管乙酰胆碱在纹状体中很重要,但多巴胺耗竭如何具体改变胆碱能传递和受体激活仍不清楚,因为在不同的PD模型中,关于ChI兴奋性和ACh水平变化的结果存在矛盾。
除了纹状体烟碱受体的回路效应外,乙酰胆碱还通过突触后G蛋白偶联的毒蕈碱受体直接调节MSNs。所有MSNs都表达Gq偶联的M1受体,但Gi/o偶联的M4受体主要表达在dMSNs中。M4受体被认为是参与DA-ACh相互作用的主要毒蕈碱亚型,通过解码ChI的放电模式和调节DA传递及相关的运动行为来发挥作用。M4受体通过调节多巴胺的突触前释放和突触后反对Golf/s偶联的D1受体信号传导,参与运动功能的控制,并调节皮质纹状体突触可塑性的诱导。因此,根据PD背景下的DA-ACh平衡假说,多巴胺丧失后乙酰胆碱水平的增加可能会转化为增强的M4信号和减少的dMSNs中的D1信号,导致直接通路的整体抑制和运动的抑制。为了抵消多巴胺的耗竭,标准的PD治疗使用前体左旋多巴(3,4-dihydroxy-L-phenylalanine, L-DOPA),但随着疾病进展,最终会导致称为左旋多巴诱导的运动障碍(levodopa-induced dyskinesia, LID)的异常不自主运动。然而,迄今为止,尚未直接确定PD中多巴胺丧失后或LID中L-DOPA治疗后M4信号如何改变。
科罗拉多大学的Beatriz E. Nielsen和Christopher P. Ford*在研究多巴胺耗竭的小鼠时发现,直接通路中M4介导的胆碱能信号传导并没有增加,反而由于dMSNs中突触后M4受体功能的减弱而减少。这种细胞亚型和突触特异性的适应对神经回路有广泛影响,并且动态依赖于多巴胺水平。恢复异常的M4信号意外地缓解了帕金森运动缺陷和L-DOPA诱导的运动障碍行为。他们的研究结果揭示,减少的直接通路M4传递可能在帕金森病的病理生理和L-DOPA诱导的运动障碍进展中起到潜在且以前未被注意到的作用。该研究成果以Reduced striatal M4-cholinergic signaling following dopamine loss contributes to parkinsonian and L-DOPA–induced dyskinetic behaviors为题发表在Science Advances上。

图源 Science Advances
首先,研究人员为了探究多巴胺(DA)耗竭对直接通路中M4介导的胆碱能信号传导的影响,向小鼠的内侧前脑束(medial forebrain bundle, MFB)单侧注射高剂量(4μg)的6-羟基多巴胺(6-OHDA),以诱导纹状体DA输入的几乎完全退化,而对照组动物则注射生理盐水。在6-OHDA注射后3-4周,背侧纹状体(DSt)和黑质致密部(SNc)中的酪氨酸羟化酶(tyrosine hydroxylase, TH)免疫反应性减少。正如预期的那样,DA系统的损伤导致了运动障碍,研究人员通过圆柱测试和旋转杆测试进一步评估。尽管DA的丧失被预测会驱动纹状体乙酰胆碱(ACh)水平的增加,但这种变化如何转化为改变的胆碱能传递仍不清楚。因此,研究人员还检查了DA损伤动物中dMSNs在M4受体突触上的ACh传递变化。结果表明,6-OHDA处理的小鼠中M4-IPSCs的幅度显著减少,即通过M4受体传递到dMSNs的胆碱能传递在多巴胺能输入退化后减少。进一步的实验还验证了乙酰胆碱酯酶(AChE)介导的ACh清除功能没有变化,说明胆碱酯酶介导的ACh清除没有功能性改变。
在帕金森病小鼠模型中,研究人员通过圆柱测试和旋转杆测试评估运动功能。圆柱测试用于评估前肢使用的不对称性,小鼠被单独放置在一个透明的塑料圆柱体中,后方放置镜子以便观察,并进行5分钟的视频录制以便后续评分。录制前不进行任何适应训练,仅记录小鼠用完全伸展的爪子接触圆柱壁的次数。数据以注射侧对侧前肢触碰次数占总前肢使用次数的百分比表示。圆柱测试中运动缺陷的存在被用作将小鼠纳入帕金森实验组的标准,并设定对侧爪使用率低于40%为阈值。小鼠的旋转杆测试则用于评估运动平衡和协调能力,采用从3到30转/分钟的加速协议,持续5分钟。每只小鼠在同一天进行三次试验,每次试验间隔10分钟,同样不进行事先训练。记录小鼠掉落的潜伏期或达到最大速度的时间,数据取两次最佳试验的平均值。通过这些测试,研究人员能够量化帕金森病模型小鼠的运动功能缺陷,并评估潜在治疗方法的效果。
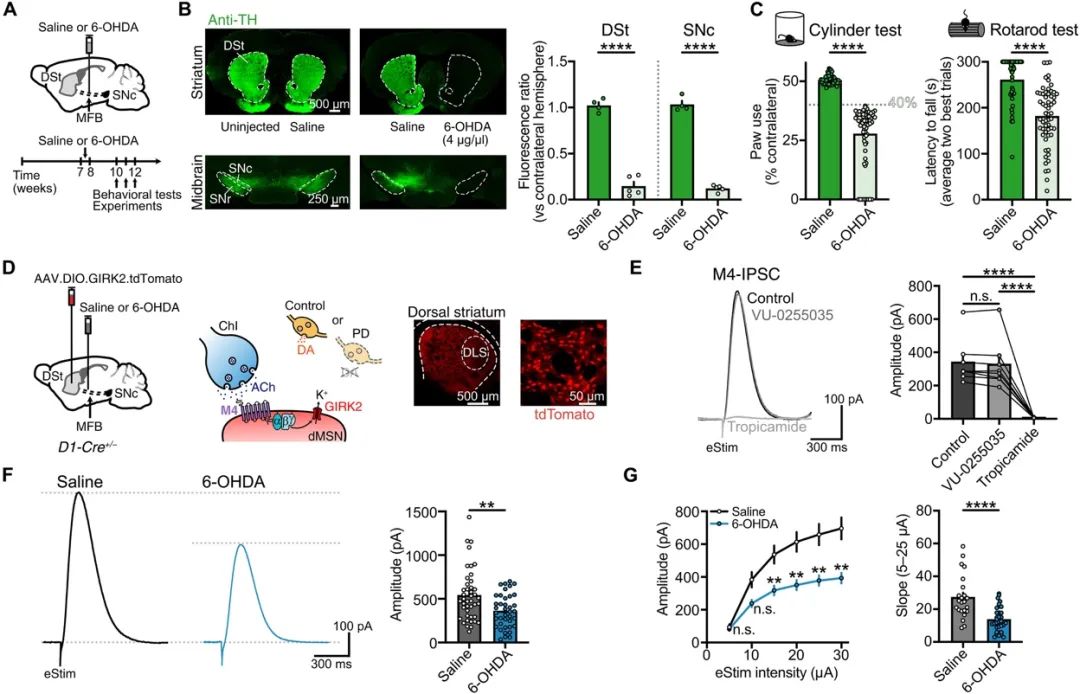
图1 DA耗竭减少M4介导的胆碱能突触传递
为了探究DA耗竭对直接通路中M4介导的胆碱能信号传导的影响,研究人员向小鼠的MFB单侧注射6-羟基多巴胺(6-OHDA),以诱导纹状体DA输入的退化。结果显示,6-OHDA处理的小鼠中M4-IPSCs的幅度显著减少,表明M4受体信号传导的减少是由于突触后M4受体功能的减弱,而非GIRK2表达的差异,部分原因是M4受体表达的减少。研究还在MitoPark小鼠模型中验证了这一发现,该模型通过选择性敲除线粒体转录因子A(Tfam)基因导致DA神经元的线粒体功能障碍和逐渐退化。结果表明,MitoPark小鼠中M4-IPSCs的幅度和Oxo-M(oxotremorine-M)诱导的最大外向电流均减少。此外,通过测量M4受体介导的电压门控钙通道(voltage-gated calcium channels, VGCCs)抑制,研究人员发现DA耗竭后dMSNs中M4受体信号传导减少。这些结果表明,DA耗竭导致的直接通路M4信号传导减弱,可能在帕金森病的病理生理中起重要作用。
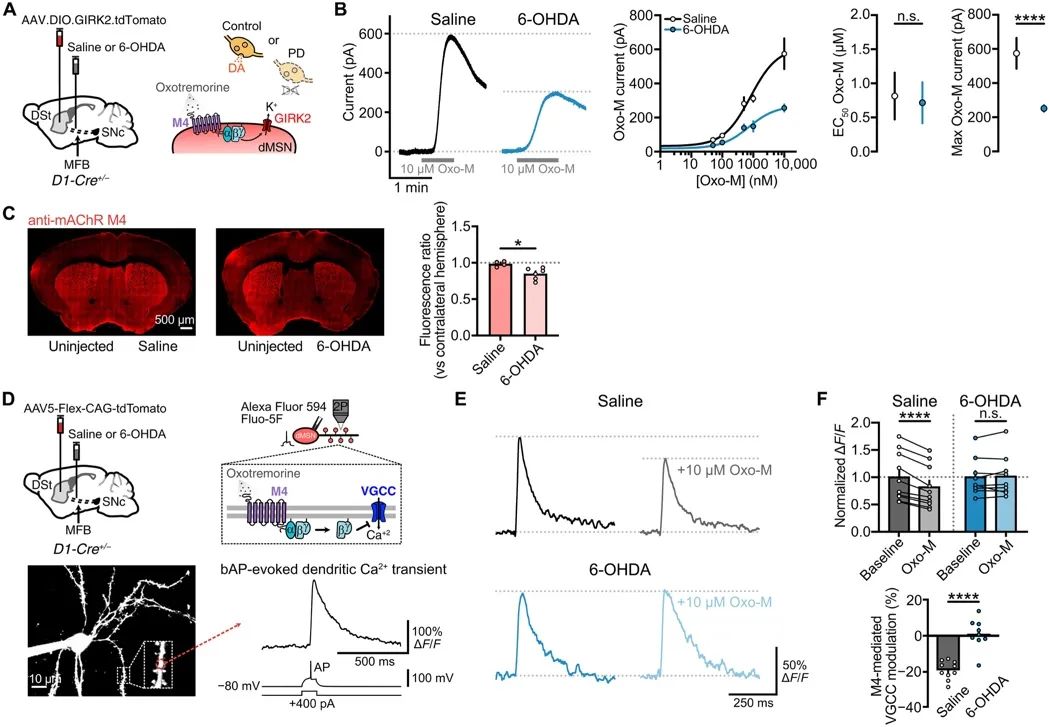
图2 DA耗竭降低dMSNs突触后M4受体功能
为了恢复传导功能的损伤,研究人员设计了一种腺相关病毒Adeno-associated virus, AAV),编码Cre依赖的M4受体和荧光报告蛋白增强型绿色荧光蛋白(eGFP),以测试在dMSNs中选择性过表达是否能挽救帕金森小鼠中的胆碱能信号缺陷。注射AAV.DIO.M4.eGFP三周后,注射半球的M4免疫反应性增加了约25%。在D1-Cre小鼠中共同注射AAV.DIO.M4.eGFP和AAV.DIO.GIRK2.T2A.tdTomato,导致重叠神经元群体中广泛表达eGFP和tdTomato荧光。记录显示,M4过表达小鼠中M4-IPSCs和Oxo-M诱导的M4介导外向电流的幅度均大于对照小鼠。M4受体的过表达恢复了DA耗竭后M4介导的胆碱能传导的损伤。尽管M4信号传导被认为在直接通路中起到抑制作用,但研究发现,M4受体的过表达改善了帕金森小鼠在平衡和协调任务中的运动表现(如旋转杆和平衡梁测试)。M4过表达小鼠在这些任务中的表现与对照组相似,表明恢复M4介导的胆碱能传导可以改善帕金森运动障碍,而不会进一步损害运动功能。
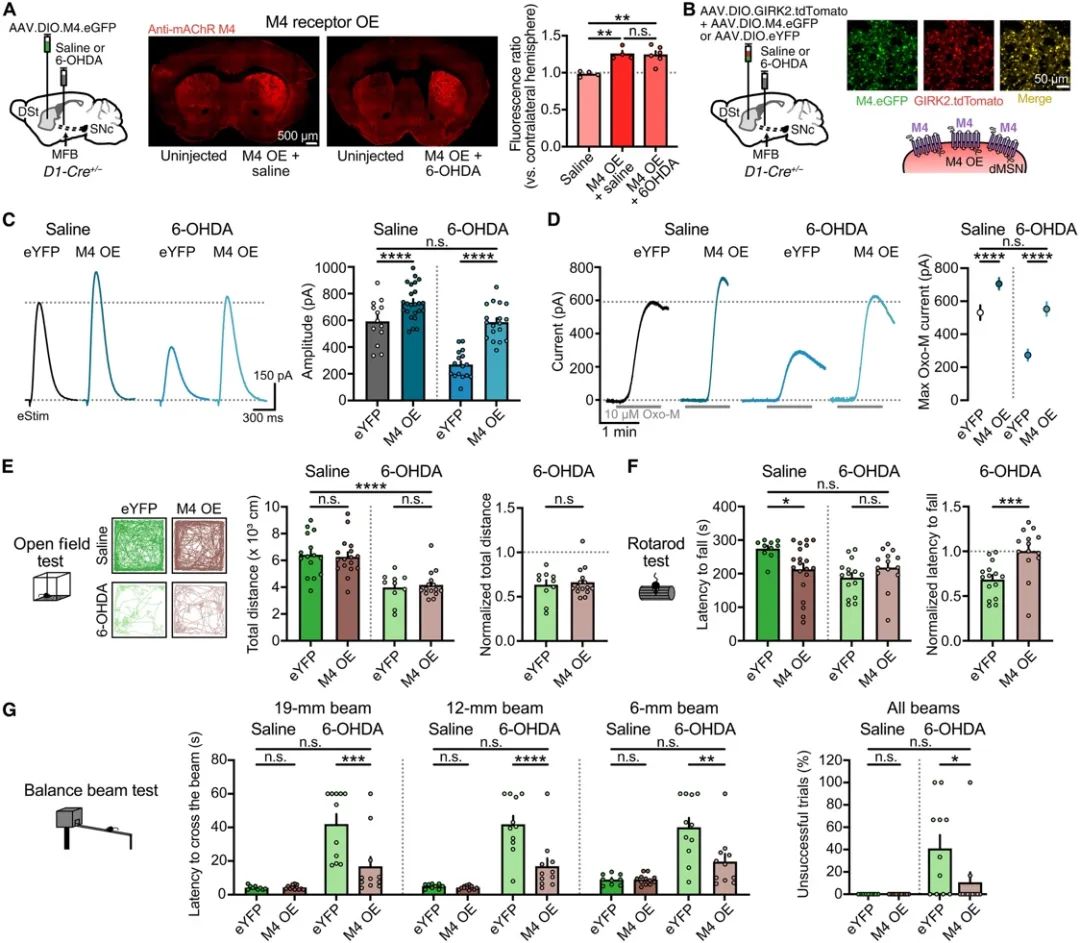
图3 M4受体在dMSNs中的过度表达可恢复帕金森小鼠胆碱能传递并改善运动缺陷

图3 M4受体在dMSNs中的过度表达可恢复帕金森小鼠胆碱能传递并改善运动缺陷
为了探究M4受体突触后功能减少的原因,研究人员生成了选择性缺失G蛋白信号调节蛋白(RGS4)的dMSNs小鼠。RGS4调节Gq和Gi/o偶联的G蛋白偶联受体(GPCRs)信号传导,缺失RGS4的小鼠中M4-IPSCs的幅度增加,激活和去激活的动力学延长,表明RGS4在调节dMSNs中的M4信号传导中起重要作用。最大外向电流也增加,而M4受体的敏感性未受影响。接下来,研究人员在6-OHDA处理的小鼠中进行了完全的DA损伤,发现缺失RGS4的小鼠中M4-IPSCs的幅度恢复到与生理盐水处理的对照组相似。选择性缺失RGS4的小鼠在旋转杆和开放场运动活动中的表现略有受损,但在校正这些基础损伤后,发现6-OHDA处理的小鼠中运动功能得到恢复,包括旋转杆上的滞留时间和穿越平衡梁的时间。缺失RGS4的小鼠在平衡梁测试中的基础表现未受影响,但在6-OHDA诱导的运动缺陷中表现出部分恢复,包括穿越梁的时间减少、脚滑次数减少和由于启动运动犹豫导致的不成功试验百分比减少。这些结果表明,DA损伤后突触后M4功能的减少可能导致帕金森运动功能障碍的某些方面。
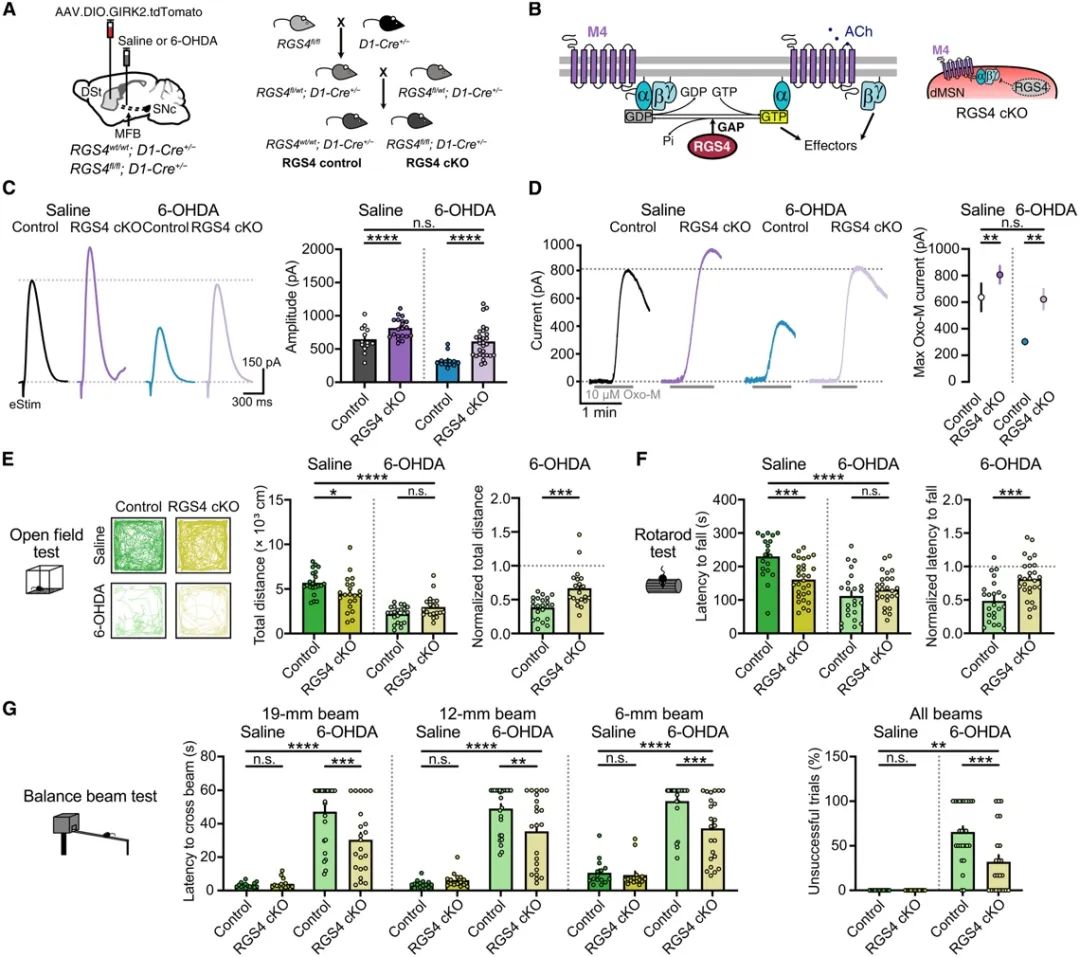
图4 在dMSNs中选择性消融RGS4可以恢复M4传递,并缓解帕金森小鼠的运动障碍
为了探究DA耗竭后M4胆碱能传导减少对L-DOPA诱导的运动障碍行为的影响,研究人员在6-OHDA处理的小鼠中选择性去除dMSNs中的RGS4蛋白,并进行每日L-DOPA注射。结果显示,尽管L-DOPA治疗恢复了运动功能,但未能逆转M4功能的减少。通过分析运动活动和旋转频率,发现RGS4缺失小鼠在L-DOPA治疗后运动功能得到改善,同时不影响其治疗效果。此外,RGS4缺失小鼠的异常不自主运动评分显著降低,表明恢复M4功能可以减轻L-DOPA诱导的运动障碍行为。这些结果表明,DA耗竭后直接通路中M4介导的胆碱能传导减少加速并加重了L-DOPA诱导的运动障碍,而恢复M4功能则改善了运动障碍行为,同时不影响L-DOPA的抗帕金森效果。
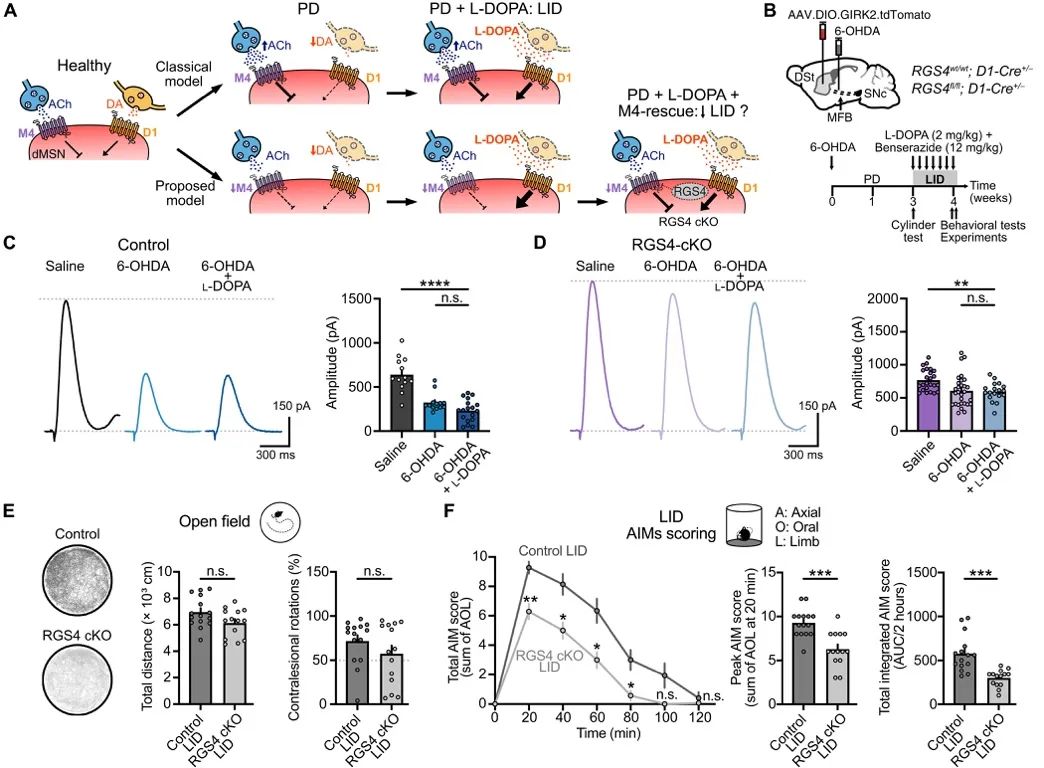
图5 M4传递的恢复减轻了L-DOPA引起的运动障碍行为
这项研究表明,多巴胺(DA)耗竭后,直接通路中M4介导的胆碱能信号传导减少,这种减少与帕金森病(PD)和左旋多巴(L-DOPA)诱导的运动障碍行为密切相关。研究人员通过恢复M4受体的功能,发现该方法可以部分缓解帕金森病的运动缺陷和L-DOPA诱导的运动障碍行为。这一研究发现揭示了M4受体在PD病理生理学中的潜在作用,并为未来的治疗策略提供了新的方向。未来的研究可以进一步探讨M4受体在不同PD模型中的作用,并开发针对M4受体的特异性药物,这可能为帕金森病和L-DOPA诱导的运动障碍提供更有效的治疗方法。此外,还可以探索其他胆碱能信号传导途径在PD中的作用,也将有助于全面理解该疾病的复杂机制。
原文地址:https://doi.org/10.1126/sciadv.adp6301
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




