- +1
Nature:严欢/石正丽团队首次提出人工设计病毒受体

编辑丨王多鱼
排版丨水成文
受体识别是病毒感染与传播过程中的关键事件。受体既是理解病毒进入宿主细胞机制的核心线索,也是构建感染模型、推动机制研究和药物研发的基础。然而,天然受体鉴定工作存在较高的不确定性与滞后性,有些重要病毒的受体鉴定几十年未有突破,严重阻碍了相关病毒学研究的深入推进。
2024年10月30日,武汉大学生命科学学院/病毒学国家重点实验室严欢团队、广州实验室/中国科学院武汉病毒研究所石正丽团队以及华盛顿大学David Veesler团队合作,在国际顶尖学术期刊 Nature 上发表了题为:Design of customized coronavirus receptors 的研究论文。
该研究首次提出了“定制化病毒受体(CVR)”的概念,旨在不依赖天然受体的条件下构建易感细胞模型。基于该技术,研究团队为多种冠状病毒成功设计了功能性人工受体,并通过合作深入探索了人工受体发挥功能的机制及其多方面的应用价值。

该设计策略采取类似于“乐高积木”的模块化设计思路,将完整受体分解为“病毒结合域(VBD)”与“人工受体框架(ARS)”两部分分别进行设计与优化。通过截取天然受体的多种结构与功能模块并重组得到具有一定兼容性的ARS,通过抗体改造、文库筛选、蛋白质从头设计等手段获得靶向特定表位的VBD作为特异性模块,最终通过分子嫁接生成候选受体(图1)。
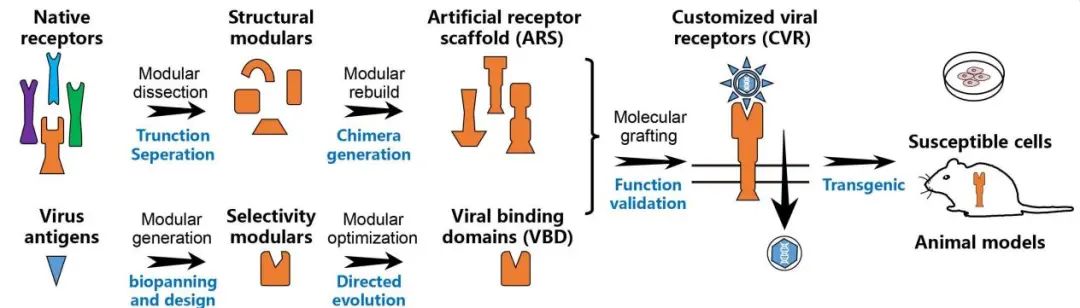
图1:人工病毒受体(CVR)的模块化设计思路
严欢团队从新冠病毒受体ACE2出发,通过不断截短、替换ACE2序列,发现受体可以被完全替换为不含任何ACE2序列的人工受体分子,并通过一系列生化与分子生物学手段揭示了影响受体功能性的关键因素,开发了一套适用于冠状病毒的人工受体模块化设计方案(图2)。在此基础上,研究团队通过对新冠病毒Spike蛋白的多种结合表位进行系统性测试,揭示了人工受体所识别的表位对受体功能性的重要影响,并阐明了其分子机制。
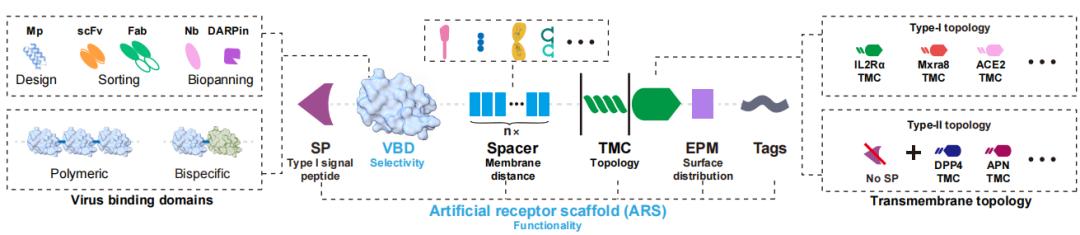
图2:冠状病毒定制化人工病毒受体示意图
值得一提的是,研究团队发现一种结合新冠病毒NTD特定表位的人工受体(S2L20-CVR),意外地可以通过结合经典的CTD受体结合域(RBD)之外的区域发挥功能,通过与David Veesler团队合作,揭示了这一特殊的功能性受体通过一种类似于“分子棘轮”的机制强制三个CTD结构域处于“开放”构像,进而发挥功能。这意味着SARS相关冠状病毒完全有能力利用NTD结合受体并实现有效入侵。
此外,研究团队发现,结合鼠肝炎冠状病毒(MHV)Spike蛋白 CTD结构域的人工受体也具有良好的受体功能性,这说明尽管MHV利用NTD识别其天然受体CEACAM1a,其CTD仍然保有充当RBD的能力。这些发现表明冠状病毒Spike蛋白可以兼容多种方式激活其融合机器并介导病毒入侵。
研究团队通过纳米抗体噬菌体文库淘选的手段获取了一系列特异性病毒识别模块,成功为来自6个不同亚属的12种冠状病毒设计了人工受体,其中多种病毒天然受体仍不明确(图3)。研究团队基于外源表达人工受体的工程化细胞,利用病毒膜融合实验、假病毒入侵实验以及可扩增型VSV嵌合病毒感染实验等手段验证了受体功能性。通过与石正丽团队合作,CVR感染模型成功实现了HKU5等冠状病毒的分离培养。这些工作为冠状病毒基础研究与抗病毒药物研发提供了具有重要价值的感染模型资源。
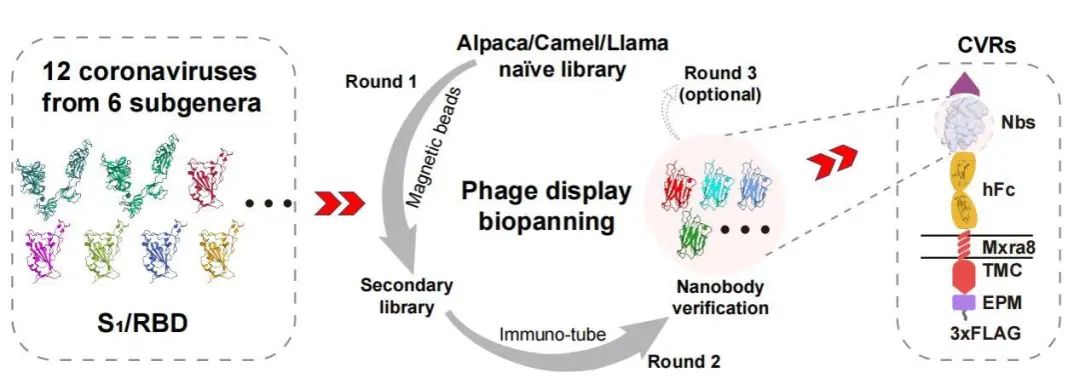
图3:利用纳米抗体淘选技术为不同冠状病毒定制化功能性受体
综上,该研究通过模块化设计思路,开发出一套兼容性、可拓展的人工病毒受体设计策略,成功实现了多种冠状病毒功能性受体的定制化设计。尽管本研究以冠状病毒为主要研究对象,理论上该策略也可以为其他自然存在的病毒设计受体,但实现最佳受体功能的难度可能因病毒而异。通过为一些受体未明且缺乏感染模型的病毒设计人工受体,有望突破病毒学研究瓶颈,促进相关病毒感染致病机制的基础研究以及疫苗与抗病毒药物的开发(图4)。
图4:人工病毒受体的科学与应用价值
严欢教授、石正丽研究员和David Veesler教授为该论文的共同通讯作者;武汉大学生命科学学院博士生刘鹏、硕士生黄美玲,中国科学院武汉病毒研究所博士后郭华,以及华盛顿大学Matthew McCallum为该论文的共同第一作者。
论文链接:
https://www.nature.com/articles/s41586-024-08121-5

本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




