- +1
范高峰/徐斌/杨小宝CCBio:靶向NAMPT的PROTAC与烟酸共给药的抗癌效果
原创 Cell Press CellPress细胞科学

生命科学
Life science
2024年6月20日,上海科技大学范高峰长聘副教授与上海交通大学医学院附属第九人民医院徐斌、标新生物创始人杨小宝博士在Cell Press细胞出版社期刊Cell Chemical Biology发表了题为“NAMPT-targeting PROTAC and nicotinic acid co-administration elicit safe and robust anti-tumor efficacy in NAPRT-deficient pan-cancers”的研究论文。该工作开发了具有更优代谢稳定性的新一代靶向NAMPT的PROTAC降解剂,其与烟酸联用在治疗NAPRT缺陷型泛癌中展示出安全性和有效性。
上海科技大学生命学院博士生朱小童、硕士生李椰、物质学院博士生刘海霞为共同第一作者。范高峰(上海科技大学生命学院)、徐斌(上海交通大学医学院附属第九人民医院)、杨小宝(标新生物)为本文的共同通讯作者。
▲长按图片识别二维码阅读原文
NAD+(烟酰胺腺嘌呤二核苷酸)是氧化还原反应的辅酶,参与能量合成、DNA修复等多种生理过程,肿瘤细胞具有高的有氧糖酵解效率,需要消耗更多的NAD+。NAMPT作为合成NAD+补救途径的关键限速酶在多种肿瘤细胞中高表达,使其成为癌症治疗的潜在靶点。NAMPT一方面在细胞内以iNAMPT的形式发挥酶活功能,负责NAD+的生物合成;另一方面还能分泌到细胞外以eNAMPT的形式发挥非酶活功能,促进肿瘤发生发展。前期靶向NAMPT的策略主要集中在传统酶活抑制剂的开发,但在临床上效果不佳。范高峰及合作者团队在先前的研究中利用蛋白降解靶向嵌合体(PROTAC)技术开发了两种化合物SIAIS630120和SIAIS630121,能够同时降解iNAMPT和eNAMPT两种形式的NAMPT蛋白,但是出现了与传统抑制剂类似的毒性问题。因此,解决靶向NAMPT带来的毒副作用至关重要。
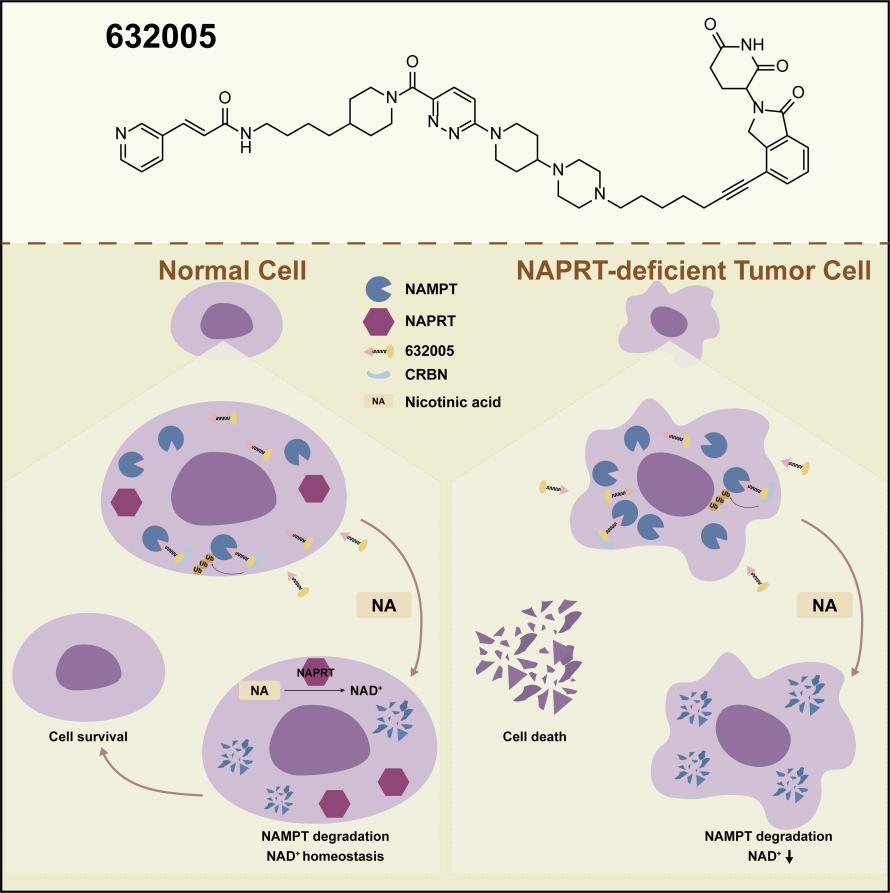
图 1 PROTAC联用烟酸(NA)减弱毒性示意图。
NAD+在机体内一共有三条合成途径,研究团队首先验证了多种肿瘤细胞对靶向NAMPT的PROTAC分子的敏感性,发现靶向NAMPT的PROTAC在NAPRT缺陷的肿瘤细胞中具有更好的杀伤效果,因此提出将NAPRT缺陷的癌症作为靶向NAMPT蛋白的PROTAC分子的适应症,同时联用烟酸(Nicotinic Acid)给药以减弱NAMPT靶点的毒副作用。
之后研究团队对已开发的PROTAC分子进行进一步优化得到了代谢稳定性更好的第二代PROTAC分子(632005),并证明在与烟酸联用时,可以在体内外有效地减弱靶向NAMPT的毒副作用。为了进一步评估联用烟酸给药对PROTAC抗肿瘤作用的影响,研究团队构建了血液恶性肿瘤、前列腺癌的异种移植模型以及来源于病人的肝癌PDX模型,证明了靶向NAMPT的PROTAC联用烟酸在NAPRT缺陷的泛癌中具有显著的抗肿瘤效果。
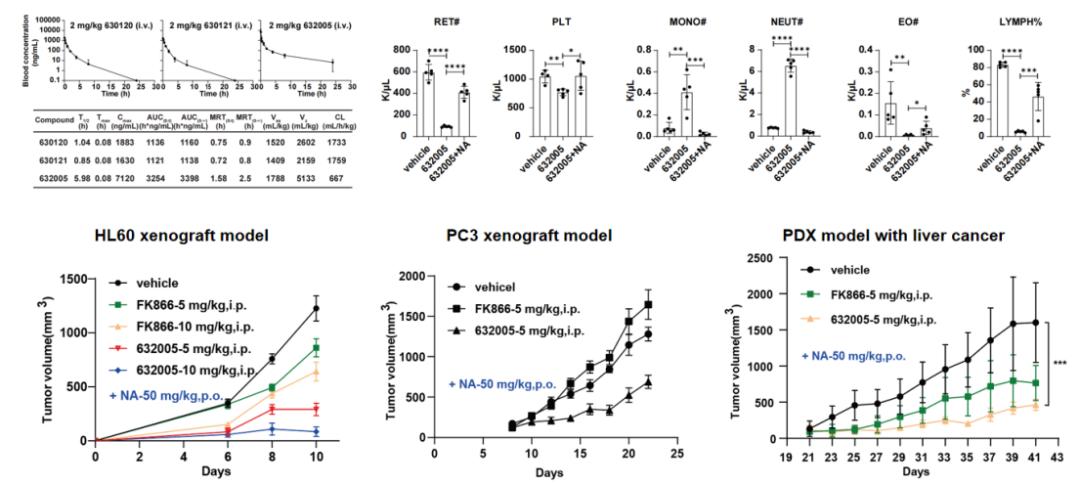
图 2 NAMPT-PROTAC联用烟酸(NA)在NAPRT缺陷的泛癌中显示出安全性和有效性。
总的来说,研究团队发现靶向NAMPT的PROTAC在NAPRT缺陷的肿瘤细胞中具有更好的杀伤效果。之后开发了第二代的PROTAC分子632005,当与烟酸联合使用时,能有效减弱毒副作用,并且在NAPRT缺陷的泛癌中显示出强大的抗肿瘤效果。该研究为NAMPT作为一个有前途的肿瘤治疗代谢靶点提供了信心,对未来临床环境中患者的选择以及安全有效的治疗策略的发展具有深远的意义。
作者专访
Cell Press细胞出版社公众号特别邀请范高峰长聘副教授进行了专访,为大家进一步详细解读。
CellPress:
近年来NAMPT抑制剂/PROTAC的研究现状如何?
范高峰长聘副教授:
近年来,NAMPT作为癌症治疗的潜在靶点受到了广泛关注。NAMPT抑制剂的研究始于其在NAD+合成中的关键作用,传统的NAMPT酶活抑制剂如FK866、CHS-828等已经在多种癌症模型中展示了抗肿瘤效果。然而,这些抑制剂临床效果不佳且面临显著的毒副作用,限制了其进一步的发展和应用。随着PROTAC技术的发展,研究者们开始探索利用PROTAC技术靶向NAMPT蛋白。PROTAC分子能够通过诱导蛋白质降解来消除目标蛋白,提供了一种不同于传统抑制剂的治疗策略。我们团队和其他研究团队已经开发了一些NAMPT-PROTAC分子,这些分子能够在细胞内外有效降解NAMPT蛋白,并展示了显著的抗肿瘤效果。
CellPress:
本文的亮点发现有哪些?
范高峰长聘副教授:
首先是新一代PROTAC分子的开发:我们在前期研究的基础上,进一步优化了PROTAC分子,开发了代谢稳定性更好的第二代PROTAC分子。其次是联合用药策略:通过与烟酸联用,我们显著减弱了靶向NAMPT带来的毒副作用。这一策略在体内外实验中均得到了验证。最后是特定癌症类型的靶向治疗:我们发现靶向NAMPT的PROTAC在NAPRT缺陷的肿瘤细胞中具有更好的杀伤效果,并提出将NAPRT缺陷的癌症作为适应症,展示了在血液恶性肿瘤、前列腺癌和肝癌等模型中的显著抗肿瘤效果。
CellPress:
本文的科学意义是什么?
范高峰长聘副教授:
通过开发新一代PROTAC分子并与烟酸联用,我们为靶向NAMPT的抗癌治疗提供了一种新的、安全有效的策略。此外,我们发现NAPRT缺陷的癌症对NAMPT靶向治疗更为敏感,为未来临床上患者的选择提供了重要依据。总的来说,我们的研究展示了PROTAC技术在靶向癌症治疗中的潜力,推动了该技术在药物开发中的应用。
CellPress:
基于本文的研究,您觉得接下来还有哪些值得深入探索的方向?
范高峰长聘副教授:
尽管靶向NAMPT的PROTAC技术展示了良好的前景,但其临床转化仍面临诸多挑战,包括药物的代谢稳定性、体内分布、毒性评估等。未来的研究需要进一步优化PROTAC分子的结构,提高其药物特性,并通过更多的临床前研究验证其安全性和有效性。
CellPress:
最后,请与我们分享一下选择Cell Chemical Biology来发表这项工作的理由。
范高峰长聘副教授:
Cell Chemical Biology是国际知名的高影响力期刊,专注于化学生物学领域的前沿研究,能够为我们的研究提供广泛的学术传播平台。该期刊的读者包括众多化学生物学和药物开发领域的专家和研究人员,能够帮助我们的研究成果迅速传播到相关领域,促进学术交流和合作。并且Cell Chemical Biology的评审过程专业且严谨,能够确保我们的研究得到高质量的评审和反馈。

作者介绍

范高峰
长聘副教授
范高峰,上海科技大学长聘副教授、研究员、博士生导师。2017年加入上海科技大学生命科学与技术学院,课题组一直聚焦肿瘤免疫和代谢调控,以最后通讯作者在Nature structural & Molecular Biology(2023)、eLife(2022)、Cell Chemical Biology(2024,2022封面文章)、Cell Reports(2023、2021)、JBC(2023、2019)等期刊发表论文,申请国际、国内专利3项,获批国际专利1项。课题组先后获得科技部重点研发、基金委面上项目、上海市“科技创新行动计划”基础研究项目等支持。获得上海市“曙光学者”(2019)、“东方学者”特聘教授(2018)和“浦江人才”计划(2018)支持。2022年获得“东方学者”特聘教授跟踪计划持续支持。担任美国癌症研究协会、美国生物化学和分子生物学协会以及美国细胞生物学协会正式会员,同时担任Cancer Research、eLife、Cell Reports等期刊的特邀审稿人。2018年、2021年、2022年三获上海科技大学年度优秀教师。

徐斌
主任医师
徐斌,九院泌尿外科行政主任、主任医师、博士生导师。美国纽约犹太医学中心Research Fellow(2011)社会任职:中华医学会泌尿外科学分会工程学组委员,中国抗癌协会介入治疗专委员,肿瘤消融专家委员会副主任委员,中国中西医结合泌尿外科学会青年委员,上海市医学会泌尿外科专科分会委员,上海市医师协会泌尿外科医师分会委员,上海市医学会男科专科分会秘书兼性功能障碍学组副组长,健康指南编委会委员。获奖荣誉:先后入选上海市教委“晨光学者”计划、上海市高校青年教师培养计划、上海市科委科技启明星、上海市“医苑新星”杰出青年医学人才、东方英才计划青年项目、上海交大双百人、上海市医学会泌尿外科分会“青年英才”等人才计划。科研成果:第一完成人获军队医疗成果三等奖1项,作为主要骨干,在国内率先开展了多项单孔腹腔镜技术,制定国际首个单孔腹腔镜专用培训教程。2010年6月起在上海市首家开展超声引导下经会阴氩氦刀前列腺癌冷冻术,2012年3月起率先在国内开展单孔腹腔镜下肾肿瘤冷冻消融术。主持国家自然基金4项、省部级基金8项,金额计5百余万元。曾获上海市优秀博士论文,第一或通讯发表SCI论文30余篇,总IF大于200分。获国家实用新型专利6项;参编专著2部。

杨小宝
博士
杨小宝,标新生物董事长兼首席运营官。原上海科技大学助理研究员,美国西奈山医学院和美国北卡罗来纳教堂山分校博士后,上海东岳药业研发部总工程师,葛兰素史克上海研发中心研究员。2013年出国加入金坚教授课题组,其在美国北卡教堂山分校和西奈山伊坎医学院任博士后,并一直在蛋白降解领域深耕,从事蛋白降解小分子药物的设计开发,期间研究工作最终发表在Nature Cancer、Nature Chemical Biology、Nature Communication、J Med Chem 和 Eur J Med Chem 等国际知名期刊上,并申请了该领域相关专利。2016年回国后加入上海科技大学免疫化学研究所姜标教授课题组任助理研究员,并组建了蛋白降解药物研发团队。在上科大任职期间作为通讯作者在J Med Chem、Org Lett、Eur J Med Chem、Org Biomol Chem等国际知名期刊上发表蛋白降解相关学术论文,同时申请该领域专利,并成功实现了和径医药和标新生物的两次科研转化。2021年初全职加入标新生物,并建立分子胶和PROTAC两大平台,从事于蛋白降解小分子药物的研发工作。
相关论文信息
论文原文刊载于Cell Press细胞出版社旗下期刊Cell Chemical Biology上,点击“阅读原文”或扫描下方二维码查看论文
▌论文标题:
NAMPT-targeting PROTAC and nicotinic acid co-administration elicit safe and robust anti-tumor efficacy in NAPRT-deficient pan-cancers
▌论文网址:
https://www.sciencedirect.com/science/article/abs/pii/S2451945624002083
▌DOI:
https://doi.org/10.1016/j.chembiol.2024.05.007
▲长按图片识别二维码阅读原文
的前身Cell Press Community Review模式于2021年推出。对于通过Cell Press Multi-Journal Submission“多刊审稿”模式投稿的作者,我们将提供稿件被多本期刊同时考虑的机会。超过80%通过Cell Press Multi-Journal Submission“多刊审稿”模式投稿的文章获得了至少一个或多个期刊的评审。
CellPress细胞出版社
原标题:《范高峰/徐斌/杨小宝CCBio:靶向NAMPT的PROTAC与烟酸共给药的抗癌效果 | Cell Press对话科学家》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




