- +1
【科学普及】渐冻症与SOD1基因突变
原创 郑一诺 刘庆 细胞世界
基于SOD1基因异常的肌萎缩侧索硬化症发病机制及治疗进展
作者:
郑一诺 刘庆
指导教师:
贾蕊 胡劲松
作者单位:
西安交通大学第一附属医院神经内科
西安交通大学医学部基础医学院
关于渐冻症,有许多悲壮、悲情的人物故事。悲壮,缘于渐冻症病症之险峻,治疗之困难。
“渐冻症”学名为肌萎缩侧索硬化症(Amyotrophic Lateral Sclerosis, ALS),是一种成人起病的进行性、致命性的神经退行性疾病。病变主要累及上、下运动神经元,临床表现为全身肌肉进行性萎缩、肌肉无力伴随肌束震颤和锥体束损伤。ALS的高峰发病年龄为55-75岁,发病后多因呼吸肌无力导致呼吸衰竭而死亡,平均病程3-5年,中位生存期约27.5个月[1]。
在寻找突破点的征途中,SOD1基因是一个重要的对象。1993年,它被鉴定出与家族遗传型肌萎缩侧索硬化症(fALS)相关,这是人类医学历史上首个被认定与ALS有关的致病基因,定位于染色体21q22.11,分子量16kDa。目前已经发现了超过180种包括点突变、无义突变、移码突变等多种突变体的存在[2],约占家族性肌萎缩侧索硬化症的25.60%,散发性肌萎缩侧索硬化症的1.60%[3]。
SOD1基因的编码产物SOD1蛋白是超氧化物歧化酶(SOD)家族的3种同工酶之一,主要位于细胞质、细胞核和线粒体膜间隙中。SOD1是真核细胞抵抗活性氧(ROS)的抗氧化应激酶系中的重要成员,主要通过将超氧自由基转化为分子氧和过氧化氢,抵御细胞内的氧化应激,对维持细胞正常的生理功能有重要作用[4]。
01 SOD1基因突变引起渐冻症的机制
近年来基于大量研究发现,SOD1相关的ALS发病机制主要体现在以下几个方面:
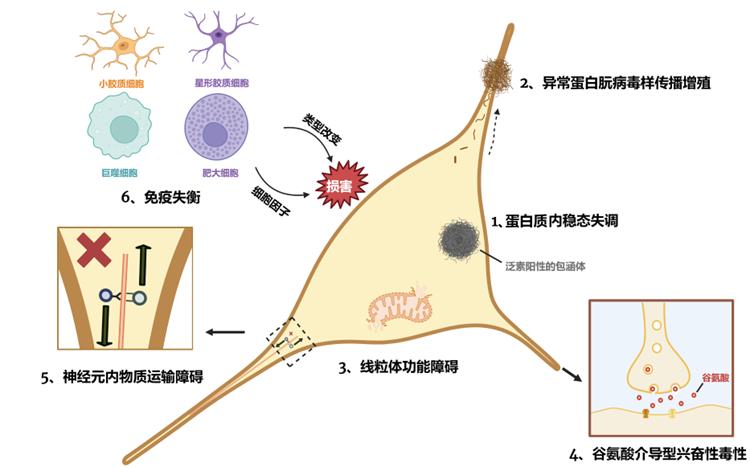 图1. SOD1基因突变引起渐冻症的机制
图1. SOD1基因突变引起渐冻症的机制(1)蛋白质内稳态失衡
SOD1基因突变可使其编码的蛋白质结构不稳定,造成错误折叠或不折叠,使蛋白不易被降解[5]。同时,干扰蛋白酶体和自噬系统正常活性[6],进而导致异常蛋白质在神经元内过度积聚,诱发内质网应激、激活泛素-蛋白酶体系统,长时间内质网应激反应可诱发神经细胞凋亡。
(2)异常蛋白质的朊病毒样增殖和传播
SOD1具有朊病毒样增殖和传播特性[7],通过把正常蛋白质转变为异常构象的蛋白质来实现自我增殖,并得以沿着神经元传播,具有细胞毒性。梁毅课题组研究发现,在SOD1错误折叠过程中,脱辅基SOD1亚基的一个α螺旋和由8个β折叠组成的β桶状结构转变成SOD1纤维的13个β-折叠结构[8],首次在原子水平上揭示了朊蛋白由细胞型朊蛋白(PrPC)向病理型朊病毒蛋白(PrPSc)结构转变的机制。
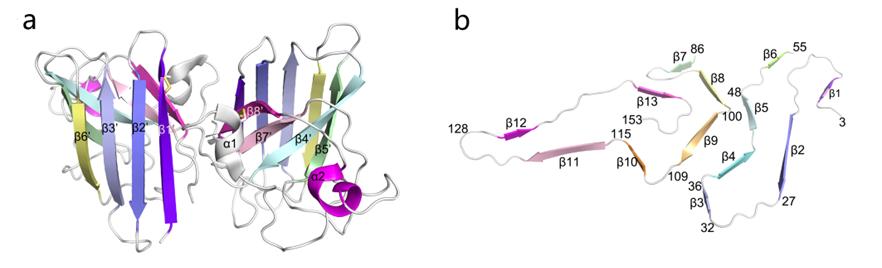 图2. 脱辅基人SOD1二聚体和SOD1纤维结构比较[8]:(a)正常SOD1蛋白二聚体结构;(b)异常SOD1蛋白纤维结构。
图2. 脱辅基人SOD1二聚体和SOD1纤维结构比较[8]:(a)正常SOD1蛋白二聚体结构;(b)异常SOD1蛋白纤维结构。(3)线粒体功能障碍
线粒体在细胞能量生成、物质代谢及调控细胞内钙离子稳态中发挥重要作用。SOD1基因突变会导致线粒体功能紊乱,包括线粒体钙缓冲能力降低、线粒体过度分裂及活性氧的生成、线粒体自噬激活,以及线粒体相关内质网膜 (Mitochondria-associated ER Membrane,MAM)的减少等[9]。异常的 SOD1 蛋白错误地定位于线粒体内外膜间隙,会造成线粒体损伤,引起线粒体形态变化,促进神经元凋亡[10]。此外,SOD1基因突变也会抑制ATP的合成,并进一步抑制钠-钾泵的功能,从而使神经元的电生理活动受损[11]。
(4)谷氨酸介导的兴奋性毒性
SOD1基因突变影响中枢神经系统谷氨酸的代谢及稳态,导致神经元过度暴露于谷氨酸等兴奋性神经递质中时,产生明显的毒性反应[10]。
(5)神经元内物质运输障碍
SOD1基因突变可抑制神经元中动力蛋白介导的神经元逆向轴突运输。此外,还可通过影响其编码蛋白质的表达水平或磷酸化水平,间接抑制驱动蛋白介导的神经元顺向轴突运输,导致受体信号转导、突触功能、基因调控、能量代谢、废物降解等功能受到明显的损害[12]。
(6)免疫失衡
神经炎症和免疫失衡被认为能够促进ALS的发生和发展。小鼠模型研究显示,在表达突变型SOD1的疾病晚期,免疫细胞和因子向对神经元产生毒性和损伤作用的方向转变[13]——小胶质细胞趋向M1型,对运动神经元产生毒性;表达突变型SOD1的星形胶质细胞对运动神经元有毒性,介导ALS的神经炎症;ALS中期单核细胞浸润致小胶质细胞活化,加重神经炎症;肥大细胞分布于肌肉和坐骨神经,损害轴突的完整性;补体系统局部激活,有助于巨噬细胞募集,加速疾病进展。
02 渐冻症的治疗
由于ALS的发病机制尚未明确,美国FDA批准用于ALS治疗并在我国上市的药物仅有利鲁唑(Riluzole)和依达拉奉(Edaravone)[14]。2022年,也出现了治疗ALS的新药——苯丁酸钠和牛磺酸二醇口服联合制剂(Relyvrio)[15]。2023年,首个靶向ALS遗传病因的基因治疗药物Qalsody(也称Tofersen)在美国获批上市 [16]。
1. 已经获批的用于治疗渐冻症的药物
表1. 美国食品药品监督管理局(FDA)批准治疗肌萎缩侧索硬化症(ALS)药物
 (1)利鲁唑
(1)利鲁唑利鲁唑是目前治疗ALS的一线用药,通过降低谷氨酸水平来减少运动神经元的损伤,患者生存期平均延长2-3个月,对延髓性ALS的治疗效果较好[17]。
(2)依达拉奉
依达拉奉具有强大的自由基清除能力,能够抗氧化应激损伤,在疾病早期、症状较轻时具有较好的改善肌力和延缓疾病进展的作用[18]。
(3)苯丁酸钠和牛磺酸二醇口服联合制剂
2022年9月,苯丁酸钠和牛磺酸二醇口服联合制剂(Relyvrio)获美国食品药品监督管理局(FDA)正式批准,成为FDA批准的第三种治疗ALS的药物;该药物通过减轻内质网应激和线粒体功能障碍来减少神经细胞死亡[19],可延长患者生存期。然而,2024年3月8日美国Amylyx公司宣布Relyviro未通过三期临床试验,在上市2年后面临退市可能。
(4)托夫生(Toferson)
2023年4月,美国FDA批准了首个靶向ALS遗传病因的基因治疗药物Qalsody(Toferson),该药物通过鞘内注射的方式靶向递送反义寡核苷酸,减少毒性SOD1蛋白的产生,从而用于治疗SOD1相关ALS[16]。
2. 靶向突变SOD1治疗渐冻症药物研发现状
自1993年发现第一个ALS疾病基因SOD1以来,研究者们对该基因突变的致病机制及治疗策略不断进行研究探索,针对SOD1突变的药物也已经出现。其药物研发的策略通常为抑制突变体合成和清除已生成的突变蛋白,目前正在研发的新型药物主要包括:
(1)新型基因治疗载体腺相关病毒9(adeno-associated virus 9,AAV9),在系统给药时能够透过血脑屏障并有效靶向神经元和星形胶质细胞,利用此技术的AAV9-SOD1 短发夹RNA(shRNA)在 ALS 动物模型上能延迟发病时间并减缓病程发展[20]。
(2)除了沉默 SOD1 基因,反义寡核苷酸ISIS333611也被发现能够从mRNA水平降低突变体的表达,延长SOD1小鼠寿命[21]。基于此技术的Ⅰ期临床试验也证实鞘内注射具有良好的安全性。
(3)热休克蛋白(heat shock protein,HSP)是一种内源性细胞保护蛋白,能够改善轴突运输。阿莫氯醇(arimoclocol)能直接诱导神经元、肌肉细胞和胶质细胞中HSP70/90的表达[22],加速突变SOD1毒性的清除,维持神经对肌肉的支配,改善神经肌肉机能。
(4)在清除突变蛋白上,抗人突变 SOD1单抗AP-101作为为SOD1抑制剂,也在开发之中[14]。
综上所述,渐冻症发病的机制不明且复杂,除了SOD1基因外,还有其他致病基因有待阐明。我们期待着,基于对肌萎缩侧索硬化症的致病机制更深入的认识,以及基因治疗手段的快速崛起与发展,不久的将来能够迎来“破冰”良药。
参考文献:
[1] Marin B, Logroscino G, Boumédiene F, Labrunie A, Couratier P, Babron MC, Leutenegger AL, Preux PM, Beghi E. Clinical and demographic factors and outcome of amyotrophic lateral sclerosis in relation to population ancestral origin[J]. Eur J Epidemiol, 2016, 31:229⁃245.
[2] 赵倩倩, 李宛真, 唐北沙, 等. 肌萎缩侧索硬化症遗传学机制研究进展[J] . 中国现代神经疾病杂志, 2023,23(03):264-269.
[3] Qianqian W, Xueping C, Yongping C, et al. Unique characteristics of the genetics epidemiology of amyotrophic lateral sclerosis in China[J]. Science China(Life Sciences), 2019,62(04):517-525.
[4] Kim G, Gautier O, Tassoni-Tsuchida E, Ma XR, Gitler AD. ALS Genetics: Gains, Losses, and Implications for Future Therapies. Neuron. 2020 Dec 9;108(5):822-842.
[5] Nishitoh H, Kadowaki H, Nagai A, et al. ALS-linked mutant SOD1 induces ER stress- and ASK1-dependent motor neuron death by targeting Derlin-1[J]. Genes Dev, 2008, 22(11):1451- 1464.
[6] Scotter EL, Chen HJ, Shaw CE. TDP-43 proteinopathy and ALS: Insights into disease mechanisms and therapeutic targets [J]. Neurotherapeutics, 2015, 12(2): 352-363.
[7] Madji Hounoum B, Mavel S, Coque E, et al. Wildtype motoneurons, ALS-Linked SOD1 mutation and glutamate profoundly modify astrocyte metabolism and lactate shuttling [J]. Glia, 2017, 65(4): 592-605.
[8] Wang L Q, Ma Y, Yuan H Y, et al. Cryo-EM structure of an amyloid fibril formed by full-length human SOD1 reveals its conformational conversion[J]. Nat Commun, 2022,13(1):3491.
[9] 郑志隆,郭兴. 肌萎缩侧索硬化症疾病进展与线粒体功能紊乱[J] . 中山大学学报(医学科学版),2022,43(5):697-704.
[10] Vehviläinen P, Koistinaho J, Gundars G. Mechanisms of mutant SOD1 induced mitochondrial toxicity in amyotrophic lateral sclerosis. Front Cell Neurosci. 2014 May 9;8:126.
[11] Hayashi Y, Homma K, Ichijo H. SOD1 in neurotoxicity and its controversial roles in SOD1 mutation-negative ALS[J]. Adv Biol Regul, 2016, 60: 95-104.
[12] Burk K, Pasterkamp RJ. Disrupted neuronal trafficking in amyotrophic lateral sclerosis[J] . Acta Neuropathol, 2019, 137 (6): 859-877.
[13] 蔡青,李梦雅,李桂凤等. 肌萎缩侧索硬化症的免疫机制研究进展[J]. 现代免疫学,2023,43(2):169-174.
[14] 李栩琳,杨婉琪,王贵彬等. 肌萎缩侧索硬化症治疗药物研发进展[J] . 中国药理学与毒理学杂志,2018,32(3):223-232. DOI:10.3867/j.issn.1000-3002.2018.03.009.
[15] 潘芳,曹静. 治疗肌萎缩侧索硬化症新药Relyvrio [J]. 中国临床药理学杂志,2023,39(17):2552-2555.
[16] van Roon-Mom W, Ferguson C, Aartsma-Rus A. From Failure to Meet the Clinical Endpoint to U.S. Food and Drug Administration Approval: 15th Antisense Oligonucleotide Therapy Approved Qalsody (Tofersen) for Treatment of SOD1 Mutated Amyotrophic Lateral Sclerosis. Nucleic Acid Ther. 2023 Aug;33(4):234-237.
[17] Dharmadasa T, Kiernan MC. Riluzole, disease stage and survival in ALS. Lancet Neurol. 2018 May;17(5):385-386.
[18] Rothstein JD. Edaravone: A new drug approved for ALS. Cell. 2017 Nov 2;171(4):725.
[19] Paganoni S, Macklin EA, Hendrix S, Berry JD, Elliott MA, Maiser S, Karam C, Caress JB, Owegi MA, Quick A, Wymer J, Goutman SA, Heitzman D, Heiman-Patterson T, Jackson CE, Quinn C, Rothstein JD, Kasarskis EJ, Katz J, Jenkins L, Ladha S, Miller TM, Scelsa SN, Vu TH, Fournier CN, Glass JD, Johnson KM, Swenson A, Goyal NA, Pattee GL, Andres PL, Babu S, Chase M, Dagostino D, Dickson SP, Ellison N, Hall M, Hendrix K, Kittle G, McGovern M, Ostrow J, Pothier L, Randall R, Shefner JM, Sherman AV, Tustison E, Vigneswaran P, Walker J, Yu H, Chan J, Wittes J, Cohen J, Klee J, Leslie K, Tanzi RE, Gilbert W, Yeramian PD, Schoenfeld D, Cudkowicz ME. Trial of Sodium Phenylbutyrate-Taurursodiol for Amyotrophic Lateral Sclerosis. N Engl J Med. 2020 Sep 3;383(10):919-930.
[20] Foust KD, Salazar DL, Likhite S, Ferraiuolo L, Ditsworth D, Ilieva H, Meyer K, Schmelzer L, Braun L, Cleveland DW, Kaspar BK. Therapeutic AAV9-mediated suppression of mutant SOD1 slows disease progression and extends survival in models of inherited ALS. Mol Ther. 2013 Dec;21(12):2148-59.
[21] Miller TM, Pestronk A, David W, Rothstein J, Simpson E, Appel SH, Andres PL, Mahoney K, Allred P, Alexander K, Ostrow LW, Schoenfeld D, Macklin EA, Norris DA, Manousakis G, Crisp M, Smith R, Bennett CF, Bishop KM, Cudkowicz ME. An antisense oligonucleotide against SOD1 delivered intrathecally for patients with SOD1 familial amyotrophic lateral sclerosis: a phase 1, randomised, first-in-man study. Lancet Neurol. 2013 May;12(5):435-42.
[22] Vígh L, Literáti PN, Horváth I, et al. Bimoclomol: a nontoxic, hydroxylamine derivative with stress protein-inducing activity and cytoprotective effects. Nature Medicine. 1997 Oct;3(10):1150-1154.
原标题:《【科学普及】渐冻症与SOD1基因突变》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




