- +1
Cell Res:颜宁最新论文,为新型抗癫痫药物和镇痛药物开发奠定基础
原创 生物世界

编译丨王聪
编辑丨王多鱼
排版丨水成文
电压门控钙离子(Cav)通道在介导膜去极化时钙离子(Ca2+)的内流中至关重要。它们在Ca2+依赖的生理过程中发挥重要作用,例如神经递质/激素释放、基因表达和肌肉收缩等。钙通道活性的精确控制涉及多种细胞因子(例如受体、钙调蛋白、磷脂和G蛋白)。此外,这些通道可以被一系列离子、毒素和许多在研药物所调节。
在Cav通道中,Cav3.2亚型因其在疼痛和癫痫中的作用而成为开发镇痛药和抗癫痫药的靶点。
2024年4月11日,颜宁团队在 Cell Research 期刊发表了题为:Structural basis for human Cav3.2 inhibition by selective antagonists 的研究论文。
该研究解析了Cav3.2及其与4种T型钙通道选择性拮抗剂形成的复合物的高分辨率结构,揭示了其结合和作用机制,为选择性靶向Cav3.2的抗癫痫药物和镇痛药物的开发或改造奠定了基础。

在哺乳动物的10种Cav亚型(Cav1.1-Cav1.4、Cav2.1-Cav2.3和Cav3.1-Cav3.3)中,Cav3亚家族,也被称为T型钙通道,其特征是小而短暂的电流,而不是大而和持久的L型Cav1通道。与Cav1和Cav2成员不同,T型钙通道的功能独立,而Cav1和Cav2成需要多个辅助亚基来进行离子通道活动。此外,Cav1和Cav2通道在高电压下被激活,因此也被称为高电压激活(high voltage-activated,HVA)通道,Cav3通道为低电压激活(low voltage-activated,LVA)通道。LVA和HVA通道之间的大量序列差异支持了它们的功能差异,这为开发针对Cav亚型的特异性调节剂提供了机会。
Cav3.2由CACNA1H基因编码,在中枢神经系统(CNS)中广泛表达,调节神经元兴奋性,参与疼痛感。其活动的改变与许多神经和神经精神疾病相关,包括特发性全身性癫痫和疼痛。研究表明,在各种炎症和神经病理性疼痛模型中,Cav3.2在脊髓背角和背根神经节神经元中表达和/或活性增加。
基因沉默或药物抑制Cav3.2通道可诱导对啮齿动物的镇痛作用。因此,Cav3.2有望作为开发新一代镇痛药物的新靶点。靶向Cav3.2的化合物,如乙琥胺(ethosuximide)、米贝地尔(mibefradil)、丙戊酸盐(valproate)、唑尼沙胺(zonisamide)、吡莫齐特(pimozide)和某些二氢吡啶(DHP),在急性疼痛、炎症性疼痛和慢性疼痛的啮齿动物模型中显示出疗效。
目前正在研究各种具有新型化学骨架的小分子作为潜在的镇痛候选药物,例如Z944、TTA-A2、TTA-P2、ML218和ACT-709478。与通常对T型钙通道(Cav3)特异性有限的已批准药物相比,这些正在研究的T型特异性阻滞剂对T型Cav通道具有更强的亲和力。尽管这些化合物尚未进一步区分T型亚型,但与Cav3.1和Cav3.3相比,Cav3.2独特的药代动力学特性为开发真正的Cav3.2选择性分子提供了机会。
获得与FDA批准的药物或先导化合物复合的钙通道的高分辨率结构,对于指导从头设计或优化药物至关重要。在这项研究中,研究团队尝试确定人Cav3.2单独的以及其与4种T型钙通道选择性拮抗剂形成的复合物的冷冻电镜结构,总体分辨率从2.8 Å到3.2 Å,这4种化合物显示两种结合姿势。
ACT-709478和TTA-A2都将其含环丙基苯基的末端放置在中央腔中,直接阻碍离子流动,同时将其极性尾延伸到IV-I窗孔中。TTA-P2和ML218将它们的3,5-二氯苯甲酰胺基团投射到II-III窗孔中,并将它们的疏水尾部放置在空腔中,以阻止离子渗透。窗孔-穿透模式立即为这些拮抗剂的状态依赖性活动提供了解释。结构指导的突变分析确定了几个决定这些药物的T型钙通道偏好的关键氨基酸残基。这些结构也提示内源性脂质在稳定中央腔内药物结合方面的作用。
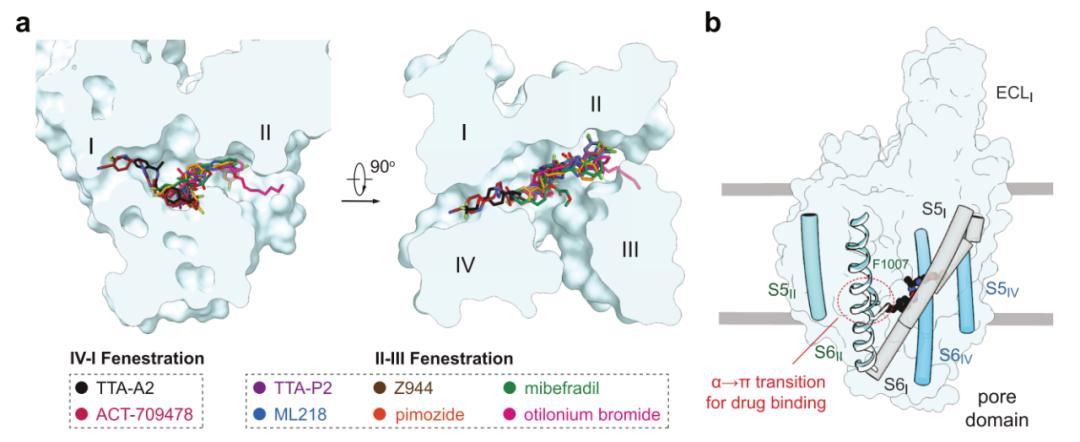
T型Cav通道中心腔内药物结合位点的结构图
Cav3.2已成为抗癫痫药物和镇痛药物开发的一个有希望的靶点。此外,自闭症、渐冻症、家族性醛固酮增多症等疾病也被发现与Cav3.2直接相关。该研究解析了Cav3.2及其与4种T型钙通道选择性拮抗剂形成的复合物的高分辨率结构,揭示了其结合和作用机制,为选择性靶向Cav3.2的抗癫痫药物和镇痛药物的开发或改造奠定了基础。
论文链接:
https://www.nature.com/articles/s41422-024-00959-8
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




