- +1
重磅发现:形成长期记忆,DNA损伤和大脑炎症必不可少
记忆是如何持续的?超现实主义画家萨尔瓦多·达利在他的名画《记忆的永恒》中思考了这个问题,20年后,他在《记忆的永恒的瓦解》中探讨了记忆丧失的悲剧性后果。
随着全球人口老龄化和阿尔茨海默病及相关痴呆症患病人数的快速增加,让记忆得以持续的机制引起了神经科学家的关注。然而,是什么使得哪怕短短几秒钟的短暂经历能够铭记一生,这仍然是个谜。
2024年3月27日,阿尔伯特-爱因斯坦医学院的研究人员在国际顶尖学术期刊 Nature 上发布了题为:Formation of memory assemblies through the DNA-sensing TLR9 pathway 的研究论文。
该研究描述了对记忆至关重要的分子机制,并标记出新的神经元亚群,为记忆如何持续这个谜题提供了关键答案。研究团队惊讶地发现,没有DNA损伤和大脑炎症,大脑就无法形成长期记忆。
海马体一直被认为是大脑的记忆中心。该研究显示,刺激会引发海马体中的特定神经元的DNA损伤和修复周期,从而导致稳定记忆的细胞群(一群代表了过去经历的大脑细胞)。

论文通讯作者、阿尔伯特-爱因斯坦医学院的 Jelena Radulovic 教授表示,大脑神经元的炎症通常被认为是一件坏事,因为它可能导致阿尔茨海默病和帕金森病等神经系统问题。而这项研究表明,大脑海马体中的某些神经元的炎症对于形成长期记忆至关重要。
根据记忆中信息储存时间的不同,我们可以把记忆分为瞬时记忆、短时记忆和长时记忆。其中,长时记忆可分为程序记忆和陈述记忆,前者是对习得行为和技能的记忆,后者是对事实信息的记忆。而陈述记忆可以进一步分为语义记忆和情境记忆,前者是对基本事实知识的记忆(例如对各种物体的名称的记忆),后者是对特定时空情景中经历过的各种事件的记忆(例如你今天早餐吃了什么)。
TLR9通路的意外激活
在这项研究中,研究团队通过给小鼠进行短暂、温和的电击,足以形成对电击事件的记忆(情境记忆),并进一步揭示这种记忆的形成机制。他们在对小鼠电击后分析了海马体中的神经元,发现一个重要的炎症信号通路——TLR9通路中的基因被强烈激活。
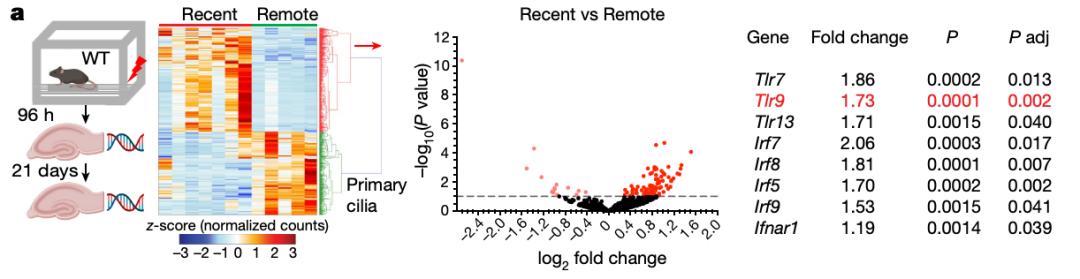
TLR9通路广为人知的是通过通过监测来自病原体的DNA片段来出发免疫反应。研究团队观察到该通路被激活后,一开始是以为小鼠被感染了,但经过仔细检查后,他们惊讶地发现,TLR9通路仅在显示出DNA损伤的海马体神经元中被激活。大脑活动通常会诱发DNA的小损伤,这些损伤在几分钟内就会得到修复。然而,在这一海马体神经元群体中,DNA损伤似乎更加严重和持久。
通过触发炎症来形成记忆
进一步的分析显示,DNA片段以及DNA损伤产生的其他分子从细胞核中释放出来,随后神经元的TLR9通路被激活,该通路反过来刺激DNA修复复合体在一个不寻常的位置形成——中心体(Centrosome)。
中心体是一种存在于大多数动物细胞的细胞质中的一种细胞器,对于协调细胞分裂至关重要。但在不分裂的神经元中,受刺激的中心体参与了DNA修复周期,似乎将单个神经元组织成记忆群体。
研究团队表示,在漫长的进化中,细胞分裂和免疫反应一直高度保守,使得生命得以继续,同时提供保护免受外来病原体的侵害,似乎在进化过程中,海马体的神经元采用了这种基于免疫的记忆机制,将免疫反应中感应DNA的TLR9通路与DNA修复的中心体的功能相结合,在不进行细胞分裂的情况下形成记忆。
抗拒无关信息的输入
在完成炎症过程所需的一周内,小鼠的记忆编码神经元被发现发生了各种变化,包括对新的或类似的环境刺激变得更加抗拒。研究团队表示,这一点值得注意,因为我们不断被信息所淹没,而编码记忆的神经元需要保存它们已经获得的信息,而不是被新的信息输入“分心”。
重要的是,该研究还发现,阻断海马体神经元中的TLR9通路不仅可以防止小鼠形成长期记忆,而且还会导致严重的基因组不稳定性。而基因组不稳定性被认为是加速衰老、癌症及精神和神经退行性疾病(例如阿尔茨海默病)的标志。这也提示了我们,维护TLR9信号通路的完整性,可能是一种有前途的神经认知缺陷的预防策略。
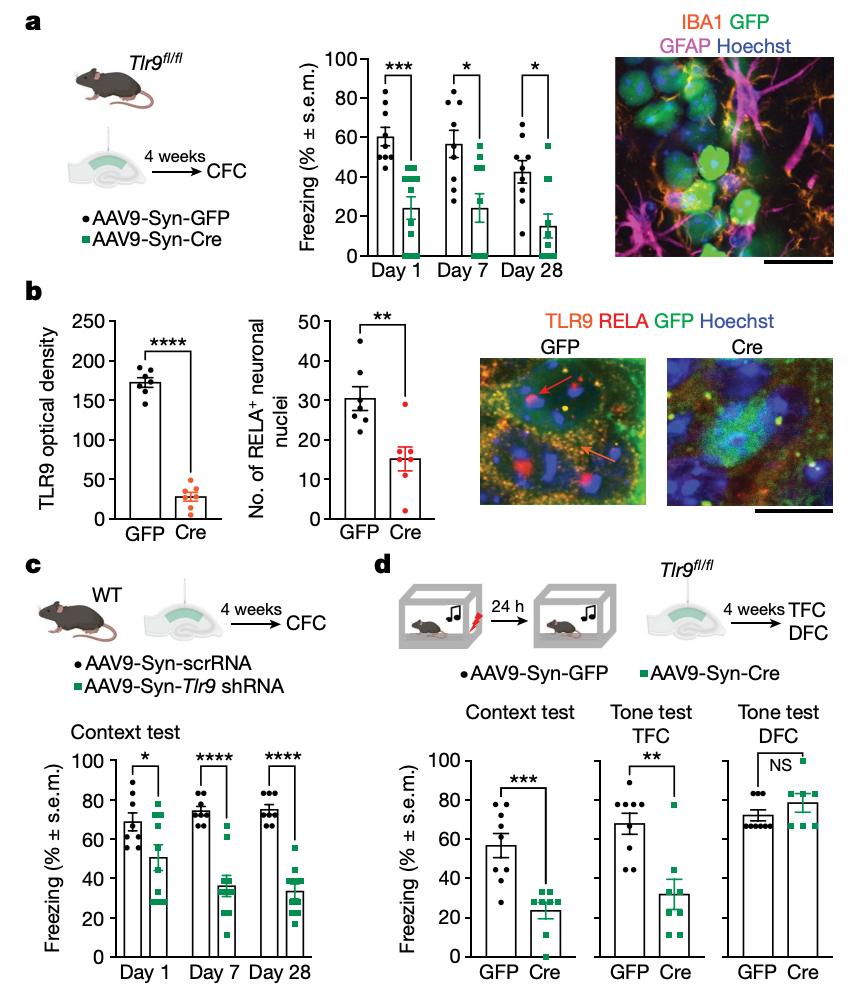
在海马体神经元中特异性敲除Tlr9基因敲除后,小鼠的情境记忆能力受损
此外,研究团队还指出,目前有研究通过药物抑制TLR9通路来缓解长期新冠(Long COVID)症状。而这项新研究提示我们,抑制TLR9通路可能会带来重大健康风险。
论文链接:
https://www.nature.com/articles/s41586-024-07220-7
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




