- +1
【前沿进展】杨硕/王曦/陈芸/ Fiachra Humphries等合作发现调控CD8+ T细胞记…
机体免疫反应核心是精准、有效和可持续的免疫应答,这对免疫系统发挥免疫防御,监视和耐受等功能至关重要1。领域内科学家几十年来一直围绕上述环节开展持续的研究,包括鉴别特异性反应抗原,了解抗原提呈的机制,解析免疫应答反应信号1(抗原识别信号),信号2(共刺激信号)和信号3(细胞因子信号)等的调控机制,以及剖析细胞应答后的细胞分化和记忆细胞形成等2-5。以上这些研究对于了解生命体免疫活动本源,开发疫苗和免疫疗法用于感染,慢性免疫炎症疾病和肿瘤的转化治疗具有重要意义。
可持续免疫反应和机体免疫力建立的核心是免疫应答后记忆细胞的分化形成,这是目前免疫学研究的前沿和热点。CD8+ T细胞是机体内主要发挥杀伤效应细胞,在机体抵御感染和癌症中发挥关键作用。以CD8+ T细胞为主要研究对象,近五年在记忆T细胞分化研究领域已取得了一系列重要发现。目前已知CD8+ T细胞在应答强抗原刺激后可分化为效应前体细胞(Short-lived effector cell,SLEC)和记忆前体细胞(Memory-precursor effector cell,MPEC)。SELC继续分化为终末效应T细胞(Effector T cell,Teff),发挥实时杀伤作用,但其寿命较短,此外部分SELC细胞也可在反应中分化为MPEC6。MPEC则继续分化为记忆T细胞(Memory T cell,Tm),包括中枢记忆和组织记忆T细胞等,具有长寿命,在病原体二次刺激时快速激活分化形成效应细胞,为机体提供免疫保护作用7。在慢性病毒感染和肿瘤中,持续的弱抗原暴露会诱导CD8+ T细胞分化为耗竭前体T细胞(Progenitor exhausted T cell,Tpex),该细胞群有与MPEC相似功能,拥有自我更新能力和接触抗原后的反应记忆性,然而持续弱抗原刺激下会导致Tpex细胞反应崩溃,最终成为耗竭终末期T细胞(Tex)6。CD8+记忆T细胞分化受多种机制的调节,包括TCR信号强度、细胞因子信号、表观调节以及转录因子调节等8,其中转录因子核心表达程序是决定细胞分化命运关键,也是目前研究CD8+记忆T细胞研究的重点及热点。目现已发现一系列转录因子可以促进CD8+ 记忆T细胞分化,包括TCF-19、BCL610、ID311和MYB12等。其中以TCF-1为中心的转录调控网络在CD8+记忆T细胞的产生中发挥关键核心作用,这为抗病毒和抗肿瘤免疫治疗提供了关键线索和靶点。尽管对TCF-1调节CD8+ T细胞分化、功能以及相关的靶基因表达和染色质表观状态等已有深入研究9, 13, 14,然而,影响TCF-1表达和活性的上游关键调控机制以及这些调控对CD8+记忆T细胞形成和功能发挥的影响仍然未知,对上述问题阐明将有助于开发新的靶向记忆T细胞调控策略用于抗病毒和抗肿瘤免疫治疗。
进化保守蛋白ECSIT分子最初被鉴定为TRAF6结合蛋白,参与Toll/IL-1信号激活和果蝇的先天免疫防御反应15。然而后续哺乳动物研究并没有发现类似作用,但发现ECSIT可定位到线粒体上,并促进线粒体ROS产生和杀菌反应,以及影响线粒体自噬等16, 17。随后研究又陆续发现ECSIT是重要组织器官发育调控蛋白,影响中胚层,心脏和肠道等组织器官发育18, 19。然而ECSIT在哺乳类免疫系统中功能,特别是适应性免疫中的作用仍然未知。
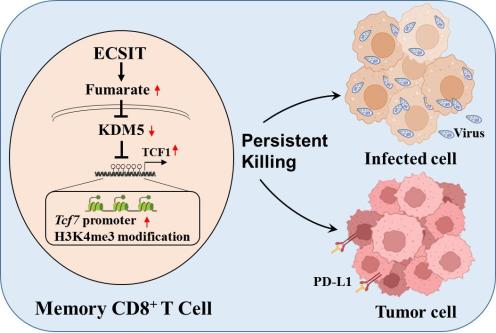
2024年2月,南京医科大学杨硕、王曦和陈芸教授以及美国马萨诸塞大学医学院Fiachra Humphries教授合作在Nature Cell Biology上发表文章“ECSIT facilitates memory CD8+ T cell development by mediating fumarate synthesis during viral infection and tumorigenesis”。该论文首次报道了ECSIT蛋白在适应免疫CD8+记忆T细胞形成中的重要作用。该研究发现ECSIT是诱导CD8+ T细胞富马酸产生关键分子,通过影响富马酸产生ECSIT可提高转录因子TCF-1启动子H3K4me3修饰和基因表达,进而影响CD8+记忆T细胞转录调节网络形成,并促进CD8+记忆T细胞发挥持续抗病毒和抗肿瘤作用。
 在该研究中,研究者首先系统分析比较了BioGPS、ImmGen、GEO等多种公开数据库,发现ECSIT是CD8+ T细胞尤其是CD8+记忆T细胞高表达蛋白。随后通过构建Ecsit-EGFP报告基因小鼠对上述结果进行确证,发现不论是稳态还是急性病毒感染或者慢性肿瘤刺激,ECSIT都高表达于CD8+记忆T细胞,提示其在CD8+记忆T细胞发育或者功能中具有重要作用。
在该研究中,研究者首先系统分析比较了BioGPS、ImmGen、GEO等多种公开数据库,发现ECSIT是CD8+ T细胞尤其是CD8+记忆T细胞高表达蛋白。随后通过构建Ecsit-EGFP报告基因小鼠对上述结果进行确证,发现不论是稳态还是急性病毒感染或者慢性肿瘤刺激,ECSIT都高表达于CD8+记忆T细胞,提示其在CD8+记忆T细胞发育或者功能中具有重要作用。研究者构建了胸腺发育后T细胞ECSIT特异性敲除小鼠(Ecsit fl/fl dLck-Cre)来观察ECSIT对发育成熟T细胞影响。通过嵌合体骨髓移植实验发现ECSIT缺失引起稳态情况下CD8+记忆T细胞的减少。随后通过抗原特异性OT-1小鼠和二次应答实验进一步证实ECSIT缺失损害记忆T细胞反应。通过构建ECSIT条件诱导型抗原特异性敲除小鼠(Ecsit fl/fl Rosa26CreERT2OT-1)在记忆T细胞形成时期破坏ECSIT表达,同时结合嵌合体T细胞移植实验,研究人员发现ECSIT缺失可直接抑制在急性病毒感染和慢性肿瘤刺激下的CD8+ 记忆T细胞发育及持续抗病毒和抗肿瘤功能的发挥。
接下来,研究人员分选出ECSIT缺失CD8+记忆T细胞,通过RNA-seq、ATAC-seq和ChIP-seq等多组学分析和体内外回补实验等,发现ECSIT缺失主要显著影响CD8+记忆T细胞核心转录因子TCF-1表达和其转录调控网络来持续影响CD8+记忆T细胞分化和功能形成。随后,根据基因组学分析提示对ECSIT缺失CD8+记忆T细胞代谢状态进行了质谱检测。研究人员发现无论在强抗原还是弱抗原刺激下,ECSIT均最显著影响CD8+记忆T细胞内富马酸产生,结合免疫荧光和电镜分析等,又进一步发现ECSIT缺失显著影响细胞器特别是线粒体状态,这可能与ECSIT缺失后细胞代谢异常相关。
随后,研究人员对ECSIT调控富马酸影响TCF-1表达机制进行了分析研究。发现TCF-1启动子在MPEC和Tm细胞中H3K4me3修饰显著增加,促进了TCF-1表达。已知富马酸是H3K4me3去甲基化酶KDM5的内源抑制剂,因此ECSIT缺失引起的富马酸减少促进了KDM5酶活性,导致转录因子TCF-1的H3K4me3修饰和转录表达下降,进而最终抑制CD8+记忆T细胞形成和抗病毒及抗肿瘤功能。
最后,研究者又系统分析比较了多个黑色素瘤病人单细胞数据库以及TCGA数据库,发现ECSIT在肿瘤病人CD8+ Tpex干性记忆细胞高表达,与众多肿瘤免疫检查点分子表达负相关,并与肿瘤病人PD-1治疗预后正相关。由于记忆和效应细胞存在部分功能拮抗,研究人员在小鼠模型上又进一步采用临床药物富马酸二甲酯(DMF)结合PD-L1抗体治疗方法,通过分别提高CD8+细胞记忆力和T细胞效应功能,发现该联合治疗可显著提高抗肿瘤免疫反应和抑制肿瘤的生长。
总结该工作,主要研究发现和意义包括:
1)首次揭示进化保守蛋白ECSIT在哺乳类适应性免疫CD8+记忆T细胞中的重要作用,并提示ECSIT在哺乳类适应性免疫系统中存在重要功能;
2)发现了一个影响CD8+记忆T细胞核心转录因子TCF-1表达和激活的重要上游调控机制;
3)进一步确定DMF联合PD-L1抗体阻断治疗的双重抗肿瘤效应,包括研究人员前期发现靶向GSDMD焦亡提高抗原提呈20,以及本研究发现促进CD8+记忆性T细胞形成,因而为肿瘤免疫新疗法开发提供了重要线索。
 综上,该工作首次确定了ECSIT蛋白在调节CD8+记忆T细胞核心转录因子TCF-1表达和转录调节功能中的重要作用,发现了一个可提高持续免疫反应力作用靶点,为临床CD8+记忆T细胞功能转化研究提供了新的线索和理论依据。
综上,该工作首次确定了ECSIT蛋白在调节CD8+记忆T细胞核心转录因子TCF-1表达和转录调节功能中的重要作用,发现了一个可提高持续免疫反应力作用靶点,为临床CD8+记忆T细胞功能转化研究提供了新的线索和理论依据。南京医科大学基础医学院已毕业博士(现工作于无锡市儿童医院检验科)杨勇兵和基础医学院博士研究生王亚男为本文的共同第一作者,南京医科大学基础医学院杨硕教授、生殖医学与子代健康全国重点实验室王曦教授、药学院陈芸教授和美国马萨诸塞大学医学院Fiachra Humphries教授为本文的共同通讯作者。
参考文献
Nicholson, L.B. The immune system. Essays in biochemistry 60, 275-301 (2016).
Speiser, D.E. et al. Unmodified self antigen triggers human CD8 T cells with stronger tumor reactivity than altered antigen. Proceedings of the National Academy of Sciences 105, 3849-3854 (2008).
Reeves, E. & James, E. Antigen processing and immune regulation in the response to tumours. Immunology 150, 16-24 (2017).
Hwang, J.-R., Byeon, Y., Kim, D. & Park, S.-G. Recent insights of T cell receptor-mediated signaling pathways for T cell activation and development. Experimental & molecular medicine 52, 750-761 (2020).
Kaech, S.M. & Cui, W. Transcriptional control of effector and memory CD8+ T cell differentiation. Nature Reviews Immunology 12, 749-761 (2012).
Zehn, D., Thimme, R., Lugli, E., de Almeida, G.P. & Oxenius, A. ‘Stem-like’precursors are the fount to sustain persistent CD8+ T cell responses. Nature Immunology 23, 836-847 (2022).
Joshi, N.S. et al. Inflammation directs memory precursor and short-lived effector CD8+ T cell fates via the graded expression of T-bet transcription factor. Immunity 27, 281-295 (2007).
Chen, Y., Zander, R., Khatun, A., Schauder, D.M. & Cui, W. Transcriptional and epigenetic regulation of effector and memory CD8 T cell differentiation. Frontiers in immunology 9, 2826 (2018).
Zhou, X. et al. Differentiation and persistence of memory CD8+ T cells depend on T cell factor 1. Immunity 33, 229-240 (2010).
Ichii, H. et al. Role for Bcl-6 in the generation and maintenance of memory CD8+ T cells. Nature immunology 3, 558-563 (2002).
Yang, C.Y. et al. The transcriptional regulators Id2 and Id3 control the formation of distinct memory CD8+ T cell subsets. Nature immunology 12, 1221-1229 (2011).
Gautam, S. et al. The transcription factor c-Myb regulates CD8+ T cell stemness and antitumor immunity. Nature immunology 20, 337-349 (2019).
Shan, Q. et al. Tcf1 preprograms the mobilization of glycolysis in central memory CD8+ T cells during recall responses. Nature immunology 23, 386-398 (2022).
Shan, Q. et al. Tcf1–CTCF cooperativity shapes genomic architecture to promote CD8+ T cell homeostasis. Nature Immunology 23, 1222-1235 (2022).
Kopp, E. et al. ECSIT is an evolutionarily conserved intermediate in the Toll/IL-1 signal transduction pathway. Genes & development 13, 2059-2071 (1999).
West, A.P. et al. TLR signalling augments macrophage bactericidal activity through mitochondrial ROS. Nature 472, 476-480 (2011).
Carneiro, F.R., Lepelley, A., Seeley, J.J., Hayden, M.S. & Ghosh, S. An essential role for ECSIT in mitochondrial complex I assembly and mitophagy in macrophages. Cell reports 22, 2654-2666 (2018).
Xiao, C. et al. Ecsit is required for Bmp signaling and mesoderm formation during mouse embryogenesis. Genes & development 17, 2933-2949 (2003).
Jiang, Y. et al. ECSIT is a critical factor for controlling intestinal homeostasis and tumorigenesis through regulating the translation of YAP protein. Advanced Science 10, 2205180 (2023).
Jiang, Y. et al. Gasdermin D restricts anti-tumor immunity during PD-L1 checkpoint blockade. Cell Reports 41 (2022).
原标题:《【前沿进展】杨硕/王曦/陈芸/ Fiachra Humphries等合作发现调控CD8+ T细胞记忆形成新机制》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




