- +1
基于环状mRNA的TCR-T细胞,治疗巨细胞病毒感染
CAR-T细胞疗法在治疗血液肿瘤方面取得了巨大成功,目前已有10种治疗B细胞肿瘤与多发性骨髓瘤的CAR-T产品获得NMPA与FDA批准上市。与CAR-T细胞类似,T细胞受体工程化T细胞(TCR-T)也是一类经工程化改造的T细胞。不同于CAR-T细胞主要识别细胞表面抗原,TCR-T细胞可以靶向细胞内部抗原,在抗病毒与抗肿瘤免疫治疗领域具有广泛的应用前景,有望成为继CAR-T细胞之后,又一类重磅工程化T细胞药物。鉴于HLA基因的多样性及TCR受体库的复杂性,筛选抗原特异性的TCR受体依然极具挑战性。
近年来,mRNA技术被成功地应用于新冠病毒疫苗的研发,今年诺贝尔医学与生理学奖也授予了发明mRNA修饰技术的两位科学家Katalin Karikó与Drew Weissman。而被称为mRNA2.0时代的环状mRNA(circRNA)技术更是引发了广泛关注,其具有生产成本低、蛋白水平表达高的优势,在免疫细胞治疗领域具有重要的应用潜力。
近日,上海交通大学医学院附属第一人民医院/上海市第一人民医院张岩与宋献民研究团队联合苏州科锐迈德生物医药科技公司左炽健团队,在 Molecular Therapy 期刊发表了题为:Circular mRNA-based TCR-T offers a safe and effective therapeutic strategy for treatment of cytomegalovirus infection 的研究论文。
该研究首次报道了基于环状mRNA技术的TCR-T细胞疗法,为临床上造血干细胞移植后人巨细胞病毒(CMV)感染提供新的、更为安全有效的免疫治疗策略。
如何有效扩增抗原特异性T淋巴细胞并获得抗原特异性TCR序列,是研发TCR-T细胞的关键。苏州科锐迈德生物医药科技公司之前的研究表明,环状mRNA (circular mRNA, cmRNA)能够显著延长外源基因在细胞中的表达时长。本项研究中,研究团队首先利用环状mRNA技术,在单核细胞分化的树突状细胞(moDCs)中表达CMV-pp65抗原,检测是否能够提供更为持久的抗原刺激信号,促进抗原特异性T淋巴细胞的活化和增殖。研究结果表明:与线性mRNA相比,转染了编码CMV-pp65 抗原的环状RNA的moDCs细胞,能更加持久地提供抗原信号,更加高效地激活和扩增CMV-pp65特异性T细胞,表明基于环状mRNA技术的抗原递呈新策略,能够显著提高TCR的筛选效率,在开发抗原特异性T细胞(尤其是含量较低的抗原特异性T细胞)方面具有巨大优势。
此外,之前有文献报道线状mRNA编码的TCR基因只能在原代T细胞中表达48-72小时。研究团队进而对环状mRNA编码的外源TCR基因在原代T淋巴细胞中的表达时长进行了测试,发现环状mRNA技术能够显著提升TCR基因在人原代T淋巴细胞中的表达时长。在电转后7天与11天,依然分别有约80%与50%的T细胞表达外源TCR受体。研究团队进一步对基于环状mRNA技术的cm-pp65-TCR-T细胞在小鼠体内的杀伤功能进行了测试,体内实验结果表明,两周输注一次cm-pp65-TCR-T细胞,即可有效清除表达CMV-pp65抗原的靶细胞。
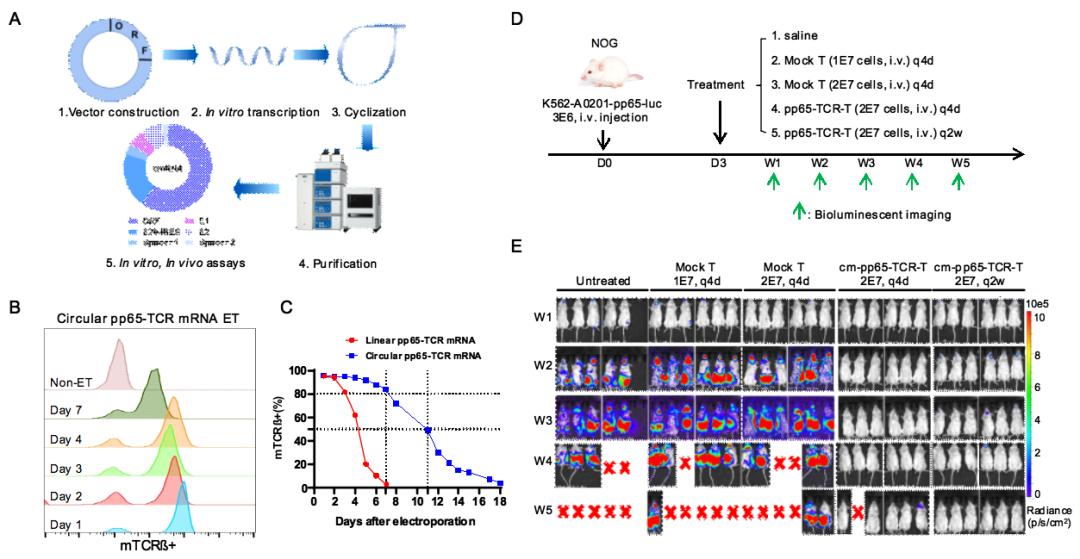
图1. cm-pp65-TCR-T靶向清除表达CMV抗原的靶细胞
数据显示,我国人群CMV病毒感染率超过95%,多数呈现潜伏感染状态。然而,临床上接受造血干细胞移植术的患者,由于经过术前清髓预处理,呈现暂时的T细胞免疫缺陷,因而患者在移植后2-3个月CMV病毒易发生再激活,发生CMV血症甚至CMV肺炎。尽管来特莫韦等抗病毒药物显著降低了造血干细胞移植后患者CMV的再激活,但对于部分患者而言CMV病毒再激活依然可能会危及患者生命。
该研究将为这部分患者提供新的治疗手段,因而具有重要的临床研究意义。多数造血干细胞移植患者在术后数月后,体内会重建针对CMV病毒的T细胞免疫。基于环状mRNA技术的TCR-T细胞,由于TCR基因不会整合到基因组,没有潜在的致瘤风险,因而具有良好的安全性。此外,如果采用造血干细胞移植供者来源的T淋巴细胞制备cm-pp65-TCR-T细胞,回输患者后不仅可以治疗CMV病毒感染,而且能够增强“移植物抗肿瘤效应”(GVL),促进供者造血干细胞的植入。目前,市一医院血液科即将在本项研究基础上,开展研究者发起的临床研究(IIT)。
综上所述,该研究是首次将环状mRNA技术应用于TCR-T细胞的研发与制备,不仅为造血干细胞移植后CMV感染的免疫治疗提供新的策略,也为其它抗病毒或抗肿瘤TCR-T疗法提供新的思路。
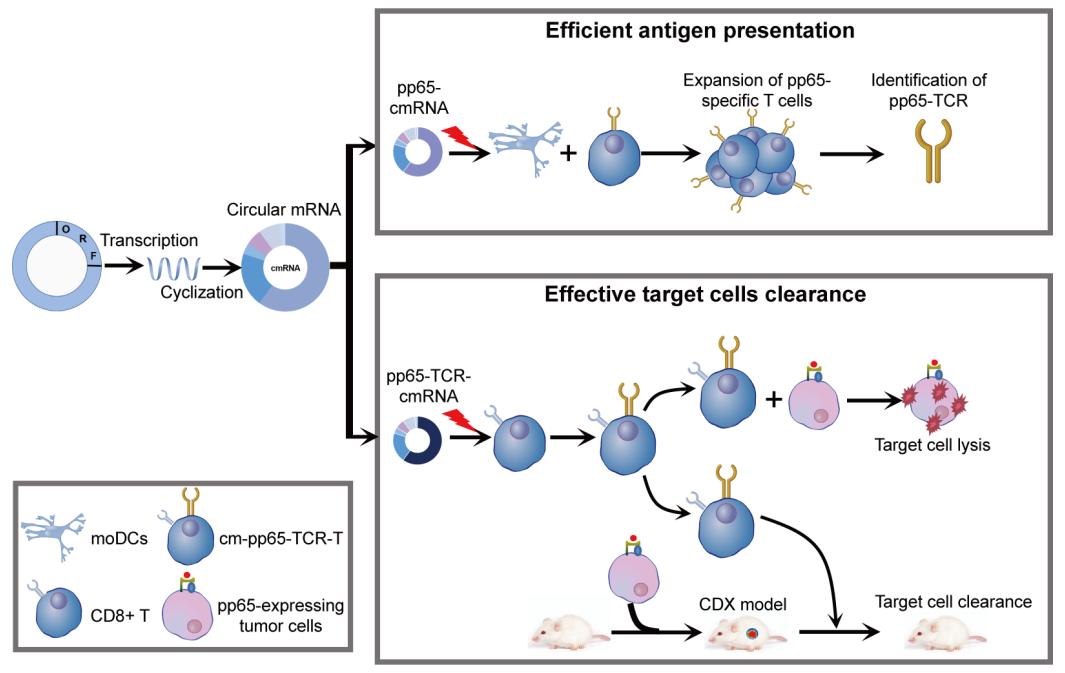
图2. 基于环状mRNA技术的TCR-T免疫疗法示意图
上海市第一人民医院血液科博士研究生沈良华与苏州科锐迈德生物医药科技公司杨嘉丽博士为文章的共同第一作者。该研究使用的环状mRNA由苏州科锐迈德生物医药科技公司制备,上海快序生物科技有限公司为本项研究提供抗原多肽质谱分析。
上海交通大学医学院附属第一人民医院/上海市第一人民医院血液科张岩/宋献民团队长期从事于血液恶性肿瘤发病机制与免疫细胞治疗的基础、转化与临床研究,近年来承担多项科技部、基金委、上海市科研项目。目前,研究团队已经建立了成熟的TCR-T细胞研发技术平台,成功开发了多种靶向CMV、EBV等病毒,以及TP53突变、KRAS突变等“肿瘤新生抗原”(Neoantigen)的TCR-T细胞,并申请了多项中国发明专利与PCT专利。本研究团队长期招聘博士后、科研助理和技术员,热诚欢迎有志于免疫细胞治疗研究方向的医学或生物学背景的人才加入。
论文链接:
https://doi.org/10.1016/j.ymthe.2023.11.017

本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




