- +1
Life Med | 徐君/邓宏魁/韩春生筛选人激酶组基因发现ErbB通路调控人原始态多能性和全能性

如何调控干细胞的发育潜能是干细胞再生医学领域的重要科学问题之一。在人类着床前胚胎发育的过程中,胚胎的发育潜能受到动态调控并发生变化,这是个体发育的基础。从人受精卵到8细胞卵裂球时期的胚胎细胞具有全能性(Totipotency),能够发育成包括胚胎、胎盘和卵黄囊在内的完整个体。随着发育进程的推进,人胚胎细胞丧失了全能性的分子特征,发育潜能逐渐受限。然而,在这一过程中形成的人着床前囊胚上胚层细胞仍然具有向胚内与胚外谱系分化的潜能,由其建立的人原始态多能干细胞(Naïve pluripotent stem cells)也具备了形成胚内、胚外谱系的能力。当前,对于人全能性调控机制的了解仍然不多,特别是对调控人全能性的信号通路知之甚少。另一方面,与小鼠原始态多能性调控机制的研究相比,对于人原始态多能性调控机制的了解仍然相当有限。要想系统性地研究这些问题,需要合适的模型和策略。
人潜能扩展多能干细胞(Human extended pluripotent stem cells)是2017年由北京大学干细胞研究中心邓宏魁团队建立的一类具备胚内、胚外发育潜能的新型多能干细胞。团队随后的研究揭示人潜能扩展多能干细胞是一类处于原始态多能性(Naïve pluripotency)与始发态多能性(Primed pluripotency)之间的中间态细胞,具备了部分的原始态多能性分子特征,不具备全能性的整体分子特征。因此,通过遗传筛选分析人潜能扩展多能干细胞与人原始态多能干细胞的调控差异,有助于揭示人原始态多能性调控的核心机制。此外,以人潜能扩展多能干细胞为起点开展的遗传筛选,也有助于发现调控人全能性的新因子、新通路。

2023年10月23日,北京大学基础医学院徐君课题组、邓宏魁课题组与中科院动物研究所韩春生课题组合作在Life Medicine杂志在线发表了题为A CRISPR/Cas9-based kinome screen identifies ErbB signaling as a new regulator of human naïve pluripotency and totipotency的研究论文,基于人潜能扩展多能干细胞转化为人原始态多能干细胞的体系,利用CRISPR/Cas9技术开展了全激酶组敲除筛选,系统鉴定分析了调节人原始态多能性的信号通路,并在随后的化学小分子筛选验证中发现抑制ErbB信号通路会促进体外人原始态多能性和全能性的诱导。
研究人员首先在人潜能扩展多能干细胞上建立了一套可诱导的CAS9表达系统,随后在细胞中转入携带全激酶组sgRNA载体的慢病毒库,通过Dox诱导CAS9表达,在人潜能扩展多能干细胞中构建起了全激酶组敲除的文库。随后,研究人员采用了两种策略来分析鉴定影响人原始态多能性调控的激酶:1)通过将此文库细胞切换到目前已报道的人原始态多能干细胞培养条件PXGL与5i/LA下进行持续传代培养筛选,收集富集存活细胞;2)通过人原始态多能干细胞特异表达的表面分子标记SUSD2直接富集在人潜能扩展多能干细胞培养基中出现的人原始态多能性细胞群。通过分别分析以上两种策略收集的细胞群中富集的sgRNA序列,研究人员在整合信息后得到了对于人原始态多能性诱导和维持调控发挥作用的潜在激酶列表。
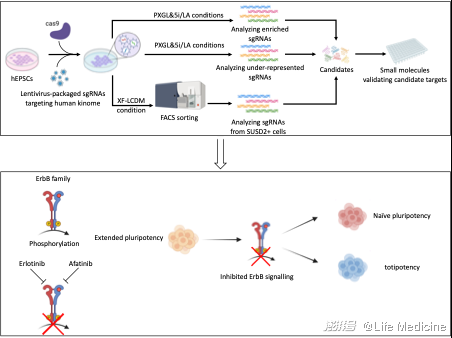
在此基础上,研究人员整理了针对这些激酶的小分子抑制剂,并构建了可以指示由人潜能扩展多能干细胞向人原始态多能干细胞转变的KLF17基因报告体系。通过在人潜能扩展多能干细胞中筛选针对以上激酶的化学小分子,研究人员发现ErbB信号通路的抑制剂阿法替尼(Afatinib)在PXGL条件下可以进一步显著激活KLF17阳性细胞的比例。通过流式分析以及qPCR分析,研究人员进一步验证了ErbB信号通路的抑制可以促进人原始态多能性分子特征的诱导。由于KLF17同时也在人全能性细胞中富集表达,研究人员进一步尝试抑制ErbB通路是否对于人全能性诱导具有调控作用。利用具有人全能性基因TPRX1报告体系的人胚胎干细胞系,研究人员发现ErbB信号通路的抑制能够在人全能性细胞诱导条件e4CL下进一步提升TPRX1阳性细胞的比例和强度。此外,在此条件下诱导的人全能性细胞中的多个典型人全能性分子标记表达水平得到了明显提升。
研究人员进一步在不同的人多能干细胞培养条件下(始发态多能干细胞、潜能扩展多能干细胞以及原始态多能干细胞)研究ErbB信号通路抑制剂阿法替尼与厄洛替尼(Erlotinib)对细胞转录组的影响。分析表明ErbB通路的抑制在不同人多能干细胞培养条件下均促进诱导了人全能性分子标记的表达提升。通过进一步的生信分析,研究人员发现ErbB信号通路与人全能性8细胞胚胎以及体外诱导的人8细胞样干细胞的调控网络存在关联,其中KLF5与TFAP2C是关联节点。为了研究KLF5、TFAP2C对ErbB信号通路是否有调控作用,研究人员在人潜能扩展多能干细胞中分别瞬时过表达了这两个基因,发现瞬时过表达KLF5与TFAP2C上调了ErbB家族的EGFR与ERBB2的基因表达。同时,研究人员发现KLF5的小分子抑制剂SR18662不仅下调了ERBB2与ERBB3的表达,还上调了全能性分子标记的表达。这些结果表明ErbB信号通路可能在人早期胚胎发育过程中起到了调控作用,并与人全能性的分子调控网络存在相互调控的关系。
总的来说,这项研究揭示了参与人原始态多能性调控的新激酶和相关信号通路。该研究中获得的筛选数据集为未来研究调控人原始态多能性和全能性的信号通路和调节因子提供了参考资源。此外,这项研究还发现了ErbB信号通路的抑制可以促进体外人全能性细胞的诱导。这些发现有助于加深对于人原始态多能性和全能性调控机制的理解,并为未来优化人原始态多能性干细胞和全能性干细胞的体外培养条件提供了新线索。
北京大学干细胞研究中心徐君研究员、邓宏魁教授以及中国科学院动物研究所韩春生研究员为本文的共同通讯作者,北京大学基础医学院博士生李佳宇为本文的第一作者。该研究得到了科技部国家重点研发计划的经费支持。
英文全文链接:
https://doi.org/10.1093/lifemedi/lnad037
引用本文:
Jiayu Li, Xiwen Lin, Liangfu Xie, Jingru Zhao, Chunsheng Han, Hongkui Deng, Jun Xu, A CRISPR/Cas9-based kinome screen identifies ErbB signaling as a new regulator of human naïve pluripotency and totipotency, Life Medicine, 2023;, lnad037, https://doi.org/10.1093/lifemedi/lnad037
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




