- +1
李超忠/朱林课题组 & 薛小松课题组:Arbuzov反应研究取得突破性进展
以下文章来源于CCSChemistry ,作者CCS Chemistry
CCSChemistry.
CCS Chemistry是由中国化学会创办的高水平旗舰新刊,面向全球科学家,收录化学各领域高质量原创科技论文。关注CCS Chemistry,即时获取期刊相关资讯。
 近日,中国科学技术大学/中国科学院上海有机化学研究所李超忠/朱林课题组与中国科学院上海有机化学研究所薛小松课题组合作,发展了新型自由基膦酰化试剂——亚磷酸(9-芴醇)(邻苯二酚)酯和亚磷酸(二苯甲醇)(邻苯二酚)酯,在室温和光氧化还原条件下实现了烷基溴化物或碘化物的脱卤自由基膦酰化。该反应是一种新颖的自由基型Arbuzov反应,反应条件温和,具有优异的官能团耐受性,可实现复杂分子的后期修饰以及含膦酸酯天然产物和药物分子的快速合成。
近日,中国科学技术大学/中国科学院上海有机化学研究所李超忠/朱林课题组与中国科学院上海有机化学研究所薛小松课题组合作,发展了新型自由基膦酰化试剂——亚磷酸(9-芴醇)(邻苯二酚)酯和亚磷酸(二苯甲醇)(邻苯二酚)酯,在室温和光氧化还原条件下实现了烷基溴化物或碘化物的脱卤自由基膦酰化。该反应是一种新颖的自由基型Arbuzov反应,反应条件温和,具有优异的官能团耐受性,可实现复杂分子的后期修饰以及含膦酸酯天然产物和药物分子的快速合成。
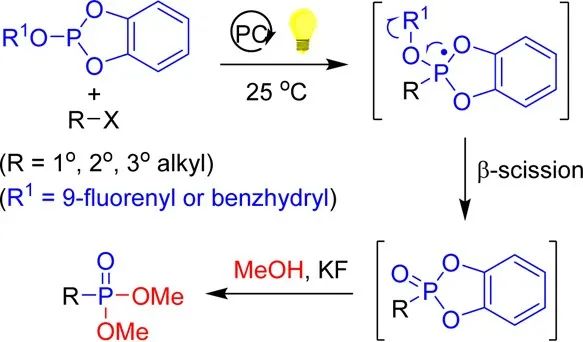 背景介绍:
背景介绍:磷是生命体中最基本的元素之一,在自然界中普遍存在。其中,含C(sp3)–P键的膦酸酯类化合物可以看作相应磷酸酯的电子等排体,由于C–P键化学性质稳定,而O–P 键易水解,因此膦酸酯类化合物在生物化学、生态学、医学、农业和材料科学等领域有着广泛的用途。
卤代烷烃与亚磷酸三酯之间的亲核取代反应,即著名的Arbuzov反应(也称为Michaelis–Arbuzov反应),是构建C(sp3)–P键的最重要方法之一。自二十世纪初发现以来,该反应已有100多年的历史,至今仍被广泛应用于有机膦酸酯类化合物的工业合成中。然而该反应存在以下一些局限性:(a) 反应温度较高 (> 150 ℃);(b) 大多数二级卤代烷和三级卤代烷不发生反应或只生成烯烃副产物;(c) 该反应与许多官能团不兼容,如酮或硝基等;(d) 反应中新生成的卤代烷与底物卤代烷存在竞争反应,导致亚磷酸三酯异构化副反应的发生。迄今为止,Arbuzov反应的改进仍然是一个艰巨的挑战。
本文亮点:
针对上述挑战,中国科技大学/中国科学院上海有机化学研究所李超忠/朱林课题组与中国科学院上海有机化学研究所薛小松课题组合作,发展了新型自由基膦酰化试剂:亚磷酸(9-芴醇)(邻苯二酚)酯和亚磷酸(二苯甲醇)(邻苯二酚)酯,在光氧化还原条件下实现了各种烷基溴化物或碘化物的脱卤自由基膦酰化。
作者以4-苯氧基溴丁烷 (Br-1) 为底物,对膦酰化试剂进行了筛选,确定了亚磷酸(9-芴醇)(邻苯二酚)酯 (P-3) 和亚磷酸(二苯甲醇)(邻苯二酚)酯 (P-4) 是较理想的自由基膦酰化试剂(图1)。膦酰化反应之后加入甲醇(或乙醇)淬灭,在KF和催化量的18-冠-6作用下进行酯交换,则得稳定的烷基膦酸二甲酯(或二乙酯)产物。经过大量条件筛选确定了最优反应条件:(1) 对溴化物的反应而言,以P-4为膦酰化试剂,1,2,3,5-四(二苯胺基)-4,6-二氰基苯 (4DPAIPN) 为光催化剂,二异丙基乙基胺 (DIPEA) 为还原剂,N,N-二甲基乙酰胺 (DMA) 为溶剂,室温下蓝光照射反应24小时,再通过后续酯交换得到烷基膦酸酯;(2) 对碘化物的反应而言,则以P-3为膦酰化试剂,fac-Ir(ppy)3为光敏剂,Zn(OAc)2和TMSCl为添加剂,DMA为溶剂,室温下蓝光照射反应24小时,再通过后续酯交换得到烷基膦酸酯。
 图1. 磷源的筛选及条件优化
图1. 磷源的筛选及条件优化在最优反应条件下,作者对底物普适性进行了考察(图2和图3)。该反应适用于一级、二级甚至三级烷基卤化物,并表现出优异的官能团耐受性,能够兼容烯烃、炔烃、酮、羧酸、酯、酰胺、磺酰胺、腈、氟、氯、噻吩、醚等官能团。同时,该方法可以放大至克级规模,也适用于对复杂天然产物分子的后期修饰。
 图2. 一级底物拓展
图2. 一级底物拓展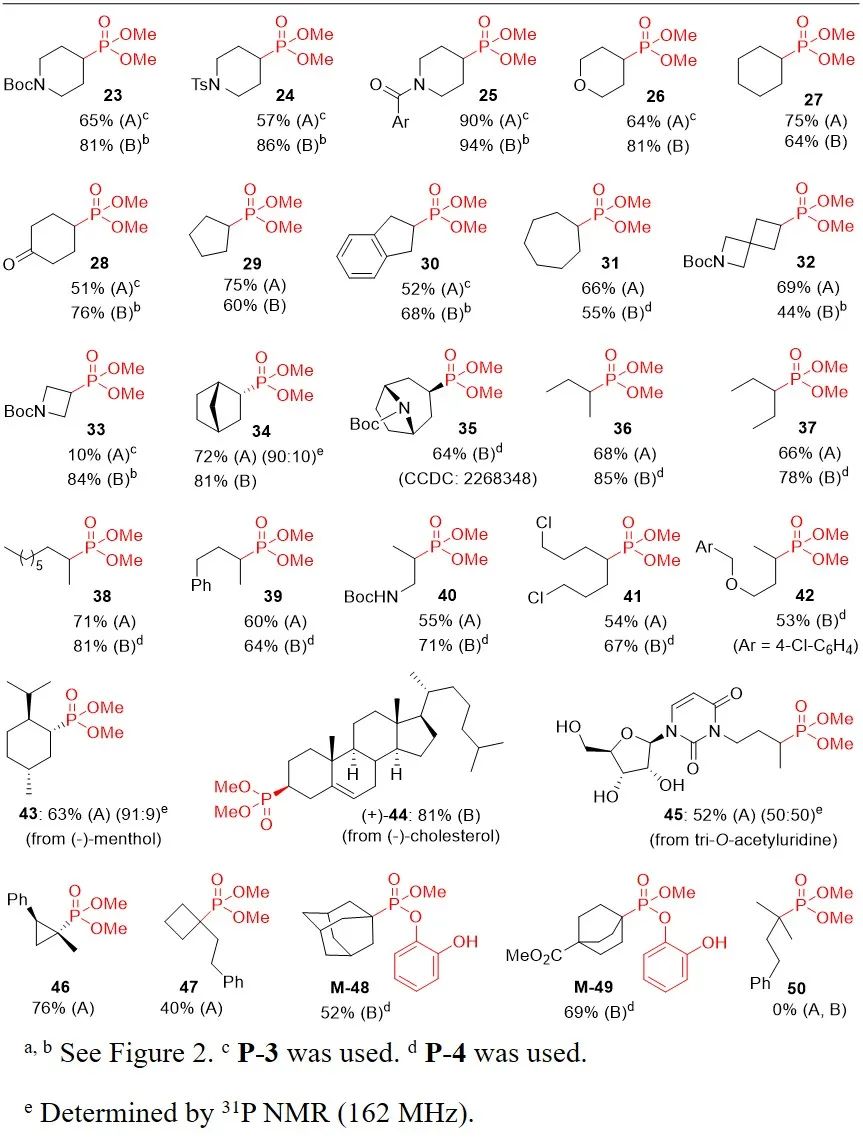 图3. 二级和三级底物拓展
图3. 二级和三级底物拓展为了进一步证明该膦酰化方法的实用性,作者开展了药物分子Fosarilate、Phosphonoalanine以及天然产物Valinophos的合成(图4)。可以看出,该膦酰化方法的应用大大缩短了反应步骤,大幅提高了总收率。
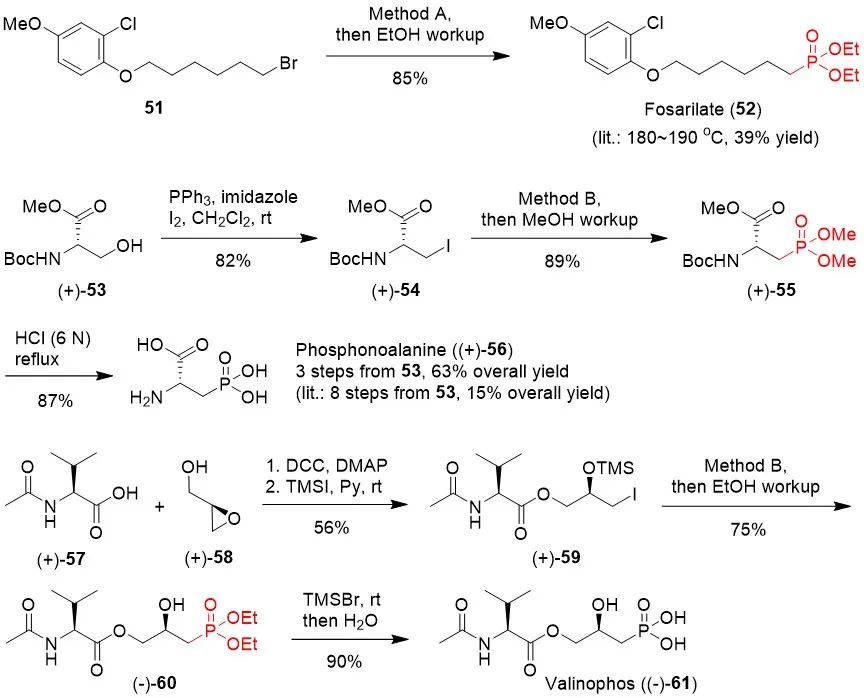 图4. 药物分子或天然产物的合成
图4. 药物分子或天然产物的合成综合机理实验结果和相关文献报道,作者提出了以下可能的反应机理(图5):(a) 在脱溴膦酰化反应中,光敏剂4DPAIPN在蓝光灯照射下激发为三线态的光敏剂[4DPAIPN]*,进而被DIPEA还原淬灭产生还原态的光敏剂,还原态的光敏剂被蓝光再次激发,然后与溴化物发生单电子转移从而回到基态的光敏剂。产生的烷基自由基进攻P-3中的磷原子,接着发生β裂解产生烷基膦酰酯中间体和二苯甲基自由基,烷基膦酰酯中间体经过后续酯交换得到最终产物烷基膦酰二甲酯,而二苯甲基自由基则从DIPEA自由基正离子处攫氢生成二苯甲烷。(b) 在脱碘膦酰反应中,[Ir]光敏剂在蓝光灯照射下激发为三线态的光敏剂[Ir]*,然后被碘化物氧化淬灭产生氧化态的光敏剂。产生的烷基自由基进攻P-3中的磷原子,接着发生β裂解产生烷基膦酰酯中间体和二苯甲基自由基,烷基膦酰酯中间体经过后续酯交换得到最终产物烷基膦酰二甲酯,氧化态的光敏剂将二苯甲基自由基氧化为二苯甲基碳正离子从而回到基态的光敏剂,完成催化循环。体系中的二苯甲基碳正离子被醋酸根捕获生成醋酸二苯甲酯。
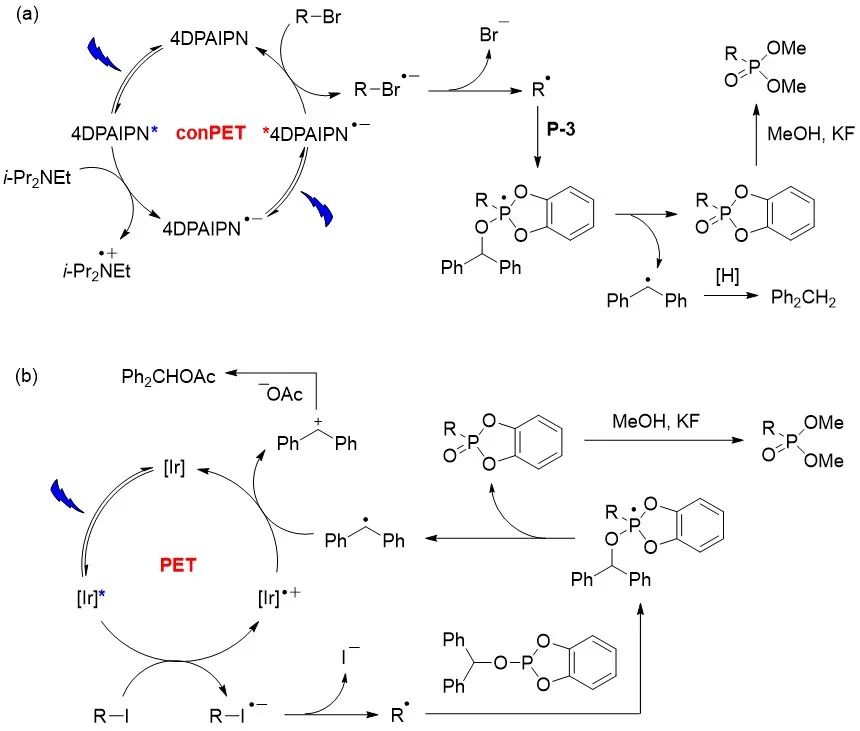 图5. 反应可能的机理
图5. 反应可能的机理为了更好地理解自由基膦酰化,中国科学院上海有机化学研究所薛小松研究员课题组对该反应进行了密度泛函理论(DFT)计算研究(图6),计算结果表明9-芴基(或二苯甲基)的引入不仅降低了β-断裂的能垒,而且有助于稳定膦自由基中间体。
需要指出的是,上世纪七十年代前后Bentrude等人对烷基自由基与亚磷酸三酯的反应进行了研究,并得出仲碳及叔碳自由基不能加成到亚磷酸三酯上的结论,该结论在过去的半个世纪中并未得到质疑。然而,上述自由基Arbuzov反应推翻了这一结论,清晰地表明伯碳、仲碳及叔碳自由基均可顺利地进攻亚磷酸三酯中的磷原子,且利用该机制可高效构建C(sp3)–P键。
 图6. 反应机理的计算研究。
图6. 反应机理的计算研究。总结与展望:
综上所述,本文作者以亚磷酸(9-芴醇)(邻苯二酚)酯和亚磷酸(二苯甲醇)(邻苯二酚)酯作为自由基膦酰化试剂,在可见光的诱导下实现了各种烷基溴化物和碘化物的脱卤自由基膦酰化。该反应可以在温和的条件下进行,适用于一级、二级甚至三级烷基卤化物,并表现出优异的官能团耐受性,从而能够实现复杂分子的后期修饰以及含膦酸酯天然产物和药物分子的快速合成。该反应是一种新颖的自由基型Arbuzov反应,解决了传统的离子型Arbuzov反应存在的大部分问题。与此同时,这一研究结果也推翻了之前认为仲碳及叔碳自由基不能与亚磷酸三酯反应的错误认知。
该工作以Research Article的形式发表在CCS Chemistry,文章的通讯作者为朱林副研究员、薛小松研究员和李超忠研究员,中国科学技术大学博士生柴林香和中国科学院上海有机化学研究所博士生王健为本论文的共同第一作者。该研究工作得到了国家自然科学基金委员会、中国科学院、中国科学院青年创新促进会以及上海市科学技术委员会的大力支持。
文章详情:
Radical Arbuzov Reaction
Linxiang Chai, Jian Wang, Jimin Yang, Junyue Yin, Zhuyong Zhang, Yulu Cheng, Lin Zhu*, Xiao-Song Xue* and Chaozhong Li*
Cite this by DOI:
10.31635/ccschem.023.202303282
文章链接
https://doi.org/10.31635/ccschem.023.202303282
扫码在线阅读
扫描或长按左侧二维码,
在线阅读全文
 中国化学会
中国化学会Chemsoc
原标题:《李超忠/朱林课题组 & 薛小松课题组:Arbuzov反应研究取得突破性进展》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




