- +1
Nature:历时六年,突破不可成药靶点,CRISPR筛选发现的抗癌新靶点进入临床试验
原创 生物世界 生物世界 收录于合集#癌症研究 435 个 #CRISPR&基因编辑 151 个
撰文丨王聪
编辑丨王多鱼
排版丨水成文
以PD-1/PD-L1、CTLA-4等分子为代表的免疫检查点阻断(ICB)疗法是近年来在肿瘤治疗领域中的革命性进展,彻底改变了癌症治疗格局。然而,该疗法在不同肿瘤病人当中的效果差异很大,大多数癌症患者无应答,长期获益比例更低。因此,需要开发新的疗法来克服耐药性问题。
酪氨酸磷酸酶PTPN2和PTPN1是炎症的中枢调节因子,2017年在 Nature 发表的研究显示,它们的缺失可以促进抗肿瘤免疫,可作为肿瘤免疫治疗新靶点。然而,磷酸酶是一类“不可成药靶点”,开发靶向它们的药物非常具有挑战性。
2023年10月4日,艾伯维公司、Broad研究所和Calico Life Sciences公司的研究人员合作,在 Nature 期刊发表了题为:The PTPN2/PTPN1 inhibitor ABBV-CLS-484 unleashes potent anti-tumour immunity 的研究论文。
该研究表明,ABBV-CLS-484是一款潜在的first-in-class、口服的PTPN2/PTPN1磷酸酶双重抑制剂,可增强抗肿瘤免疫,抑制肿瘤生长。研究数据支持ABBV-CLS-484作为一种有前景的癌症免疫治疗新策略的进一步开发。
目前,ABBV-CLS-484已开始治疗实体瘤的1期临床试验,这也是首个作为癌症治疗药物进入临床试验的活性位点磷酸酶抑制剂。
 早在2017年,Robert Manguso 等人就在 Nature 期刊发表论文【2】,通过体内CRISPR筛选,发现PTPN2及其密切相关的PTPN1可作为癌症免疫治疗的新靶点,敲除PTPN2,能够通过增强干扰素γ(INF-γ)介导的抗原呈递和生长抑制作用,提高肿瘤免疫治疗效果。
早在2017年,Robert Manguso 等人就在 Nature 期刊发表论文【2】,通过体内CRISPR筛选,发现PTPN2及其密切相关的PTPN1可作为癌症免疫治疗的新靶点,敲除PTPN2,能够通过增强干扰素γ(INF-γ)介导的抗原呈递和生长抑制作用,提高肿瘤免疫治疗效果。 然而,挑战性在于,他们发现的是一个传统意义上的“不可成药靶点”。而在这项新研究中,艾伯维的研究人员克服了这一挑战,通过基于结构的药物设计和药物样性质的优化,发现了PTPN2/PTPN1双重抑制剂——ABBV-CLS-484。艾伯维、Broad研究所和Calico的研究人员进一步揭示了ABBV-CLS-484的生物学和作用机制。
然而,挑战性在于,他们发现的是一个传统意义上的“不可成药靶点”。而在这项新研究中,艾伯维的研究人员克服了这一挑战,通过基于结构的药物设计和药物样性质的优化,发现了PTPN2/PTPN1双重抑制剂——ABBV-CLS-484。艾伯维、Broad研究所和Calico的研究人员进一步揭示了ABBV-CLS-484的生物学和作用机制。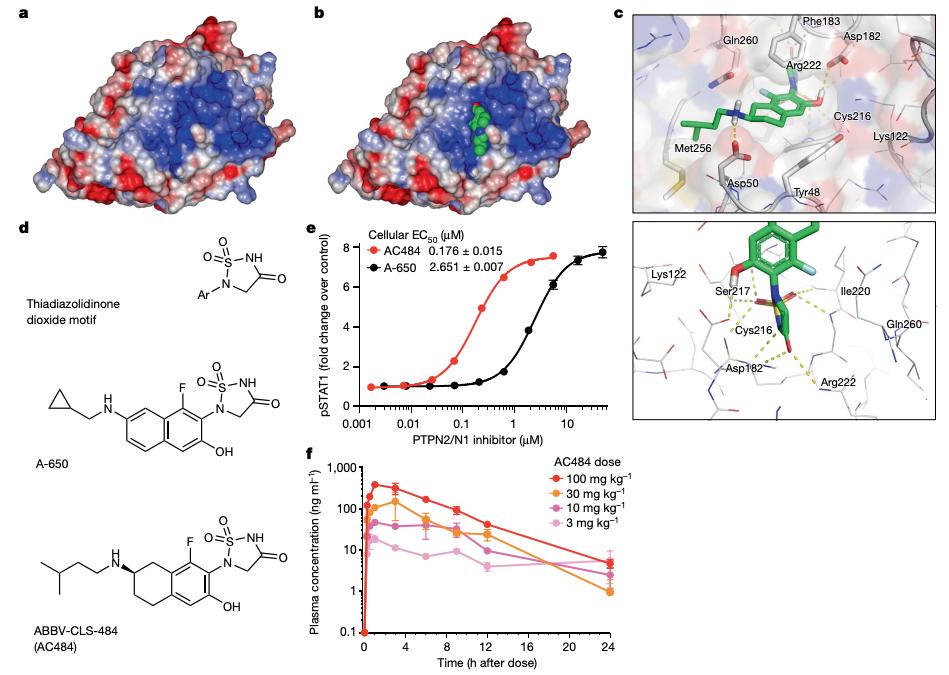 临床前研究结果表明,ABBV-CLS-484治疗放大了肿瘤对干扰素的固有反应,并增加了几种免疫细胞亚群的激活和功能,在小鼠模型中促进了包括JAK-STAT信号在内的细胞通路。
临床前研究结果表明,ABBV-CLS-484治疗放大了肿瘤对干扰素的固有反应,并增加了几种免疫细胞亚群的激活和功能,在小鼠模型中促进了包括JAK-STAT信号在内的细胞通路。在对抗PD-1单抗耐药的小鼠肿瘤模型中,单药ABBV-CLS-484治疗产生强大的抗肿瘤免疫效果。通过在体内研究和从ABBV-CLS-484治疗小鼠的肿瘤浸润淋巴细胞的单细胞转录组分析,研究团队发现,ABBV-CLS-484使肿瘤微环境发炎,并促进NK细胞和CD8+T细胞功能。在T细胞中,ABBV-CLS-484诱导表观遗传和代谢变化,导致一种独特的功能状态,增加T细胞毒性作用,减少T细胞耗竭和功能障碍。
该论文的第一作者、艾伯维公司高级首席研究科学家 Christina Baumgartner 博士表示,像PD-1阻断疗法这样的免疫疗法已经彻底改变了癌症治疗,但许多癌症患者对它们的反应并不好。通过艾伯维药物化学团队的非凡努力,我们现在有了潜在的first in class 的PTPN2/PTPN1抑制剂。我们很高兴能分享它的生物学和作用机制,并期待在临床中进行进一步评估。
该论文的合作者、Calico公司肿瘤新靶点开发负责人 Marcia Paddock 表示,这项研究有力地证明了通过合作汇集各种专业知识,以推进我们对疾病生物学的理解,并导致支持癌症患者新治疗策略的发现,我们很自豪能与艾伯维和Broad研究所合作,并期待分享我们对这种新型免疫疗法的临床研究的进一步进展。
ABBV-CLS-484是首个作为癌症治疗药物进入临床试验的活性位点磷酸酶抑制剂,目前正在艾伯维和Calico主导的实体瘤治疗的1期临床试验中(NCT04777994)。
论文通讯作者 Robert Manguso 教授表示,这是一个前所未有的机会来评估免疫反应是如何起作用的,在临床研究中进一步探索这种信号通路的能力非常重要。
论文链接:
1. https://www.nature.com/articles/s41586-023-06575-7
2. https://www.nature.com/articles/nature23270
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




