- +1
阿尔茨海默病再迎新药?礼来公布三期完整结果,美国上市申请预计年底出结果

礼来制药。人民视觉 资料图
卫材/渤健宣布其阿尔茨海默药仑卡奈单抗在美国转为完全批准不到半个月,礼来宣布其阿尔茨海默病药物一项三期临床研究的最新完整结果。
当地时间7月17日,全球制药巨头礼来在官网宣布,三期临床试验TRAILBLAZER-ALZ2的最新完整结果显示,公司研发的阿尔茨海默药物donanemab可显著减缓早期阿尔茨海默病(AD)患者认知和功能的下降。这些数据作为专题研讨会在2023年阿尔茨海默病协会国际会议 (AAIC) 上发布,并同时发表于《美国医学会杂志》(JAMA) 。
完整的研究数据显示,无论疾病的基线临床或病理阶段如何,与安慰剂相比,donanemab治疗都能带来认知和功能益处,其中该药对处于疾病早期阶段以及75岁以下的患者具有更大的益处。
具体来看,在患有轻度认知障碍的参与者(n=214)中,donanemab在iADRS(阿尔茨海默病综合评分量表)上使衰退减慢了60%,CDR-SB减慢了46%;对于阿尔茨海默病源性轻度痴呆患者(n=534),donanemab对iADRS和CDR-SB的下降分别延缓了30%和38%;在75岁以下的参与者(n=542)中,donanemab使iADRS组的下降速度减缓了48%,CDR-SB(临床痴呆评定量表)的下降速度减缓了45%;在75岁或以上的受试者(n=551)中,donanemab使iADRS的下降减缓了25%,CDR-SB的下降减缓了29%。
礼来表示,TRAILBLAZER-ALZ 2临床研究结果将有力支持公司向监管部门申请批准donanemab治疗淀粉样蛋白阳性早期症状性阿尔茨海默病(轻度认知障碍或轻度痴呆)患者,无论其tau基线水平如何。公司上季度已完成向美国食品药品监督管理局(FDA)递交上市申请,预计将在今年年底得到反馈。此外,礼来目前正在向全球其他监管机构提交申请,大部分将在年底前完成。
当地时间7月6日,FDA官网发布消息称,卫材/渤健联合开发的仑卡奈单抗用于治疗AD的加速批准已成功转为完全批准,该药是20年来首个获得FDA完全批准的阿尔茨海默病药物。如果礼来的新药能顺利获批,将成为AD治疗的另一个重磅产品。
与卫材/渤健的仑卡奈单抗一样,礼来的donanemab同样属于抗β淀粉样蛋白(amyloid-β,Aβ)药物。两个多月前,也就是今年5月初,礼来就曾公布上述三期临床试验取得积极结果。当时公布的数据显示,在tau中低水平的参与者(n=1182)中,donanemab显著减缓iADRS下降35%,CDR-SB下降36%。在所有淀粉样蛋白阳性的早期症状性AD研究参与者(n=1736)中,donanemab治疗显著减缓了iADRS下降22%,CDR-SB下降29%。
根据最新的研究结果报告,在整个试验过程中,donanemab的总体治疗效果持续增长,与安慰剂相比,差异最大的情况出现在18个月时。在所有参与者中,该药在18个月时淀粉样斑块平均减少了84%,而安慰剂组减少了1%。一旦达到预先定义的淀粉样斑块清除标准,参与者就能够停止服用药物。大约一半的参与者在12个月时达到了这一阈值,大约每10名参与者中有7人在18个月时达到了该阈值。
5月份公布积极结果时,donanemab的安全性成为外界的关注点。当时的研究中,礼来提到,严重淀粉样蛋白相关性影像异常(ARIA)的发生率为1.6%,包括两名归因于ARIA而死亡的受试者和另一名在出现严重ARIA事件后死亡的受试者。
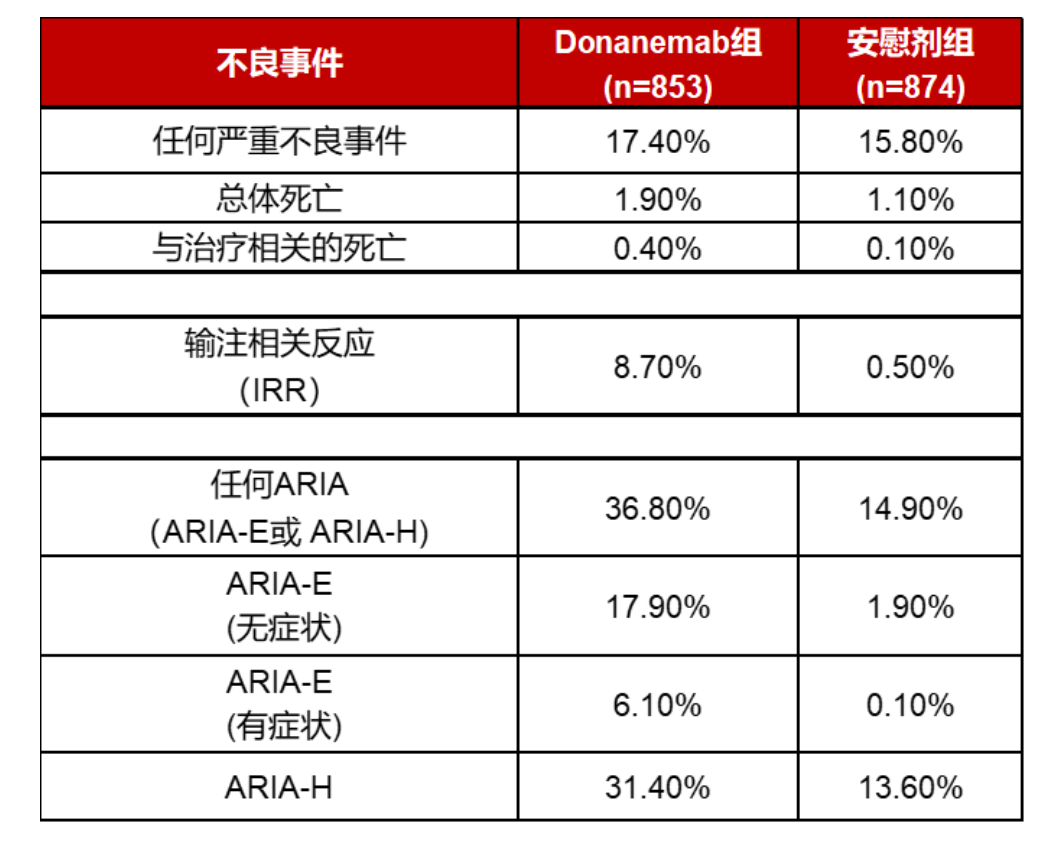
对于donanemab的安全性,在最新的研究中,ARIA和输注相关反应的发生率与之前的TRAILBLAZER-ALZ研究一致。从数据来看,donanemab组,36.8%发生了ARIA,高于安慰剂组的14.9%。
礼来表示,ARIA在这一类清除淀粉样蛋白斑块抗体药物中都有观察到,最常见的表现是大脑一个或多个区域的暂时性肿胀(ARIA-E)或微出血或浅表铁沉积(ARIA-H),无论哪种情况都可以通过核磁共振成像检测到,并且在某些情况下这些可能是严重,甚至致命的。因此应通过仔细观察、核磁共振成像监测以及在检测到ARIA时采取适当行动来管理此风险。此外,研究中还观察到严重的输注相关反应和过敏反应。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




