- +1
Nature:解锁RNA靶向成药难题,童玉铨等将无活性RNA结合小分子重编程为生物活性降解剂
原创 生物世界 生物世界

撰文丨nagashi
编辑丨王多鱼
排版丨水成文
1958年,弗朗西斯·克里克提出了著名的中心法则,为生遗传信息的传递构建一个大框架——DNA→RNA→蛋白质。其中,RNA发挥着一种连接枢纽的作用,如果说DNA是司令官,蛋白质是执行者,那么RNA就是沟通两者的通讯官。
事实上,RNA在健康和疾病生物学中的重要性已被充分证明,这也为生物医学研究RNA的功能或干预其功能障碍以治疗相关疾病创造了机会。对此,RNA降解、RNA编辑是当前干预RNA的常规手段,这些技术大多是基于序列的RNA靶向,即通过寡核苷酸的互补识别并招募核糖核酸酶进行切割。例如,siRNA、Cas13以及其他RNA编辑工具。
值得注意的是,这些技术需要碱基互补配对来识别靶标RNA,因此只能作用于RNA的非结构化区域。然而,许多天然RNA并不是一成不变的线性结构,而是折叠成复杂的三维结构。因此,目前迫切需要开发可以识别RNA结构区域的干预手段。
今日,美国斯克里普斯研究所的 Matthew Disney 教授团队(博士生童玉铨、博士后刘晓辉等为论文第一作者)等在 Nature 期刊发表了题为:Programming inactive RNA-binding small molecules into bioactive degraders 的研究论文。
该研究首次将核糖核酸酶靶向嵌合体(RIBOTAC)策略应用于非活性靶向RNA的小分子,从而将生物学上无活性的RNA靶向结合小分子转化为强大的特异性降解效应器,由此提供了一种靶向识别RNA结构区域的新型RNA降解工具,实现了通过小分子在体内特异性靶向降解致癌RNA。


通讯作者Matthew Disney教授(左),第一作者童玉铨(右)
打个形象的比喻,如果把基于碱基互补配对的RNA干预比作是开垦平原沃土,那么靶向RNA结构区域的干预技术就像是开采深山矿产,两者相辅相成,共同点亮“RNA王国”的全地图。
RNA可以是高度结构化的,并且其生物学功能通常由它的结构决定。值得注意的是,与蛋白酶类似,一些小分子可以与RNA折叠后呈现的结构性口袋相互作用,从而靶向结合RNA结构区域。然而,单靠小分子占据RNA结构性口袋往往不足以引发生物学效应,因此这些RNA结合小分子通常表现为没有生物活性。
在这项新研究中,研究团队开发了一种策略,将生物上无活性的RNA结合小分子转化为有效和特异性的功能效应子。具体来说,研究团队将这些RNA分子识别元件连接到RNase L1,该化合物可以结合并激活核糖核酸酶靶向嵌合体(RIBOTAC),从而切割靶标RNA结构区域。
而RIBOTAC技术正是由 Matthew Disney 教授团队开创的,他也在此基础上创立了RNA靶向小分子药物开发公司 Expansion Therapeutics,该公司致力于通过RIBOTAC技术,来靶向消除致病RNA,治疗肌强直性营养不良、遗传性渐冻症、额颞叶痴呆等因序列异常扩增导致的疾病。
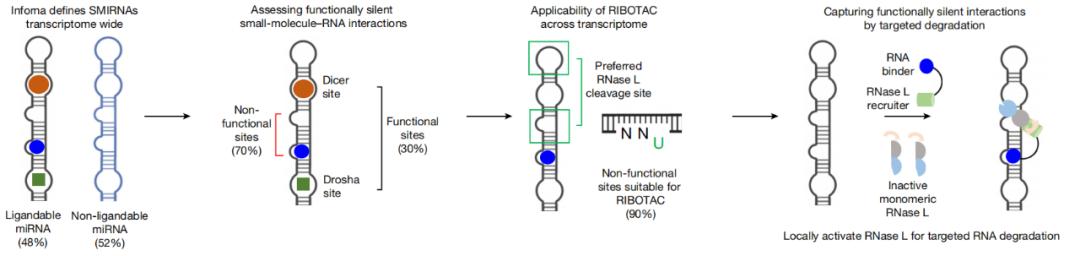
改造生物上无活性的RNA结合小分子,将其转化为强大的特异性RNA降解效应器
研究团队重点有三个方面:1)定义RNA结合小分子和RNA折叠之间的结合相互作用;2)以可编程的方式,将生物惰性的高选择性结合相互作用转化为靶向降解的诱导剂,从而提供有效和选择性的功能抑制剂;3)建立一个RNA结合小分子可以消除RNA结构区域的研究范例。
该论文的通讯作者 Matthew Disney 教授表示,他们发现了大约2000种能够结合药物样小分子的新RNA结构,并确定了六种能够结合RNA的新化学型,基本上创造了一本关于可成药RNA折叠的百科全书!
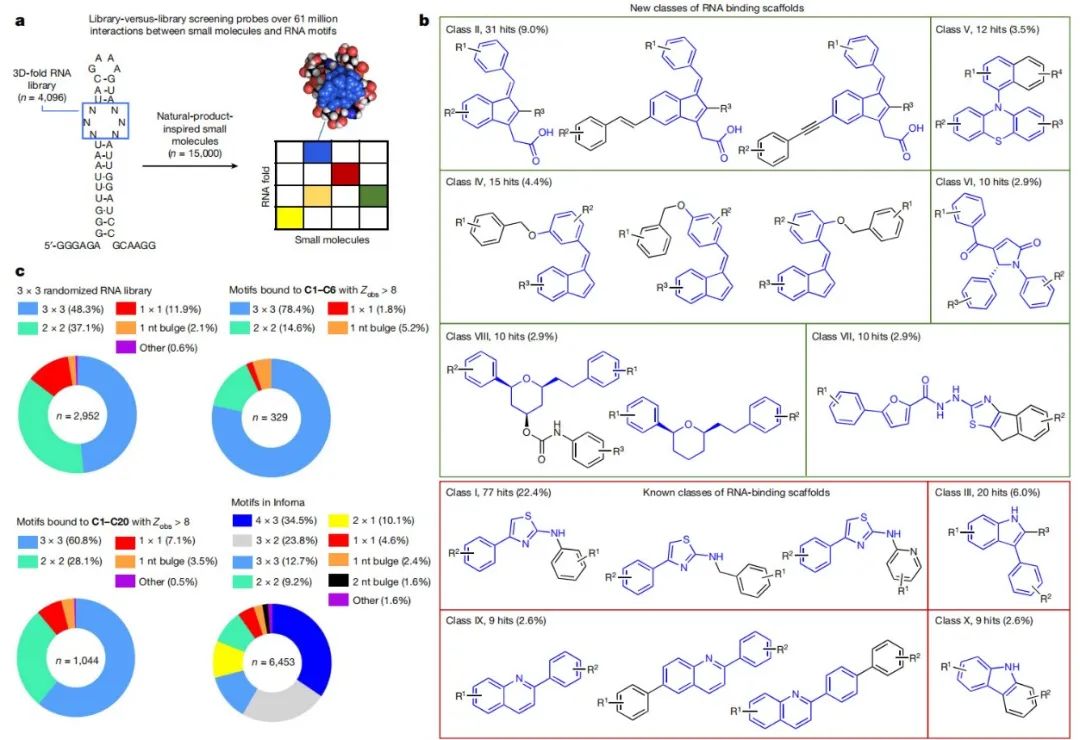
文库筛选定义了新的RNA结合小分子和可药物化靶点
使用Informa数据库设计的结合物作为模板,研究团队开发了RIBOTAC降解剂,使依赖于这些癌蛋白活性的转录和蛋白质组学的生物学过程失效。不仅如此,研究团队提供了一个概念验证,为疾病相关的microRNA-155(pre-miR-155),JUN mRNA和MYC mRNA的前体设计选择性降解剂。
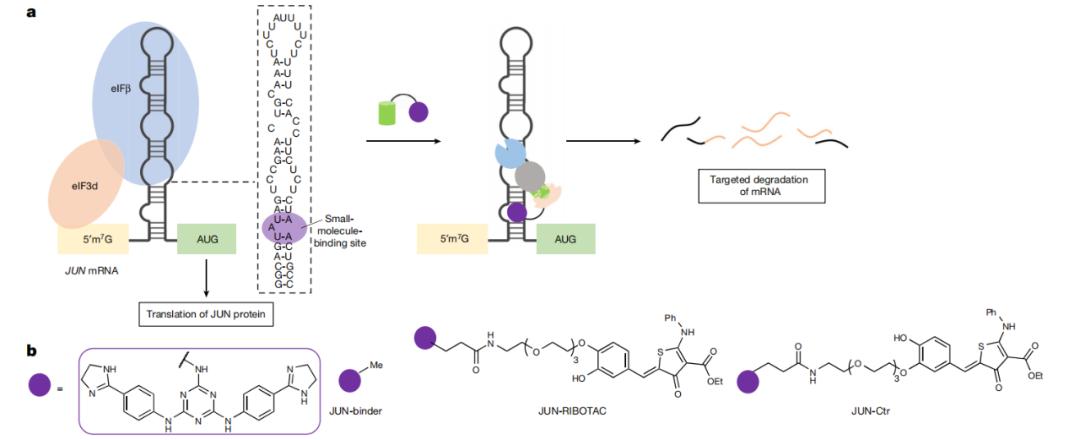
在乳腺癌细胞中以RNase-L依赖的方式选择性降解JUN mRNA
值得一提的是,MYC基因突变也是人类癌症中最常见的基因突变之一,它不仅能够导致正常细胞的癌变,还会促进癌细胞逃避免疫系统的攻击。研究团队旨在测试破坏MYC RNA的RIBOTAC化合物的功效,并显示它们有效地杀死由MYC驱动的B细胞淋巴瘤。
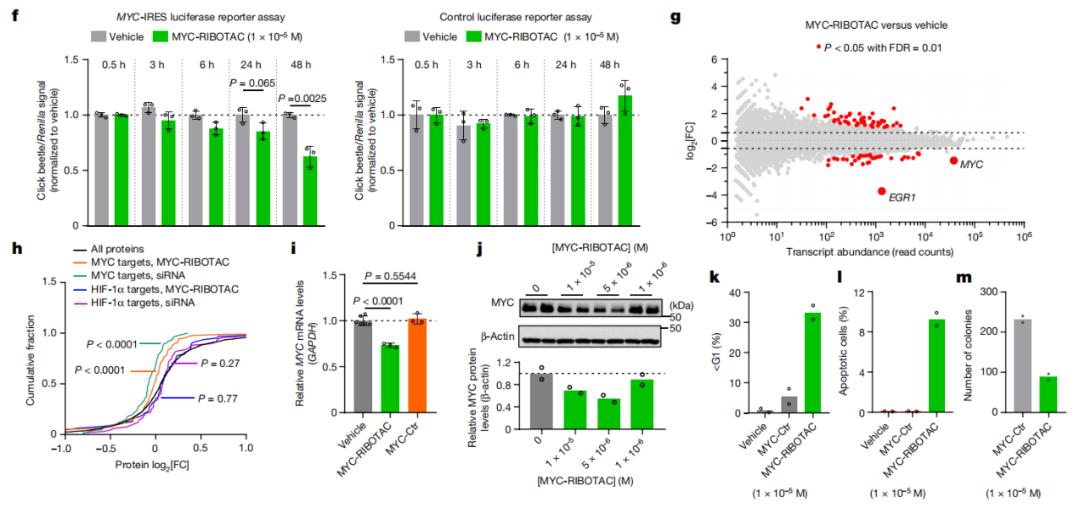
靶向降解MYC RNA有效地杀死由MYC驱动的B细胞淋巴瘤
总的来说,这些研究结果表明,可以利用小分子RNA靶向降解将强而无活性的结合相互作用转化为有效且特异性的RNA功能调节剂。基于此,科学家们现在可以设计出特定的RNA降解物来降解许多致癌RNA,这将代表癌症治疗中真正的革命性意义的进步。
论文链接:
https://www.nature.com/articles/s41586-023-06091-8
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




