- +1
TIL疗法即将进入临床使用:免疫时代,肺癌患者如何科学选择?
·免疫治疗有什么优势?第一,可以增强其他治疗手段的效果;第二,可以减少其他治疗的副作用;第三,可以降低肺癌复发和转移的风险。
·人体的免疫系统有一定的记忆能力,如果它学会了如何识别和清除癌细胞,那么即使有少量的癌细胞残留或者再次出现,免疫系统也能够及时地发现和消灭它们,从而让肺癌成为可控制的慢性病。

Iovance Biotherapeutics
5月26日,新兴生物技术公司 Iovance Biotherapeutics(IOVA.US)宣布,美国食品药品监督管理局(FDA)接受了其治疗晚期黑色素瘤患者的肿瘤浸润淋巴细胞(TIL)疗法 Lifileucel 的生物制剂许可的申请(BLA),这也是首个向FDA提交BLA的TIL疗法。初步审查后,FDA没有发现任何潜在的审查问题。这昭示着TIL即将正式进入临床使用阶段。
TIL(Tumor Infiltrating Lymphocytes,肿瘤浸润淋巴细胞)是一种从肿瘤组织中分离出的浸润淋巴细胞。可以这样说,每个人体内都有着抗肿瘤免疫。当机体免疫系统发现体内的癌细胞后,就会发动免疫大军,深入到肿瘤组织内部,与癌细胞厮杀,这些深入癌组织内部的淋巴细胞,就是TIL。
简单来讲,免疫疗法主要是利用人体自身的免疫系统来攻击肿瘤。近五年来,免疫疗法百花齐放,TILs疗法是其中发展较早的肿瘤免疫疗法之一,面对如此多的选项,加上免疫疗法通常费用不菲,肺癌患者如何选择合适的免疫治疗方案,避免少走或者不走弯路?
首先,要知道免疫治疗有什么优势?第一,可以增强其他治疗手段的效果;第二,可以减少其他治疗的副作用;第三,可以降低肺癌复发和转移的风险。人体的免疫系统有一定的记忆能力,如果它学会了如何识别和清除癌细胞,那么即使有少量的癌细胞残留或者再次出现,免疫系统也能够及时地发现和消灭它们,从而让肺癌成为可控制的慢性病。
当然,免疫治疗也不是没一点副作用的,免疫治疗是利用肺癌患者自身的免疫力来抗击肿瘤,这类药物不能直接消灭癌细胞,而是激活针对癌细胞的免疫反应,让免疫细胞成为杀死癌细胞的利器【1】。但是被激活的免疫细胞也会攻击正常的细胞,导致一些自身免疫性的副作用,比如皮疹、肠炎、腹泻、肝损害等。这些副作用发生率和严重程度都比较低,大多数患者可以耐受。
目前有哪些免疫治疗方法可以用于肺癌呢?
1、免疫检查点抑制剂
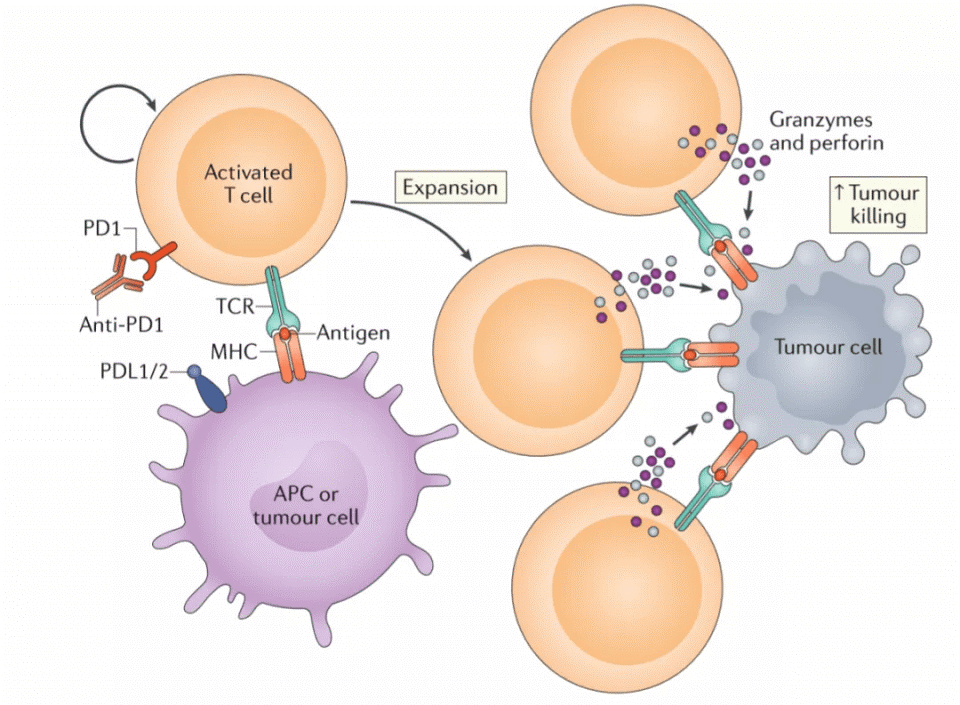
免疫检查点抑制剂的作用原理。图片来源:Thoracic cancer
免疫检查点抑制剂是目前最常用也最有效的一类免疫治疗药物,它们主要作用于免疫系统中调节 T 淋巴细胞激活的分子,在肿瘤情况下则可以被癌细胞利用来逃避免疫监视【2】。目前已经批准上市用于肺癌治疗的免疫检查点抑制剂主要有CTLA-4单克隆抗体、PD-1和PD-L1单克隆抗体等。这些药物可以单用或者联合使用,根据不同的靶点和机制,产生不同程度的抗肿瘤效果。
2、过继性细胞免疫治疗
过继性细胞免疫治疗是指将来源于患者或供者体内具有抗肿瘤活性的免疫细胞,在体外进行激活、扩增或改造后再输回患者体内,以达到清除肿瘤或增强机体免疫力的目的。过继性细胞免疫治疗主要包括肿瘤浸润性淋巴细胞(TILs)和T细胞受体修饰(TCR-T)两种方法【3】。
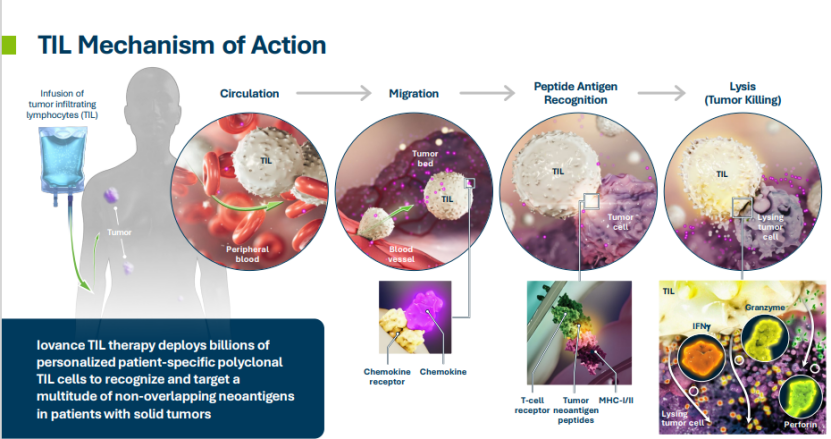
肿瘤浸润淋巴细胞的提取和制作流程。图片来源:https://www.pharmcube.com/index/news/article/10805)
TILs是从肿瘤组织中分离出来的淋巴细胞,它们已经对肿瘤抗原有了一定的识别和反应能力,经过体外扩增后再输回患者体内,可以增强对肿瘤的杀伤作用【4】。
TILs有其天然优势:首先,靶向性强,TIL不是单个T细胞克隆,包含针对多种肿瘤特异性抗原的T细胞,多靶点靶向肿瘤组织,治疗后复发率低;其次,对实体瘤效果好、副作用小,TIL是人体本身存在的T细胞,没有免疫原性,且对肿瘤的特异性强,靶向毒性小;最后,TILs细胞经过分离筛选后,加入IL-2(白细胞介素-2,是免疫系统中的一类细胞生长因子)进行培养,增加免疫细胞存活的几率,最大限度地扩增免疫细胞。
TIL疗法也有一定的缺陷,对样本要求高,一般可以提取到淋巴细胞的新鲜肿瘤样本难获得,此外,具有抗肿瘤活性、增殖能力强的TIL细胞更难获得。TIL是高度定制化的疗法,现有操作程序成本高、耗时长。TIL也容易被肿瘤微环境抑制,发生功能耗竭。
TCR-T是指将人工合成的特定T细胞受体(TCR)基因转染到患者自身T细胞中,使其能够识别肿瘤细胞表面的抗原肽,从而发挥抗肿瘤效果【5】。
总之,过继性细胞免疫治疗的优点是可以持久地存在于体内,发挥长期的免疫记忆作用,但是也可能引起一些副作用,如细胞因子风暴和神经毒性等。
3、CAR-T细胞
CAR-T细胞是个明星,传说中的120万元一支的就是“它”,这种疗法在肺癌治疗能否发挥它神奇的功效,一举把肺癌攻克呢?这个问题在临床中我被问了无数次,再向大家解释一下。
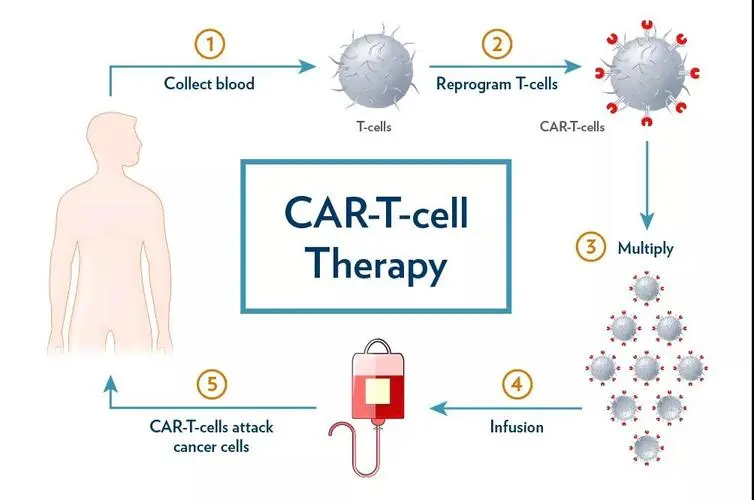
什么是CAR-T及制作流程。图片来源:CAR-T细胞临床试验官网 http://www.aibbang.com/NewDetail.aspx?aid=591
所谓CAR-T细胞疗法,就是嵌合抗原受体T细胞免疫疗法。通俗一点,CAR-T细胞就是把病人的免疫T细胞在体外通过技术改造,令其识别肿瘤细胞表面的抗原,把改造过的T细胞扩增后回输给病人,达到识别、杀死癌细胞的治疗效果【6】。T细胞的提取好解决,难就难在这个抗原,肺癌是实体肿瘤,不像血液病,血液病的所有细胞长得一模一样,然而一个肺癌病人的一块肿瘤,所有的细胞不是一个模子里刻出来的,他们部分长得一样,部分长得不一样,不一样的地方就是他们表面的抗原。所以大家就可以理解了CAR-T疗法在肺癌治疗上一直存在个卡脖子的问题,疗效嘛,就知道了。
CAR-T 细胞在血液肿瘤方面已取得了显著的效果,关键是血液肿瘤是单克隆,所有细胞基本一致,没有太大变化;而实体肿瘤则面临着很多挑战,首先是缺乏特异性和高表达的靶点抗原;其次是可能引起严重的毒副反应,如细胞因子风暴和神经毒性;再次是受到肿瘤微环境中多种因素的影响和抑制。
4、肿瘤疫苗
肿瘤疫苗是一种利用肿瘤相关抗原(TAAs)或肿瘤细胞裂解物等刺激机体产生肿瘤特异性免疫应答的方法,既可以用于预防肿瘤的发生,也可以用于治疗已有的肿瘤【7】。
肿瘤攻克的方向是疫苗。图片来源:MIT Technology Review
肿瘤疫苗分为预防性和治疗性两大类,预防性肿瘤疫苗主要针对一些由病毒感染引起的肿瘤,如乙型肝炎疫苗和人乳头瘤病毒(HPV)疫苗,它们可以在健康人群中注射,产生针对这些致癌病毒的免疫反应,从而降低肝癌和宫颈癌的发生率。
治疗性肿瘤疫苗主要针对已有的肿瘤患者,通过注射含有特定抗原的物质,激活机体对抗癌细胞的免疫反应,从而达到治愈或缓解肿瘤的目的。目前已经有一些治疗性肿瘤疫苗进入临床试验阶段,如全细胞、多肽或蛋白、核酸等类型的肿瘤疫苗。肿瘤疫苗的优势在于可以产生持久的免疫记忆效果,降低复发和转移的风险,但是也存在着一些挑战。
5、新兴免疫治疗方法
一些新兴的免疫疗法正在不断探索中,主要包括寻找新的免疫检查点或联合使用不同的免疫检查点抑制剂、开发新型的CAR-T细胞或TCR-T细胞、利用微生物或纳米材料等增强免疫反应等,这些方法有望为肺癌患者带来更多的治愈机会【8】。
总结一下肺癌免疫治疗的原则:
免疫治疗是肺癌治疗的新希望,但也不是万能的,不是每个患者都能从中获益。需要根据患者的免疫微环境状态、肿瘤特性、基因突变结果等因素进行个体化的选择和调整。
(作者唐东方,系复旦大学附属华东医院胸外科主治医师,ESTS member ship,杜克大学访问学者,上海市医师协会胸外科分会会员,主持国家自然科学基金和上海市浦江人才课题,主持在研临床研究项目:肿瘤浸润淋巴细胞治疗晚期肺癌的临床研究。)
参考文献:
1. 杨森. 肿瘤免疫疗法是如何帮助人类抗击癌症的. 健康忠告. 2020.
2. 温玉琴. 研究发现治疗肺癌的新免疫疗法. 广东药科大学学报. 2018;34(2):1.
3. 谭思怡, 孟凡岩, 刘宝瑞. T淋巴细胞归巢:实体肿瘤过继性细胞治疗的关键因素. 中国肿瘤生物治疗杂志. 2021;28(2):6.
4. 任嘉慧, 周云乔, 高鹏翼, 张琪, 张秀军, 王铁山. 肿瘤浸润淋巴细胞在实体瘤治疗中的研究进展. 中国医药导刊. 2022;24(11):6.
5. 罗斌, 楚小鸽, 于盼, 田建辉. T细胞受体(TCR)组库多样性及其在肺癌防治中的应用进展. 细胞与分子免疫学杂志. 2022;38(10):5.
6. 王翔宇, 张彦明, 吴德沛. 双靶点嵌合抗原受体T细胞免疫疗法在血液肿瘤中的研究新进展. 国际输血及血液学杂志. 2022;45(2):6.
7. 王艳梅, 陈坤, 曲春枫. 肿瘤疫苗的研究进展. 国际免疫学杂志. 2018;41(6):7.
8. 彭译漫, 罗香梦, 陈婧瑶. 肿瘤微环境代谢的研究进展及免疫治疗新策略. 四川大学学报(医学版). 2023;54(3):505.





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




