- +1
港大化学团队以营养补剂铬元素靶向能量合成调控糖代谢
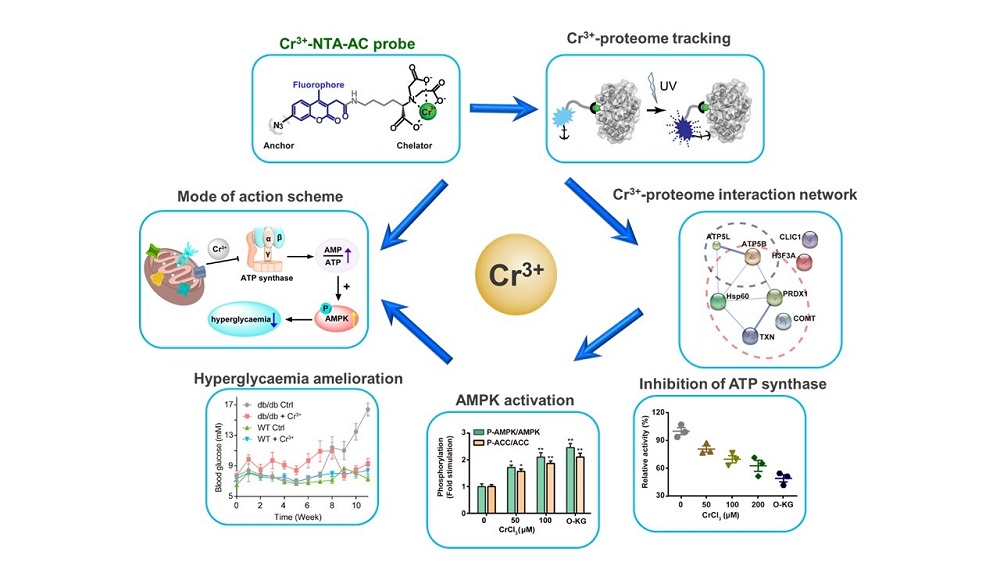
图1. 铬(III)荧光探针可以标记细胞内铬(III)特定结合蛋白质(上),铬(III)结合蛋白集中于线粒体生物功能调节(右),铬(III)降低ATP synthase 活性(右下),铬(III)启动下游的腺苷单磷酸活化蛋白激酶AMPK通道(下),铬(III)改善葡萄糖代谢(左下),铬(III)作用模式图(左)。
(原新闻稿已于4月12日发布)
香港大学(港大)理学院化学系孙红哲教授团队最近于降血糖研究取得突破进展,并于国际著名学术期刊《自然·通讯》(Nature Communications)上发表成果。
团队的研究确认,营养补充剂铬元素(III)可以通过抑制三磷酸腺苷(ATP)合成酶 (ATP synthase) 的活性,调节细胞能量稳态,增加细胞对葡萄糖的代谢能力,改善由高糖引起的线粒体形变,并提高二型糖尿病小鼠对葡萄糖的代谢能力。为了找到铬(III)蛋白标靶及其作用机制,研究团队开发了新型的荧光探针,实现铬(III)蛋白组在细胞内的高分辨时空示踪及鉴定。实验进一步揭示铬(III)取代 ATP synthase活性中心的镁离子,从而降低其活性,改善葡萄糖代谢的机制。这一研究结果为降血糖研究提供了新的思路。
「铬(III)是一种常用的营养补充剂,常被用于治疗糖尿病、减肥和促进肌肉发育等方面。但科学家们一直无法确定铬(III)在生物体内的蛋白质标靶和作用机制。研究团队使用了基于荧光探针的新方法,成功解决了这个科学难题,揭示了铬(III)的蛋白标靶和分子机制。这是一个极为重要的研究成果,对基础科学和人类健康应用领域都有着重要意义。」领导团队的孙红哲教授说。
研究背景
糖尿病是一种慢性的代谢疾病,全球超过五亿人患有此病,每年造成近两百万人死亡,且超过95%的糖尿病患者患有二型糖尿病(T2DM),严重危害人类的健康。三价铬(铬(III))此前已于对抗二型糖尿病的动物实验中显示功效(例如胰岛素抵抗小鼠和高脂饮食诱导的糖尿病小鼠)。自有报导大鼠膳食添加铬(III)可增加血糖去除率以来,铬(III)已被广泛用于糖尿病治疗、减肥以及肌肉发育的营养补剂。目前铬(III)是美国市场上第二畅销的矿物质补剂,仅次于钙。
尽管铬元素在病理生理学中非常重要,但它是元素周期表中最不容易理解的过渡金属元素之一。半个世纪以来,关于铬(III)在人体生理学中的重要性、药物学特性、分子靶点和作用机制,一直是学术界热烈辩论的议题。最初,人们认为活性低分子量铬(III)与肽(chromodulin)结合可以起到调节作用,但这种理论未被充分证实。目前普遍认为,铬(III)可以改善葡萄糖代谢,保持正常血糖水平,调节碳水化合物和脂类代谢,并增强胰岛素信号。然而,其中潜在的分子机制仍不清楚,这是因为难以确定铬(III)的生理作用分子标靶。这些生物分子对于了解铬(III)的生理学和药理学作用至关重要,因此它们也被称为铬生物化学的「圣杯」。
迄今为止,除了血浆中的蛋白质以外,在细胞或组织中尚未找到能与铬(III)直接结合的蛋白质。即使使用各种分离和检测方法,也很难检测到铬(III)结合蛋白质的信号,这可能归因于它容易和与其结合的蛋白质解离,而目前尚无方法适合于追踪活细胞中铬(III)结合蛋白。对于与蛋白质结合较弱或瞬态的金属,利用小分子荧光技术标记金属蛋白质有助于理解它们在活细胞中的分布和功能调节。
主要发现
团队根据之前的研究工作,成功合成了一种能够在活细胞内识别铬(III)结合蛋白的荧光探针。该探针由三部分组成:荧光基团香豆素(AC)、金属螯合基团氨三乙酸(NTA)和光敏感交联基团迭氮苯基。探针进入细胞后与铬(III)结合,铬(III)与蛋白质中的特异氨基酸结合,使得探针稳定地结合在金属蛋白质上,而在紫外光照射下,迭氮苯基会与金属结合位点邻近的氨基酸形成共价键。这种探针能够帮助研究人员更好地理解铬(III)结合蛋白质在活细胞中的位置和功能。
团队使用上述探针在活细胞中监测铬(III)结合蛋白质的分布,结果发现这些蛋白质主要集中在细胞的线粒体上。通过进一步的实验,他们确认了人体细胞中第一个铬(III)蛋白组,并发现铬(III)结合在ATP synthase活性中心后,会取代酶底物的镁离子,从而降低ATP合成酶的酶活性并启动下游通道,减缓高血糖对线粒体的损伤,改善葡萄糖代谢。这个作用模式在二型糖尿病小鼠模型中得到了验证。此外,这项研究还解决了铬(III)如何在分子水平上改善高血糖应激的问题,同时,该探针也可广泛用于其它金属离子结合蛋白的监测。由于确认了多个铬(III)结合蛋白质,这项研究也为以后深入研究铬(III)在其他疾病(如抗神经退化性疾病和抗衰老)中的药理作用开启了新的视野。
该研究在《自然·通讯》期刊获得了多位审稿人的高度评价。他们认为这项研究利用了一种荧光探针,巧妙地解决了七十多年来铬元素分子标靶鉴定的重大难题。而且,研究人员还成功地使用了荧光成像与质谱联用的方法,来鉴定铬结合蛋白。这不仅是化学生物学领域的一次创新,更是对人类健康事业的一次重大突破。
关于研究团队
本研究由香港大学理学院化学系孙红哲教授带领,同属化学系的王海波博士、胡立刚博士、李洪艳博士授为本文的共同第一作者。其他参与这项研究的成员包括同系的黎佑芷博士、魏雪莹研究生、徐小晗博士、曹振坤博士、张苑茵博士,以及港大李嘉诚医学院的徐爱民教授、中国科学院生态环境研究中心江桂斌院士、胡立刚和周群芳研究员、香港城市大学何明亮教授及万倩娅博士、江汉大学曹慧明博士。特此鸣谢香港研究资助局和香港特别行政区食物及卫生局医疗卫生研究基金,以及港大叶志成范港喜基金对本研究的大力支持。
关于孙红哲教授
孙红哲教授是港大叶志成范港喜基金教授(生物无机化学)及化学系讲座教授。他的研究重点包括金属蛋白质组学、药物化学(抗菌剂的发现)和生物化学。孙教授在克服对超级细菌的抗菌素耐药性、开发抗冠状病毒药物和金属生物学等领域发表了一系列广受认可的工作。
更多有关孙教授的资料,可参看以下网址:https://www.bioinorg-chem.hku.hk/
研究论文可见于:https://www.nature.com/articles/s41467-023-37351-w
图片下载及说明:https://www.scifac.hku.hk/press
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




