- +1
【学术前沿】Cell Regen l IL-6/gp130信号在器官再生中的作用

Research Highlight | Published: 23 March 2023
在古老的神话中,肝脏具有惊人的再生能力,为人类盗火的普罗米修斯就因此而不得不每日承受被恶鹰啄食肝脏的惩罚。在现实中,肝脏是一种具有显著再生能力的器官,而肝细胞向未成熟状态的重编程是补充肝细胞的重要机制之一。

因盗火而遭受惩罚的普罗米修斯
近日,中国医学科学院阜外医院聂宇研究员在Cell Regeneration上发表了题为“IL-6/gp130 signaling: a key unlocking regeneration”的研究亮点文章,主要探讨了日前中国科学院分子细胞科学卓越创新中心研究员惠利健研究组、上海营养与健康研究所研究员李虹研究组和研究员李亦学研究组的一项合作研究(Li et al. 2023)。该研究报道,肝细胞的去分化依赖于Kupffer细胞的IL-6信号,并且在炎症条件下基因表达的重编程不同于胚胎肝细胞特化期间基因表达的调控,突出了组织再生修复过程中细胞外微环境与细胞可塑性之间的紧密联系。

组织再生过程中新生细胞的来源主要有两种,一种来自于成体干细胞自我扩增并分化,另一种来自于原有的已分化的细胞。已分化的细胞可以通过去分化或者重编程的过程促进组织再生,该现象在多种组织器官中均有发现,如肺脏、肝脏、胰腺和小肠等。在肝脏的损伤再生修复过程中,成熟肝细胞发生去分化,重编程为Sox9+阳性类肝前体细胞(Liver progenitor-like cells, LPLCs),是肝脏组织再生的细胞重要来源之一。
IL-6及其家族细胞因子介导的炎症反应已被广泛报道与多种器官的组织再生密切相关。IL-6在调控肝脏中的作用及其机制还不清楚。在前述惠利健、李虹和李亦学研究组的合作研究发现,kupffer细胞来源的白细胞介素-6(IL-6)用于LPLC生成。
该研究团队利用单细胞测序技术解析肝细胞重编程过程中响应的损伤信号,发现免疫信号的激活与肝细胞重编程过程高度正相关;通过对肝脏不同种类免疫细胞的敲除,并结合不同巨噬细胞亚群敲除的小鼠模型,鉴定出Kupffer细胞是肝细胞重编程发生必要的巨噬细胞亚群;进一步对Kupffer细胞表达谱和Kupffer细胞特异分泌因子的筛选研究发现,IL-6通过结合肝细胞IL-6受体/gp130受体,可直接激活STAT3信号通路诱导肝细胞去分化,促进肝脏组织再生;利用结合位点分析法(ChIP-seq),证实STAT3作为转录因子结合在损伤特异的增强子上,促进了肝前体基因的表达。
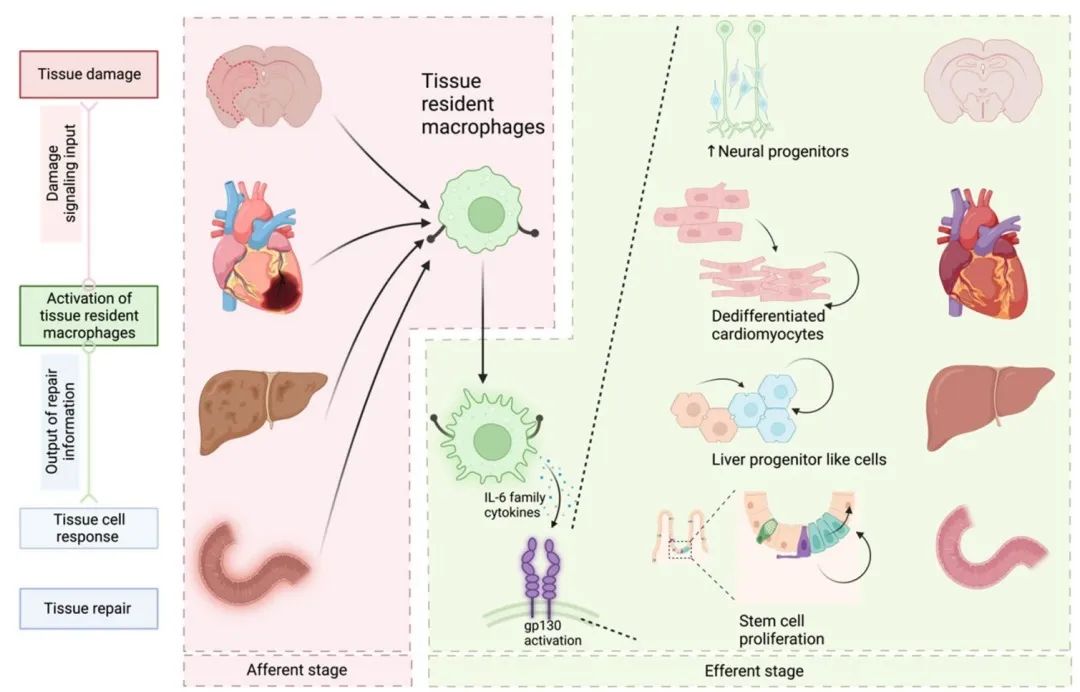
组织驻留巨噬细胞作为组织损伤的感受器
总之,文章总结了肝脏损伤后驻留巨噬细胞的炎症信号通过损伤特异的转录调控模式诱导肝细胞去分化、促进肝脏组织再生的分子机制,为开发诱导肝细胞去分化相关药物治疗肝脏疾病提供了潜在的作用靶点。
–
原标题:《【学术前沿】Cell Regen l IL-6/gp130信号在器官再生中的作用》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




