- +1
中山大学马骏、柳娜团队发现肿瘤抑制放疗免疫激活新机制
原创 转网 转化医学网

本文为转化医学网原创,转载请注明出处
作者:Sophia
导读:放疗是多种肿瘤的重要治疗手段,虽然放疗可以促进抗肿瘤免疫,但这种现象背后的机制尚不清楚。
近日,中山大学肿瘤防治中心马骏、柳娜团队在《Nature Communications》上发表了题为“TRIM21 inhibits irradiation-induced mitochondrial DNA release and impairs antitumour immunity in nasopharyngeal carcinoma tumour models”的研究论文,该工作鉴定出抑制放疗免疫激活的关键E3泛素连接酶TRIM21,并发现其通过抑制放疗诱导的线粒体DNA的释放,抑制 cGAS-STING及IFN-I信号介导的CD8+T细胞抗肿瘤免疫反应的激活,最终引起肿瘤放疗抵抗。

https://www.nature.com/articles/s41467-023-36523-y
研究背景
01
放射治疗广泛用于治疗各种类型的实体瘤,肿瘤细胞中的DNA损伤被认为是其细胞毒性作用的主要机制。最近,辐射诱导的先天性和适应性免疫反应已成为研究重点。同样,放疗是鼻咽癌的主要治疗策略,因为它对辐射高度敏感。联合放化疗显著提高了生存率,但约 20% 的患者因放射阻力而出现肿瘤复发。据报道,癌蛋白(即 MYC 和 β-连环蛋白)和肿瘤抑制蛋白(即USP44)与鼻出血抗性有关。越来越多的证据表明,放疗诱导的抗肿瘤作用是由先天性和适应性免疫反应的激活引发的。然而,我们对损害辐射诱导的抗肿瘤免疫的机制知之甚少。
泛素-蛋白酶体系统是翻译后水平上蛋白质降解、功能和亚细胞运输的关键同源调节因子。E3泛素连接酶的功能障碍是参与各种类型癌症发展和进展的关键调节因素。研究指出,肿瘤内在E3连接酶介导程序性死亡配体-1(PD-L1)表达的调节和巨噬细胞浸润,强调了泛素系统在抗肿瘤免疫中的作用。然而,肿瘤中TRIM21的表达是否会影响抗肿瘤免疫,特别是放疗诱导的免疫力,在很大程度上尚不清楚。
研究进展
02
为了确定可能损害T细胞介导的抗肿瘤免疫的潜在致癌靶点,我们首先表征了128名鼻咽癌患者的CD8 T细胞浸润和抗肿瘤反应升高指标的基因集表达评分,通过具有弱而强大的 T 细胞抗肿瘤免疫力的生存分析显示,T细胞介导的抗肿瘤免疫评分低的患者在根治后无病生存率较差。
正如预期的那样,具有弱而强大的T细胞介导的抗肿瘤免疫评分的肿瘤表现出不同的基因表达图谱。三种E3泛素连接酶在T细胞介导的抗肿瘤免疫评分较弱的患者的肿瘤中显著上调。由于只有TRIM21与鼻咽癌无病生存率差显著相关,其表达水平与CD8 T细胞浸润和抗肿瘤反应相关基因的转录水平呈负相关,例如CD8A,PRF1,GZMA,GZMB,IFNG和LCK,我们选择了TRIM21进行进一步研究。分析进一步证实,具有较高TRIM21表达的NPC肿瘤含有较少的浸润CD8 T细胞和活化的DC,这表明TRIM21可能在抑制T细胞介导的抗肿瘤免疫中起至关重要的作用。
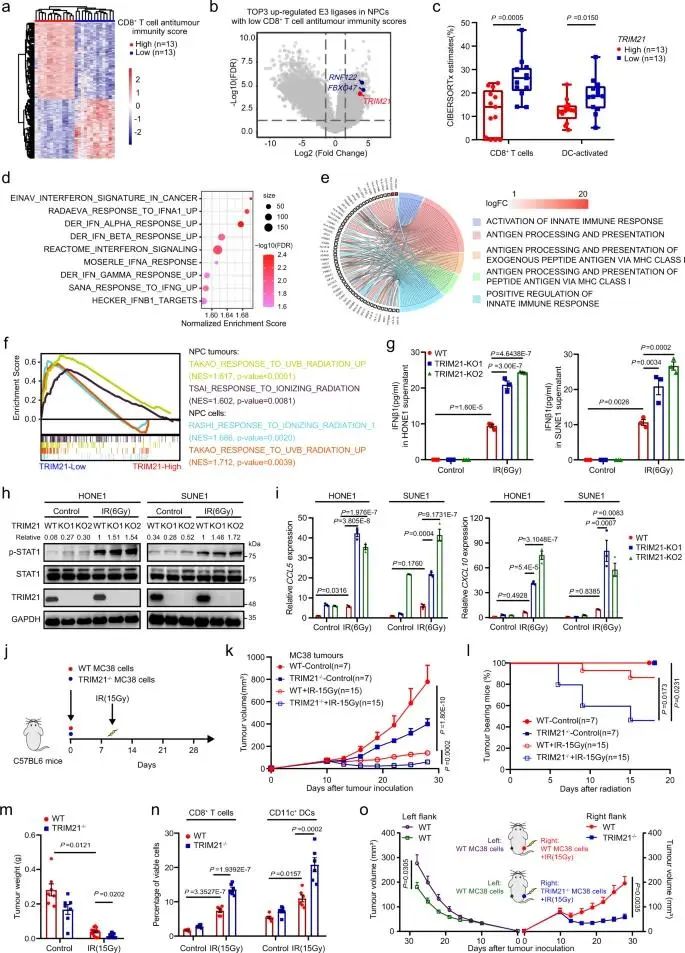
肿瘤细胞中的TRIM21表达会损害辐射诱导的T细胞介导的抗肿瘤免疫
研究意义
03
总之,我们的研究表明,肿瘤细胞内在E3连接酶TRIM21抑制辐射引发的,VDAC2依赖性和mtDNA诱导的鼻咽癌中STING-I型IFN信号传导和抗肿瘤免疫反应。鉴于TRIM7的耗竭可以增强辐射诱导的抗肿瘤免疫力,TRIM21的基因缺失或药理学抑制可能是一种有前途的癌症治疗策略。
参考资料:
https://www.nature.com/articles/s41467-023-36523-y
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。

原标题:《【Nature子刊】中山大学马骏、柳娜团队发现肿瘤抑制放疗免疫激活新机制》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




