- +1
【学术前沿】Cancer Res | 中山大学郭剑平团队发现AKT阻断SIK1介导的STAT3抑制…
PI3K - AKT信号通路在癌症中经常失调,在大约50 %的乳腺癌中被过度激活。虽然目前已经开发了直接靶向PI3K - AKT轴的抑制剂,但其临床疗效仅限于部分患者。确定AKT驱动肿瘤发生的机制有利于开发出新的阻断通路信号及抑制乳腺肿瘤生长的替代方法。
2023年2月20日,中山大学郭剑平团队在Cancer Research 上在线发表题为“AKT blocks SIK1-mediated repression of STAT3 to promote breast tumorigenesis”的研究论文,该论文结合质谱分析发现,盐诱导激酶1 ( SIK1 )与AKT结合并发生AKT介导的磷酸化,这损害了SIK1的肿瘤抑制功能。因此,AKT以磷酸化依赖的方式解除了SIK1对STAT3的结合和抑制,从而导致乳腺细胞肿瘤发生。
在AKT介导的磷酸化后,SIK1与14 - 3 - 3相互作用,并转移到细胞质中,异构酶Pin1促进SIK1与E3连接酶ITCH相互作用,促进SIK1泛素化和随后的降解。这些发现表明,SIK1是AKT的底物,将AKT的致癌功能与STAT3的激活联系起来,提示靶向JAK2 - STAT3轴或可作为治疗AKT的新策略。
乳腺癌是全球女性肿瘤发病率和死亡率的首要原因。近几十年来,尽管多种经典分子已经成功地通过靶向雌激素受体( ER )或人类表皮生长因子受体2 ( HER2 )介导乳腺癌的治疗,但耐药性和缺乏有效的策略来对抗三阴性乳腺癌( TNBC )仍是当前乳腺癌治疗的主要挑战。
随着多组学技术的发展,研究者们越来越多地在其基因组驱动因素的基础上发现新的乳腺癌亚型,包括PI3K - AKT - mTOR通路复合物、生长因子受体(例如ERBB2)、细胞周期调节因子(例如CCND1)、ER信号和DNA修复(如BRCA1 / 2)等。在乳腺癌中,PI3K - AKT通路在大约50 %的患者中持续激活,因此成为乳腺癌的研究热点和潜在的治疗靶点。然而,其副作用使得直接靶向PI3K - AKT通路的抑制剂的临床应用受到了限制。因此,迫切需要一种在乳腺癌中调节AKT下游效应因子的替代方法。
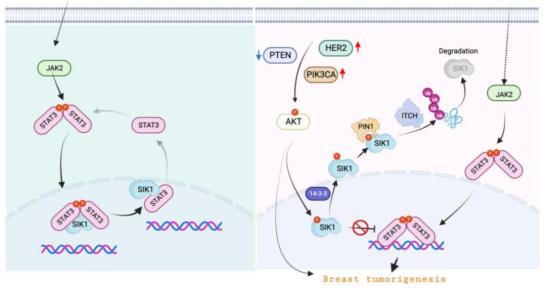 AKT在乳腺癌发生过程中调控SIK-STAT3通路的模型(图源自Cancer Research )
AKT在乳腺癌发生过程中调控SIK-STAT3通路的模型(图源自Cancer Research )盐诱导激酶1 ( SIK1 )是AMPK相关激酶,调节能量反应相关的生理病理过程,如糖异生和脂质代谢。最近的研究确定了SIK1是肝激酶1 ( LKB1 )缺陷的非小细胞肺癌的主要参与者。然而,SIK1在乳腺癌中的确切作用及其上游调控因子尚不清楚。信号转导和转录激活因子( signal transducers and activators of transcription,STAT )家族转录因子,包括STAT1 - 6,在生理和病理过程中发挥独特而关键的作用。在这些转录因子中,STAT3可能通过响应IL6诱导的JAK2激活,在肿瘤发生中发挥重要的作用。虽然已经确定了调节STAT3转录激活的多种机制,包括磷酸化、甲基化和棕榈酰化,但经典的信号通路如PI3K - AKT通路是否激活STAT3尚不清楚。
尽管拮抗JAK2或STAT3的抑制剂已被开发并用于癌症治疗,这些抑制剂是否能成功用于乳腺癌治疗尚未确定。针对这些发现和问题,该团队发现生理水平的SIK1通过与STAT3结合来抑制STAT3的转录激活和致癌功能来维持其肿瘤抑制功能。在特定条件下,活化的AKT直接磷酸化SIK1,促进SIK1胞质转位、Pin1结合和ITCH识别降解,从而激活STAT3的致癌功能,促进乳腺癌的发生。总之,该发现强调了一个有前途的策略,即靶向JAK2 - STAT3通路来对抗由AKT过度激活驱动的乳腺癌。
参考信息:
https://doi.org/10.1158/0008-5472.CAN-22-3407
原标题:《【学术前沿】Cancer Res | 中山大学郭剑平团队发现AKT阻断SIK1介导的STAT3抑制促进乳腺肿瘤发生》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




