- +1
Science:曾启群等揭示肿瘤免疫逃逸新机制,带来癌症治疗新靶点
以免疫检查点抑制剂(ICB)为代表的肿瘤免疫疗法彻底改变了癌症治疗格局。ICB可以激活T细胞,从而逆转CD8 T细胞耗竭、促使免疫细胞发现并杀死肿瘤细胞。然而,ICB的局限性也很明显。ICB仅对少数肿瘤患者有效,并且不少患者无法长期从治疗中受益。因此,科学界亟需找出肿瘤细胞发生免疫逃逸的机制,从而开发新的肿瘤免疫疗法。
2022年11月17日,瑞士洛桑联邦理工大学的 Douglas Hanahan 团队(第一作者为曾启群等人)在 Science 期刊发表了题为:Aberrant hyperexpression of the RNA binding protein FMRP in tumors mediates immune evasion 的研究论文。。
该研究阐述了一个介导肿瘤免疫逃逸的新组分:脆性 X 染色体智力迟滞蛋白(Fragile X mental retardation protein,FMRP)。

对于这种由FMR1基因编码的蛋白,科学家们并不陌生。基因突变或表观遗传学修饰可以导致FMR1基因出现一系列三核苷酸重复,阻扰FMRP蛋白的合成,进而引发一种遗传性智力障碍疾病:脆性X综合征(Fragile X syndrome,FXS)。
除了导致这种罕见病,作为RNA结合蛋白,FMRP在大脑的神经细胞上高表达,可以结合并调控数百种神经细胞相关的mRNA的翻译以及稳定性。近年来,有些研究还发现了FMRP与癌症的潜在关联:高表达FMRP的肿瘤细胞扩散性、转移性更强,但FMRP在癌症中的具体功能以及机制尚不明朗。
Hanahan教授课题组的前期工作提示,FMRP蛋白参与N-甲基-D-天门冬胺酸受体(NMDAR)信号通路,促进胰腺癌的侵袭性生长。
在这项最新研究中,研究团队首先检验了FMRP在不同肿瘤中的表达情况。他们发现,FMRP在人或小鼠的胰腺癌、结肠癌、三阴性乳腺等肿瘤组织异常高表达,而在对应的正常组织不表达或者低表达。这与人类蛋白质图谱(Human Protein Atlas)的独立研究结果一致。进一步的分析表明,FMRP的异常高表达不是由FMR1基因突变或者扩增引起的;而原癌基因Myc的激活是导致FMRP在肿瘤中高表达的原因之一。
FMRP作为维系神经系统正常功能的关键蛋白,却在各种肿瘤组织中异常高表达。它们在肿瘤进展中究竟起到了怎样的作用?
研究团队利用CRISPR-Cas9技术敲除了数种小鼠肿瘤细胞中的FMR1基因,构建了FMRP敲除的肿瘤细胞,之后分别将野生型(WT)或FMRP敲除(FMRP-KO)的肿瘤细胞注射至小鼠体内。
他们发现,在免疫正常的小鼠体内,FMRP敲除可以极其显著地抑制原位瘤和肺转移瘤的生长,延长小鼠的总体生存期,而在缺乏T细胞以及B细胞的免疫缺陷鼠中则没有效果。对免疫正常小鼠的进一步分析显示,FMRP敲除肿瘤被大量杀伤性CD8 T细胞浸润,而WT肿瘤基本上没有被CD8 T细胞浸润,因此,FMRP的缺失可能诱发了抗肿瘤的适应性免疫。
进一步去除FMRP敲除小鼠的T细胞后,肿瘤生长基本恢复到WT肿瘤水平,这表明T细胞是抑制FMRP敲除肿瘤生长的关键性免疫细胞。
FMRP敲除是如何诱发抗肿瘤免疫的?作者发现,关键在于肿瘤微环境的变化。相比于WT肿瘤,FMRP敲除肿瘤中的淋巴细胞,尤其是杀伤性的效应CD8 T细胞增多,而调节性T细胞大幅减少。
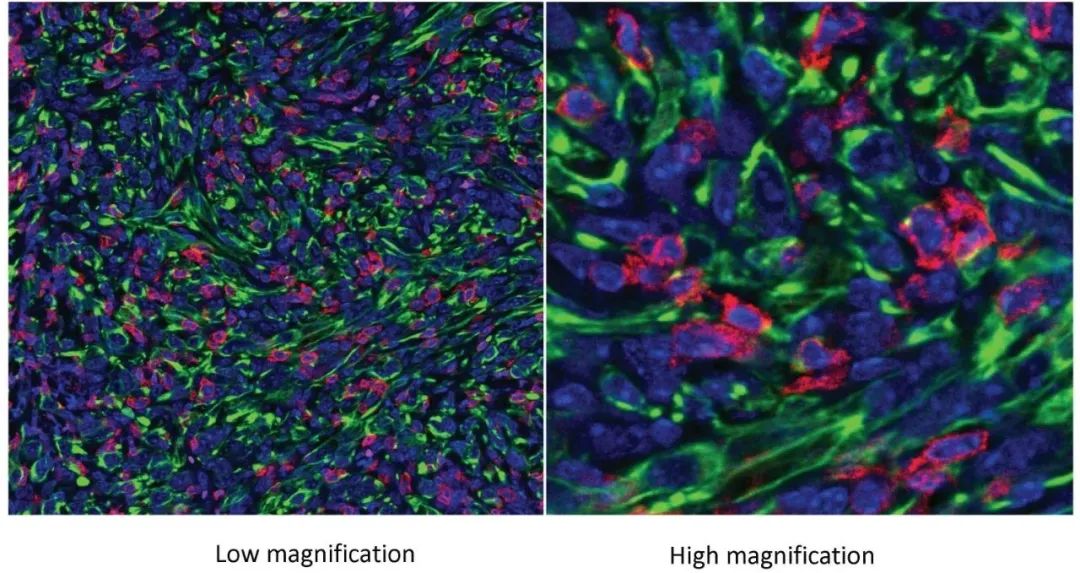
杀伤性CD8 T细胞(红色)浸润FMRP缺失的肿瘤细胞(绿色)(图片来源:Jeremy Guillot)
进一步的研究揭示了FMRP敲除阻止肿瘤免疫逃逸的分子机制。总体而言,FMRP敲除的作用可以分为两方面:提升促炎因子的表达,以及降低免疫抑制因子的表达。两者共同诱导促免疫反应的肿瘤微环境。
具体而言,在提升促炎因子方面,FMRP敲除直接促进肿瘤细胞分泌促炎因子CCL7,并且间接促进巨噬细胞表达促炎因子CCL9、CXCL9 和CXCL10,从而招募更多杀伤性CD8 T浸润、杀死肿瘤细胞。
而对于降低免疫抑制因子,作者发现FMRP敲除一方面降低了免疫抑制因子——细胞因子白细胞介素33(IL-33)的表达,从而减少了调节性T细胞浸润肿瘤;另一方面使得蛋白S(Pros1)、外泌体的表达下降,抑制肿瘤内巨噬细胞M1-M2极化反应。这两类变化均能激活淋巴细胞的抗肿瘤活性。
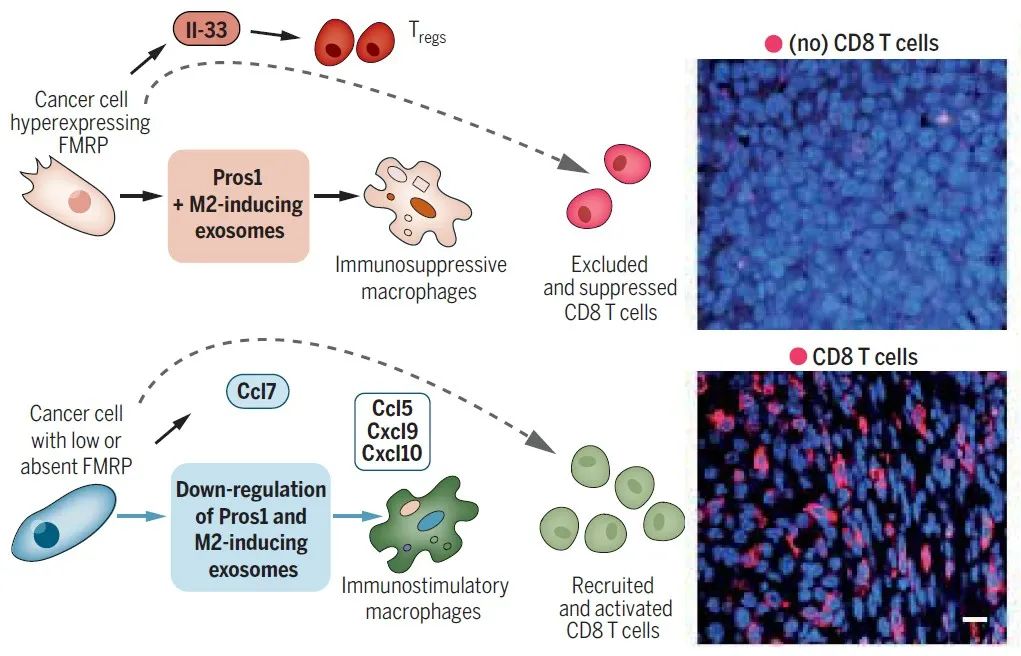
FMRP高表达时,CD8 T细胞耗竭、被清除(上图);FMRP不表达或低表达则会招募、激活CD8 T细胞(下图)
相反,对于WT肿瘤,FMRP的异常高表达促进了免疫抑制因子IL33、蛋白S、外泌体的表达,招募大量调节性T细胞以及免疫抑制性的巨噬细胞,使得肿瘤微环境处于免疫抑制状态,导致CD8 T细胞的耗竭和清除。
综上所述,该研究发现FMRP结合各种免疫基因相关mRNA并调控其蛋白表达,是一个全局掌控肿瘤免疫反应的关键蛋白。在进一步的基因signature分析中,作者发现该FMRP signature 在数种人肿瘤数据库中与患者预后,以及CD8 T细胞浸润显著相关,预示着FMRP介导的肿瘤免疫逃逸极具临床意义。
该论文的通讯作者Douglas Hanahan教授曾担任瑞士癌症研究实验中心主任,与Robert Weinberg教授合作或者独自撰写了3篇肿瘤领域奠基巨作, “Hallmarks of cancer” (2000), “Hallmarks of cancer: the next generation” (2011), “Hallmarks of cancer: new dimensions” (2022)。

曾启群博士
基于这项重要发现,Hanahan教授于2020年12月成立生物初创公司Opna Bio SA,致力于寻找靶向FMRP 蛋白的小分子抑制剂,用于肿瘤免疫治疗。该论文的第一作者第一位为中国学者曾启群, 其研究兴趣为神经与肿瘤之间的相互作用;曾发现乳腺癌-大脑转移细胞通过与神经细胞形成类似突触结构,促进脑转移肿瘤生长,于2019年9月18号以封面文章的形式发表在 Nature 期刊。
论文链接:
https://www.science.org/doi/10.1126/science.abl7207
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




