- 12
- +1
器官再生?揭示细菌促进肝脏生长的新机制
原创 转网 转化医学网 收录于合集 #行业动态 474个
细菌诱导的重编程重新激活肝脏祖细胞,并上调生长、代谢和抗衰老相关标志物,衰老和致瘤基因的变化最小,提示细菌劫持稳态再生途径以促进新生器官发生。这可能促进内源性途径的解开,这些途径有效且安全地重新参与肝器官生长,具有广泛的治疗意义,包括器官再生和恢复活力。

本文为转化医学网原创,转载请注明出处
作者:kope
尽管体外模型、类器官和微型器官在药物发现、疾病建模和再生医学方面具有潜力,他们无法模拟所需的器官级复杂性。因此,尽管这些方法取得了进展,目前没有策略能够在慢性或衰老相关的人类疾病中实现成人器官的有效再生或恢复活力。
肝细胞的再生恢复
01
肝脏是研究生长和再生的典范器官。与其他实体器官不同,成人肝脏有能力在组织丢失后恢复先前的质量,恢复体内平衡。在人类慢性肝病中,反复的炎症损伤和实质细胞死亡刺激肝细胞团的再生恢复,同时产生伤口愈合反应。肝硬化仍有一些再生能力,但不可能完全恢复,移植仍然是唯一的治疗方法。慢性损伤与恶性肿瘤风险增加有关,恶性肿瘤在慢性病毒感染中最高。再生受损肝脏的内源性途径仍然描述不佳,理解失败导致缺乏促再生的临床策略。随着肝脏疾病的健康和经济负担迅速增加,缺乏这种修复策略至关重要。此外,随着生理功能的下降,老化的肝脏更容易患上进行性疾病。维持健康的肝脏对于健康的衰老至关重要,因为它直接或间接地影响其他器官功能,但没有恢复活力的策略来减缓或逆转衰老过程中肝功能的下降。
目前对肝脏再生的研究使用需要肝细胞损失来刺激再生的短寿命啮齿动物模型,当达到原始肝脏大小时,这将停止。一旦达到先前的器官大小,停止反应的机制是未知的。绕过这种上限限制的能力将允许在没有先前肝损伤的情况下研究再生。了解如何从头参与再生机制将提供范式转变的成人器官再生和复兴临床策略,可以减少或取代移植,但目前还没有这样的体内模型可用。

麻风分枝杆菌
02
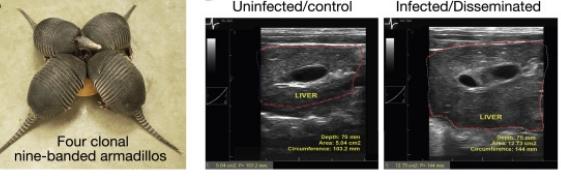
近日,英国爱丁堡大学的研究人员发现麻风病细菌可以对细胞进行重新编程,以增加成年动物肝脏的大小,而不会造成损伤、纤维化或肿瘤,还可以帮助受损的肝脏再生,从而减少移植的需要。在该研究中,研究人员用麻风病细菌感染了57只犰狳,这种动物是麻风病细菌的天然宿主,并将其肝脏与未感染犰狳的肝脏以及经发现具有抗感染性的肝脏进行了比较。
报告了一种天然的体内模型,即ML感染的九带犰狳在器官水平上用于哺乳动物成年肝脏生长,而没有先前的损伤。细菌诱导的体内部分重编程显著增加了肝脏大小,具有持续的功能和结构,但在感染的建立阶段没有损伤、纤维化或肿瘤发生。定义了哪些细胞类型促进该器官的生长,并表明健康的肝小叶数量,而不是大小,肝细胞质量以及血管和胆管系统的比例扩张。显示ML已经适应了动态部分重编程,再生和发育/胎儿机制的证据,以促进从头肝脏器官发生,同时保持组织保护和肿瘤预防策略。
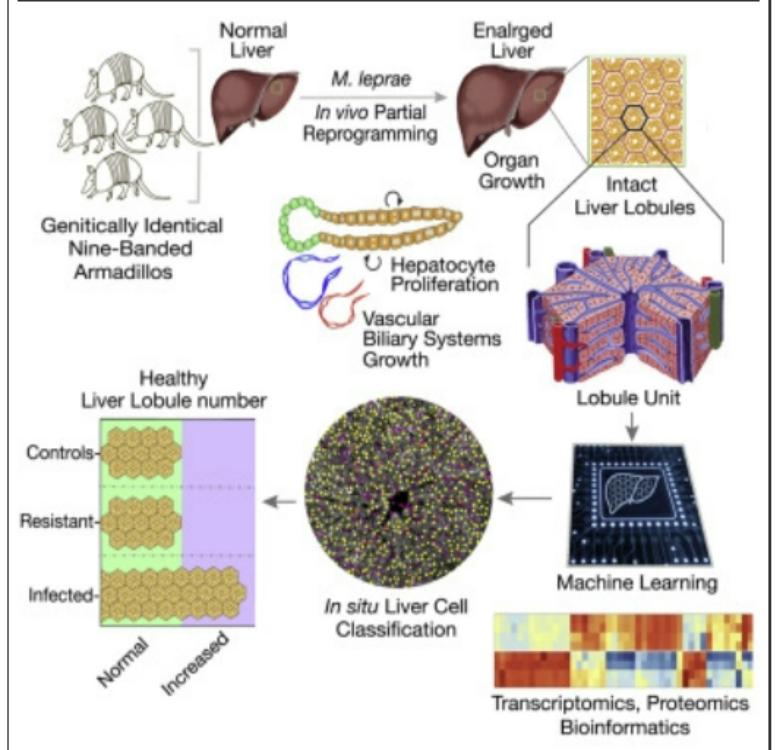
概念上的进步
03
肝病每年造成200万人死亡。没有任何使用实验室培养干细胞治疗肝硬化的试验产生任何许可的疗法。使用注射干细胞开发实体器官疾病疗法的失败表明,应该探索反映器官生长和再生复杂性的替代策略。2D、3D和体外模型已经显示出进展,但它们在大型实体器官中的临床应用有限。此外,目前对体内肝脏再生的知识来源于短暂的啮齿动物损伤或肝切除术模型。
利用肝脏的再生和代谢特性,代谢丰富的肝脏微环境补偿已知的ML代谢缺陷,在受感染的肝脏中诱导许多代谢基因。由于观察到的体内健康肝脏生长不受其他细菌物种或药物治疗的刺激,因此肝脏生长似乎是ML特异性的。维持扩增的功能性肝脏允许宿主细胞依赖性细胞内细菌在感染的建立阶段繁殖。鉴于免疫细胞的存在不同,但没有组织学细胞死亡或纤维化,人们可以推测ML对宿主反应的适应部分涉及调节先天免疫细胞活性,防止组织损伤。
这种进化改进的体内模型可能会促进我们对天然再生机制的理解,并确定如何从头参与以允许新的器官再生策略用于潜在的临床用途,这是一个概念上的进步,在再生医学中具有更广泛的影响。
参考资料:
https://doi.org/10.1016/j.xcrm.2022.100820
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。







- 习近平参加首都义务植树活动
- 世贸组织就美国关税政策发表声明
- 加拿大:对美汽车加征25%关税

- 亿达中国:已履行复牌指引,申请4月7日复牌
- 美股三大期指延续弱势,纳斯达克100指数期货跌幅扩大至1%

- 京剧伴奏乐器中的主要弦乐器,又名胡琴的是
- 连接地中海与红海,属于亚非分界线一部分的人工水道是

- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司