- +1
Nature子刊:胆固醇转运蛋白通过调控自噬和线粒体,影响癌症发展
原创 生物世界 生物世界

撰文丨丁芃芃
编辑丨王多鱼
排版丨水成文
自噬(autophagy)指损伤的细胞器、长寿命蛋白、病原体等胞质成分,被运输到溶酶体降解的过程。根据降解底物被运送到溶酶体的方式,自噬又可分为巨自噬、微自噬和分子伴侣介导的自噬。通常所说的自噬指的是巨自噬。巨自噬过程中,首先在待降解底物周围形成双层膜,形成自噬体(autophagosome),与内体或溶酶体融合,形成自噬溶酶体(autolysosome),之后在膜表面的V-ATPase质子泵作用下,腔内pH值下降以激活相关水解酶,降解底物。
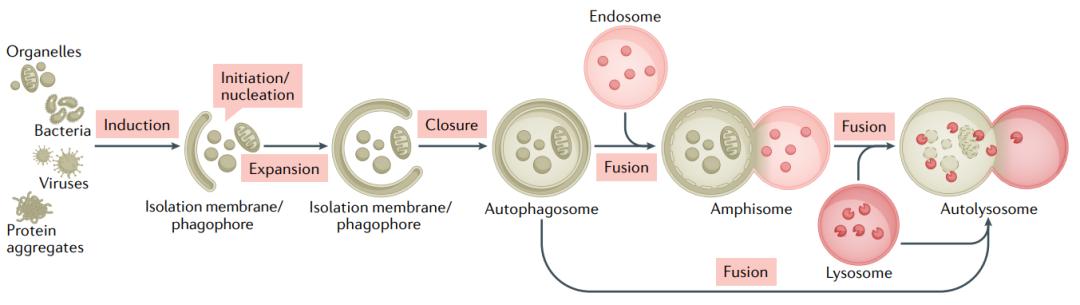
图片来自参考文献1
作为自噬启动的关键环节,自噬体膜的形成有十分重要的意义。在自噬启动早期,自噬体膜缺少跨膜蛋白,其调节可能主要依靠膜相关蛋白和膜本身的脂质成分。既往研究表明,自噬体膜缺少胆固醇成分,且短期清除细胞中的胆固醇成分或长期提高胆固醇水平都能提高自噬水平。这些发现都提示:胆固醇代谢可能是影响自噬水平的关键因素之一。
GRAMD蛋白家族是一类通过特征性GRAM结构域与细胞膜上的磷脂酰丝氨酸结合的蛋白。已知的GRAMD蛋白包括了GRAMD1A、GRAMD1B、GRAMD1C、GRAMD2、GRAMD3,其中只有GRAMD1A、GRAMD1B、GRAMD1C这3种蛋白可以通过自身的固醇结合结构域VASt,介导胆固醇从细胞膜到内质网的运输。有研究发现,GRAMD1A是自噬启动的必要条件。由于GRAMD蛋白常常形成异源复合物共同发挥作用,因此,其他GRAMD蛋白很有可能通过调节胞内胆固醇代谢,调控细胞自噬水平。
近日,奥斯陆大学的 Anne Simonsen 教授团队在 Nature Communications 期刊发表了题为:The cholesterol transport protein GRAMD1C regulates autophagy initiation and mitochondrial bioenergetics 的研究论文。
这项研究发现,不论是通过药物降低细胞膜胆固醇含量,还是干扰GRAMD1C蛋白的表达,均能够提高U2OS细胞(人骨肉瘤细胞)的自噬水平。此外,敲低/敲除GRAMD1C蛋白可提高线粒体胆固醇含量,上调线粒体ATP偶联的有氧呼吸速率。最后,该研究团队通过对TCGA数据库分析,揭示了GRAMD蛋白家族与肾透明细胞癌预后之间存在关系。这项研究启示我们从细胞胆固醇代谢角度,思考细胞自噬及癌症预后背后的分子机制。

营养缺乏时,细胞往往会启动自噬,为生命活动提供必需的氨基酸等原料。甲基β环糊精(MBCD)可以快速清除细胞膜成分中的胆固醇,阿托伐他汀(ATV)则可以长效清除细胞中的胆固醇。研究团队通过EBSS培养基诱导自噬,他们发现:MBCD/ATV处理后,细胞的自噬水平上升,自噬起始复合物表达量增加。此外,他们还发现MBCD/ATV处理可以使自噬在mTOR抑制信号未降解的情况下提前发生,并上调自噬早期弯曲的富集有PtdIns(3) P的自噬膜表达水平,提示胆固醇消除可以影响自噬的动态发生过程。
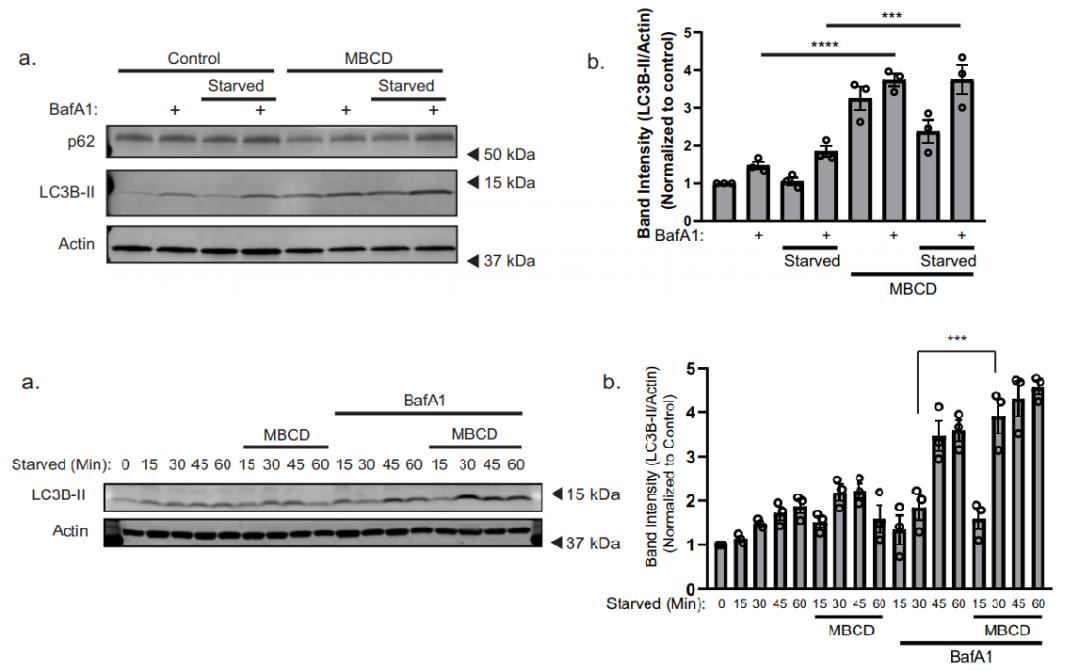
MBCD处理后,自噬水平提高,发生提前
在此基础上,研究团队使用siRNA及CRISPR/Cas9技术,研究细胞中胆固醇转运蛋白在自噬发生过程中的作用。他们发现,敲低/敲除GRAMD1C蛋白,可以上调细胞的自噬水平:增加自噬溶酶体数目,提高14C缬氨酸培养后上清液的放射性、增加LC3-Ⅱ自噬流、提高自噬起始复合物表达量、上调弯曲自噬膜表达水平。
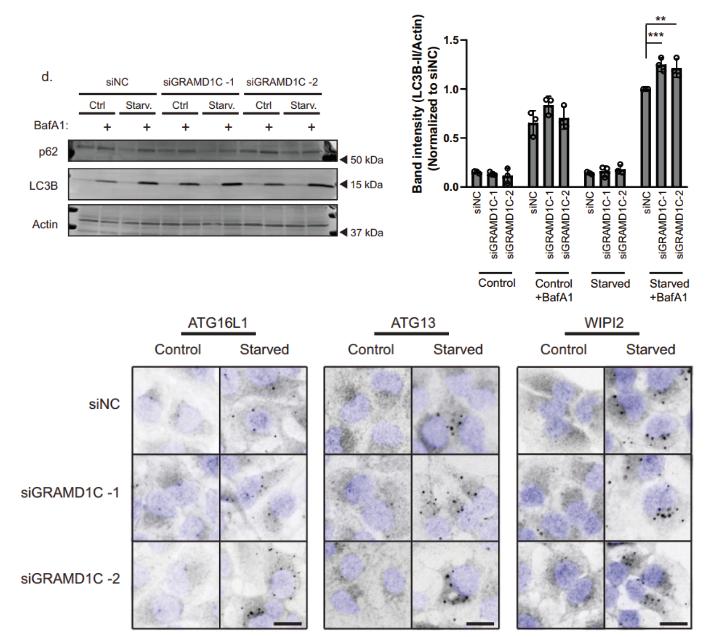
敲低GRAMD1C蛋白后,自噬水平升高,自噬起始复合物表达量升高
综上所述,研究团队认为,GRAMD1C蛋白可以通过抑制自噬早期的弯曲自噬膜形成,抑制自噬起始复合物的招募,从而抑制自噬体的生物合成。
由于既往研究证明自噬体形成部位往往与ER-Mit接触位点相关,且酵母细胞中GRAM的同源序列Lam6往往在囊泡接触位点高表达,因此,研究团队进一步探究GRAMD1C蛋白是否在ER-Mit接触位点表达,甚至影响线粒体功能。
Anne Simonsen团队发现,GRAMD1C蛋白不仅与ER、Mit在空间上存在共表达,而且与线粒体外膜蛋白TOMM70A、RHOT2等存在互作。在此基础上,研究团队敲低/敲除GRAMD1C蛋白,发现在不影响线粒体形态、线粒体蛋白质组、线粒体膜电位以及细胞ROS水平的前提下,线粒体的胆固醇含量升高,内质网的胆固醇含量降低,且线粒体ATP偶联的有氧呼吸速率升高。提示了GRAMD1C蛋白可介导内质网与线粒体的胆固醇运输,抑制线粒体生物能。
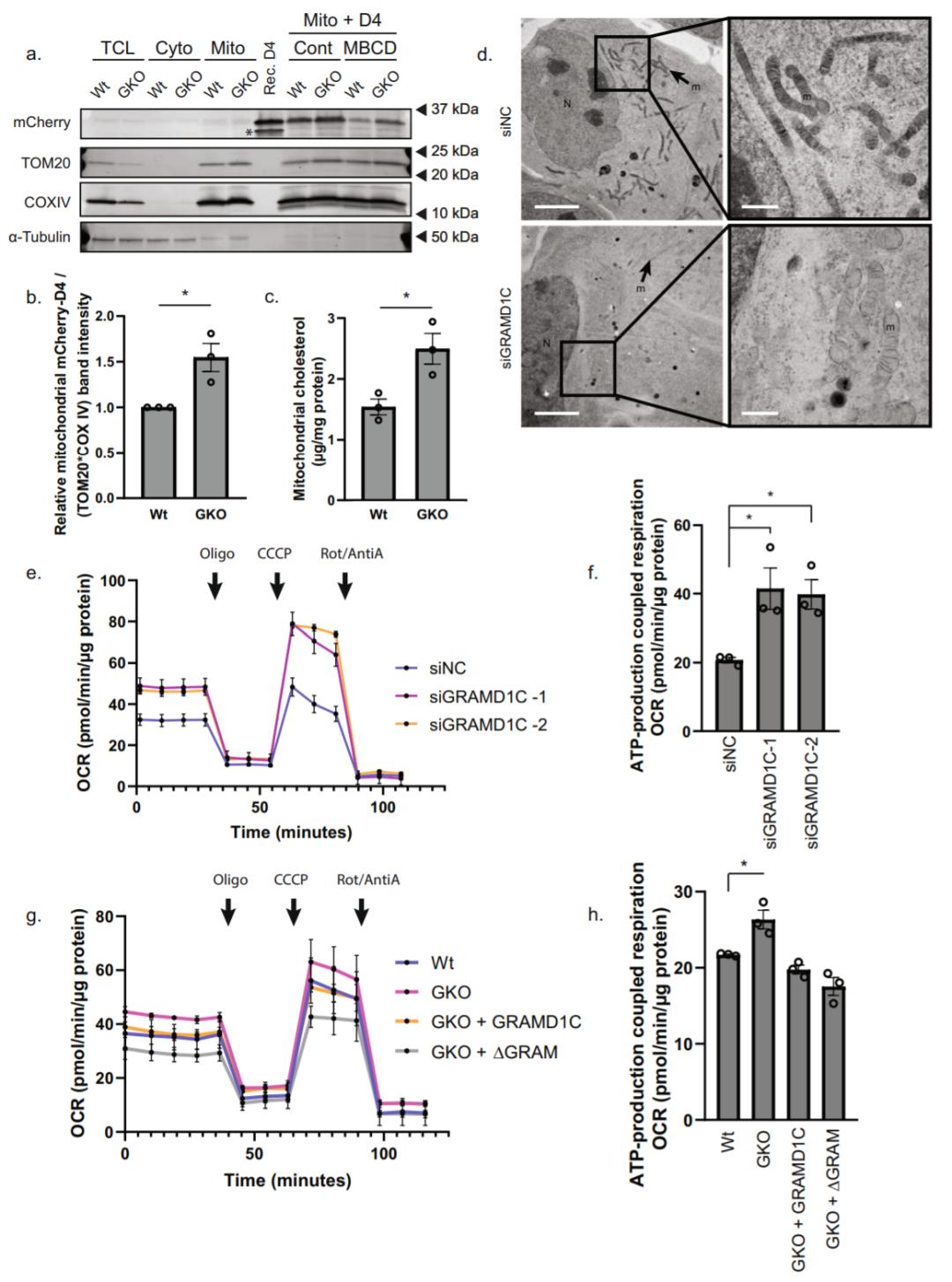
敲低/敲除GRAMD1C蛋白,线粒体胆固醇含量升高,有氧呼吸速率提高
最后,研究团队以肾透明细胞癌疾病模型,通过TCGA数据库分析,揭示了GRAMD1C、GRAMD2B是肾癌预后的不利因素,GRAMD1A、GRAMD1B是肾癌预后的有利因素。
Anne Simonsen 教授表示,该项研究发现:下调细胞膜胆固醇有利于自噬起始蛋白招募,促进自噬体的合成;GRAMD1C蛋白可能通过调控细胞膜与内质网、内质网与线粒体之间的的胆固醇运输,抑制自噬体合成,下调线粒体生物能。这些新的发现与癌细胞的聚落、增殖、迁移以及患者预后也有一定联系,下一步的研究应当聚焦于生物膜系统的胆固醇调控在自噬发生与癌症进展当中的作用。
论文链接:
https://www.nature.com/articles/s41580-021-00392-4
https://www.nature.com/articles/s41467-022-33933-2
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




