- +1
与阿尔茨海默病相关的是特定蛋白质的减少而非淀粉样斑块
辛辛那提大学的一项新研究支持了一个假设,即阿尔茨海默病是由特定蛋白质水平的下降引起的,这与最近受到质疑的流行理论相反。

辛辛纳提大学10月4日消息
由辛辛那提大学(University of Cincinnati,UC)医学博士 Alberto Espay 和医学博士 Andrea Sturchio 领导的研究人员与瑞典卡罗林斯卡学院(Karolinska Institute,KI)合作,近日在《阿尔茨海默病杂志》(Journal of Alzheimer's Disease)上发表了这项研究[1]。


研究于2022年9月16日在线发表在《Journal of Alzheimer's Disease》(最新影响因子:4.160)杂志上
质疑主导假说
这项研究的重点是一种叫做 β-淀粉样蛋白的蛋白质。这种蛋白质通常以可溶性的形式在大脑中执行功能,这意味着它可溶于水,但有时它会硬化成块状,称为淀粉样斑块。
100 多年来,阿尔茨海默病研究领域的传统观点认为,阿尔茨海默病是由大脑中淀粉样斑块的积聚引起的。但 Espay 和他的同事们假设,斑块只是大脑中可溶性 β-淀粉样蛋白水平下降的结果。这些水平的下降是因为正常蛋白质在生物、代谢或感染压力的情况下,会转化为异常的淀粉样斑块。
辛辛纳提大学医学院神经病学教授、辛辛纳提大学加德纳神经科学研究所(UC Gardner Neuroscience Institute)James J. and Joan A. Gardner 帕金森病和运动障碍家庭中心主任和讲席教授、辛辛纳提大学卫生系统(UC Health)医生 Espay 说:“矛盾的是,随着年龄的增长,我们中的很多人的大脑中会积累斑块,但很少有人会发展成失智症。然而,这些斑块仍然是我们关注的中心,因为它关系到生物标志物的发展和治疗策略。”

Alberto Espay 教授
Sturchio 指出,多年来,许多研究和临床试验都旨在减少大脑中的淀粉样斑块,有些已经减少了斑块,但直到 9 月 27 日,渤健(Biogen)和卫材(Eisai)宣布一项阳性试验(药物 Lecanemab)之前,没有一项能减缓阿尔茨海默病的进展。更重要的是,为了支持他们的假设,在一些降低可溶性 β-淀粉样蛋白水平的临床试验中,患者出现了临床结果恶化的情况。
“我认为这可能是最好的证据,证明降低蛋白质的可溶性形式的水平可能是有毒的,”该报告的第一作者、辛辛纳提大学医学院的兼职研究讲师 Sturchio 说。“这样做之后,患者的情况变得更糟了。”

Andrea Sturchio 博士
研究成果
该团队此前的研究[2]发现,不管大脑中斑块的积聚情况如何,可溶性 β-淀粉样蛋白水平高的人认知能力正常,而可溶性 β-淀粉样蛋白水平低的人更有可能出现认知障碍。

此前的研究于2021年6月28日发表在
《柳叶刀》子刊
《eClinicalMedicine》杂志上
在目前的研究中,研究团队分析了一组突变(APP、PSEN1 或 PSEN2)患者的 β-淀粉样蛋白水平,这些突变预示着大脑中淀粉样斑块的过度表达,这被认为使他们更有可能发展为阿尔茨海默病。
Sturchio 说:“对淀粉样蛋白毒性假说最有力的支持之一就是基于这些突变。我们研究这一人群,因为它提供了最重要的数据。”
即使在这组被认为患阿尔茨海默病风险最高的患者中,研究人员也发现了与对普通人群的研究相似的结果。
Espay 说:“我们发现,那些在大脑中已经积累了斑块的人,如果能够产生高水平的可溶性 β-淀粉样蛋白,那么在三年的时间里,发展成失智症的风险就会更低。”
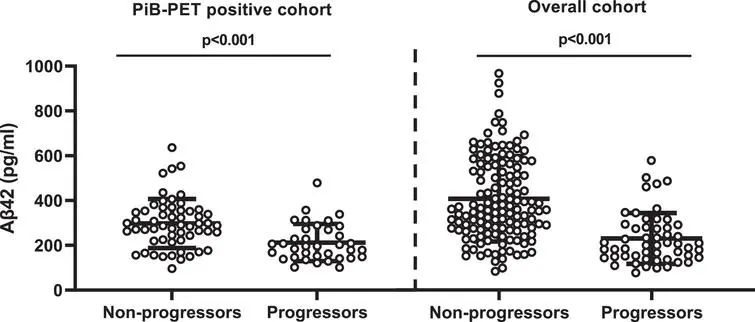
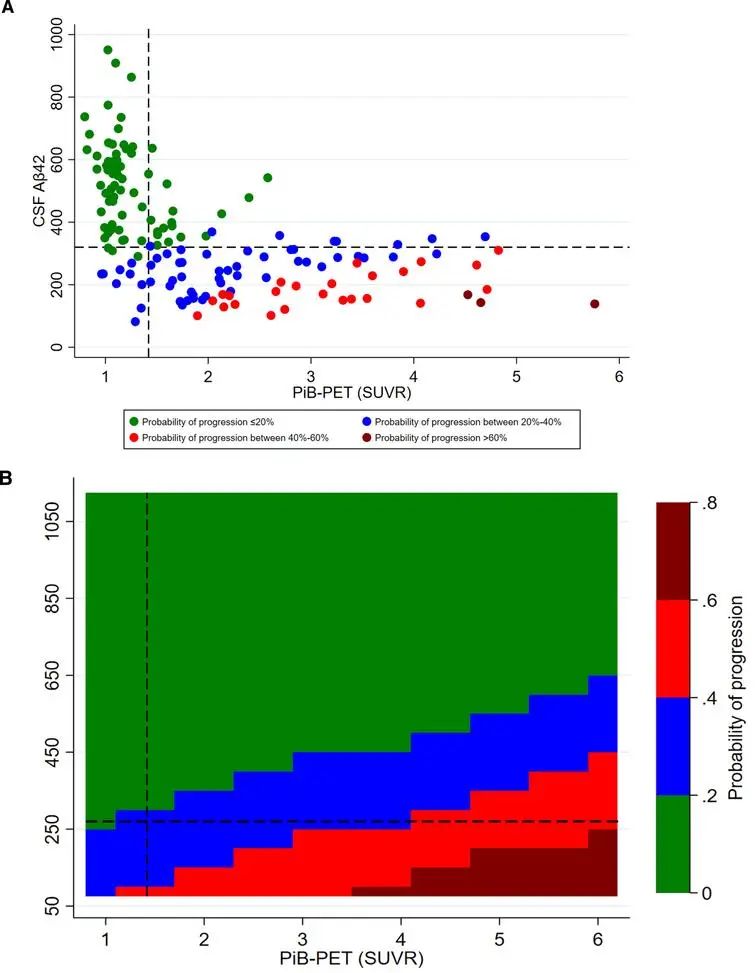
研究发现,当大脑中可溶性 β-淀粉样蛋白的基线水平高于每毫升 270 pg(1皮克等于一万亿分之一克)时,无论大脑中淀粉样蛋白斑块的数量如何,人们都可以保持认知正常。
Espay 说:“如果你能跳出我们长期以来形成的偏见,那么神经退行性过程是由我们失去的东西可溶性 β-淀粉样蛋白引起的,而不是由我们获得的东西淀粉样斑块引起的,这就太符合逻辑了。退化是一个失去的过程,而我们失去的反而更加重要。”
下一个步骤
Sturchio 说,研究正在向前推进,以研究增加大脑中可溶性 β-淀粉样蛋白的水平是否对阿尔茨海默病患者是一种有益的治疗方法。
Espay 说,重要的是要确保引入大脑的蛋白质水平升高后不会转化为淀粉样斑块,因为正常功能需要这种蛋白质的可溶性版本在大脑中产生影响。
在更大的范围内,研究人员表示,他们相信类似的导致神经退行性变的假设可以应用于其他疾病,包括帕金森病和克雅氏病(CJD),这些领域的研究也在继续。
例如,在帕金森病中,大脑中一种名为 α-突触核蛋白(α-synuclein)的正常可溶性蛋白质会硬化成一种名为路易体的沉积物。研究人员假设,帕金森病不是由大脑中的路易体聚集引起的,而是由正常的可溶性 α-突触核蛋白水平下降引起的。

Espay 说:“我们主张,在所有退行性疾病中,更有意义的可能是正常蛋白质的损失,而不是可测量的异常蛋白质的部分。随着这些疾病的发展,大脑持续萎缩,其净效应是蛋白质的损失而不是增加。”
Espay 说,他设想未来有两种治疗神经退行性疾病的方法:救援医疗(rescue medicine)和精准医疗(precision medicine)。
救援医疗看起来就像目前的工作,研究提高可溶性淀粉样蛋白等关键蛋白质的水平是否会带来更好的结果。
Espay 说:“有趣的是,最近被报道为有益的抗淀粉样蛋白药物 Lecanemab,除了减少淀粉样蛋白斑块外,还能实现大多数其他抗淀粉样蛋白治疗无法实现的效果:它能提高可溶性 β-淀粉样蛋白的水平。”
或者,精准医疗需要更深入地了解是什么导致可溶性 β-淀粉样蛋白的水平下降,是病毒、毒素、纳米颗粒还是生物或遗传过程。如果根本原因得到了解决,蛋白质的水平就不需要提高,因为不会发生从可溶性正常蛋白质到淀粉样斑块的转化。
Espay 表示,精准医疗将考虑到没有两个患者是相似的这一事实,提供更个性化的治疗。研究人员正在通过“辛辛那提队列生物标志物计划”(Cincinnati Cohort Biomarker Program,CCBP)在精准医疗方面取得进展,该项目旨在按生物亚型划分神经退行性疾病,以便将基于生物标志物的治疗方法与最有可能从中受益的治疗方法相匹配。

Espay 说:“辛辛那提队列生物标志物计划致力于在这个十年中部署精准医疗的第一个成功。通过识别帕金森病和阿尔茨海默病的生物、传染性和毒性亚型,我们将有特定的治疗方法,可以减缓这些受影响的患者的进展。”


创立于1819年的辛辛纳提大学
参考文献
Source:University of Cincinnati
Study: Decreased proteins, not amyloid plaques, tied to Alzheimer’s disease
References:
[1].Sturchio A, Dwivedi AK, Malm T, Wood MJA, Cilia R, Sharma JS, Hill EJ, Schneider LS, Graff-Radford NR, Mori H, Nübling G, El Andaloussi S, Svenningsson P, Ezzat K, Espay AJ; Dominantly Inherited Alzheimer Consortia (DIAN). High Soluble Amyloid-β42 Predicts Normal Cognition in Amyloid-Positive Individuals with Alzheimer's Disease-Causing Mutations. J Alzheimers Dis. 2022 Sep 16. doi: 10.3233/JAD-220808. Epub ahead of print. PMID: 36120786.
[2]. Sturchio A, Dwivedi AK, Young CB, Malm T, Marsili L, Sharma JS, Mahajan A, Hill EJ, Andaloussi SE, Poston KL, Manfredsson FP, Schneider LS, Ezzat K, Espay AJ. High cerebrospinal amyloid-β 42 is associated with normal cognition in individuals with brain amyloidosis. EClinicalMedicine. 2021 Jun 28;38:100988. doi: 10.1016/j.eclinm.2021.100988. PMID: 34505023; PMCID: PMC8413261.
免责声明
本公众号上的医疗信息仅作为信息资源提供与分享,不用于或依赖于任何诊断或治疗目的。此信息不应替代专业诊断或治疗。在做出任何医疗决定或有关特定医疗状况的指导之前,请咨询你的医生。
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




