- +1
南京大学张辰宇团队开发体内自组装的siRNA递送系统

结肠炎为累及回肠、直肠、结肠的一种特发性肠道炎症性疾病,包括溃疡性结肠炎(Ulcerative Colitis,UC)和克罗恩病(Chron’s Disease,CD)。结肠炎在全球的发病率不断攀升,严重威胁着人类健康。结肠炎的发病受遗传因素、免疫失调、微生物群失衡和环境因素影响,由于其发病机制复杂、发病过程漫长、涉及因素众多,因此在治疗过程中仅仅控制一个致病基因或作用于一个药物靶点,往往得不到很好的治疗效果,导致彻底治愈结肠炎仍然十分困难。
针对结肠炎这一复杂疾病的病理特征,目前亟待开发多靶点的联合治疗策略,从而对结肠炎致病因素的多个环节加以控制,达到协同治疗的目的。
在RNA干扰(RNAi)技术中,由于siRNA设计简便灵活,理论上能够通过同一载体串联表达,实现多种siRNA的同时生成,进而一次性靶向抑制多个致病基因,并且彼此之间往往不会像传统联合治疗药物一样产生交叉作用。然而,siRNA的体内递送问题一直阻碍着RNA干扰技术的临床应用。如何让siRNA在体内稳定传输,能否找到一种安全、可靠、与机体高度兼容的递送载体,一直是RNA干扰技术临床转化应用的核心科学问题。
2022年9月28日,南京大学张辰宇、陈熹、张骑鹏团队在 Nature Communications 期刊发表了题为:In vivo self-assembled siRNA as a modality for combination therapy of ulcerative colitis 的论文,利用体内自组装siRNA的策略,避免了siRNA体内递送的瓶颈问题,从而在动物模型上实现了结肠炎的多靶点联合治疗。

具体而言,该技术利用合成生物学设计理念,通过向小鼠静脉注射可同时表达TNF-α siRNA、B7-1 siRNA和integrin α4 siRNA的合成生物学基因环路(以质粒DNA的形式),将小鼠的肝脏重构成可以产生和分泌siRNA的器官,继而利用机体自身的外泌体分泌和传输途径,实现siRNA在体内稳定、高效、安全的生产和传输。
利用该策略,研究团队成功实现了对结肠炎的多个靶基因(TNF-α、B7-1和integrin α4)的同时干预,在结肠炎动物模型上显示了卓越的协同治疗作用,且治疗效果优于单独靶向TNF-α的英夫利昔单抗。
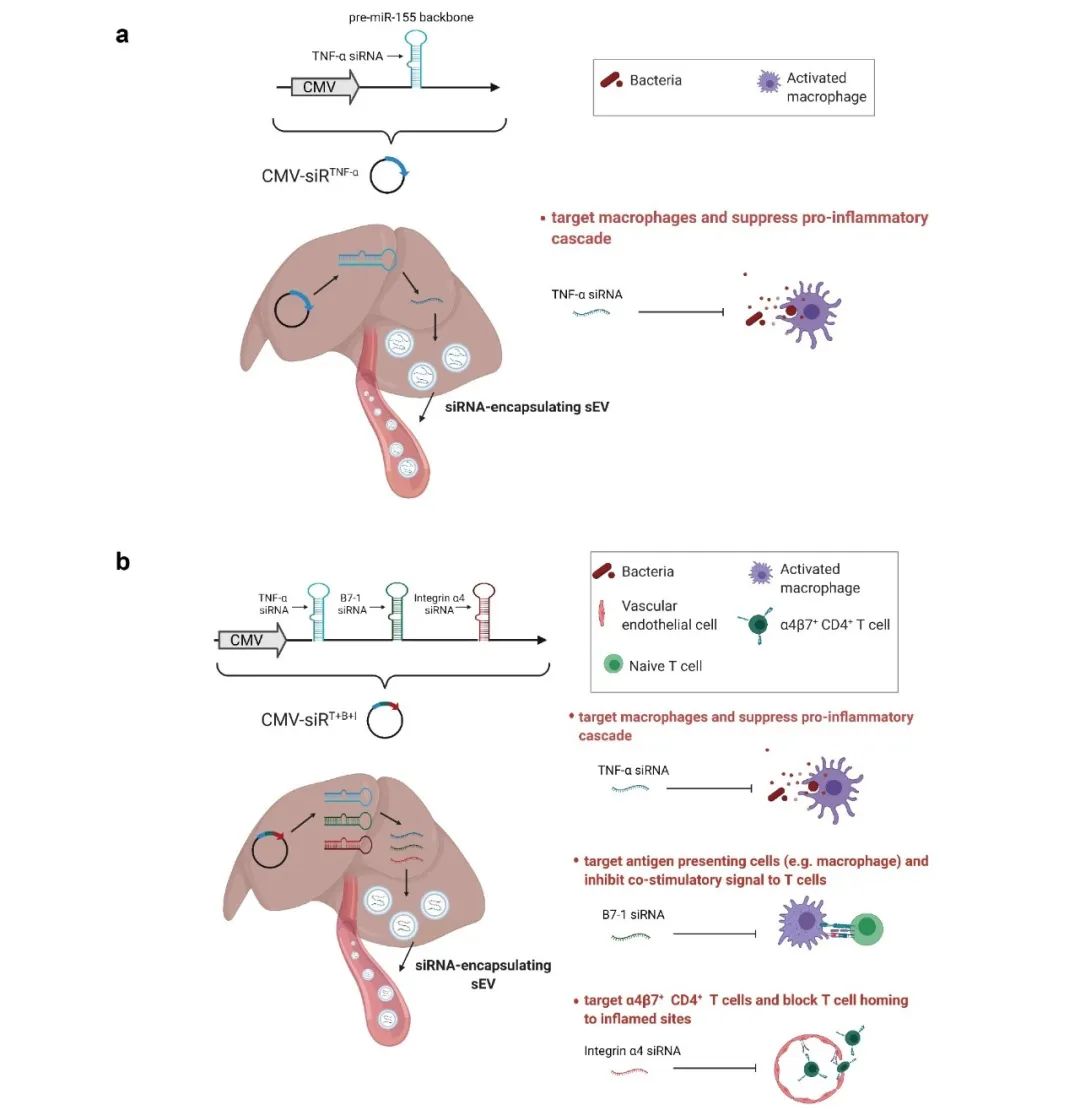
体内自组装siRNA,同时作用于多个靶点从而联合治疗结肠炎的模式图:CMV-siRT+B+I基因环路
该环路包含一个CMV启动子部分和一个siRNA串联表达框,这个串联表达框携带三个siRNA表达单元,可以同时驱动TNF-α siRNA、B7-1 siRNA和integrin α4 siRNA的转录;该基因环路通过尾静脉注射进入小鼠体内后,能被肝脏细胞吞噬,通过重编程宿主肝脏从而指导siRNA在肝脏的自动合成和向外泌体的自组装;进而,外泌体包裹的TNF-α siRNA通过外泌体内分泌循环,被递送至结肠巨噬细胞,通过抑制结肠巨噬细胞中TNF-α的表达,调控促炎反应以及调节免疫平衡;外泌体包裹的B7-1 siRNA能被抗原呈递细胞(APC)摄取,并抑制T细胞共刺激信号通路,促进T细胞耗竭;外泌体包裹的integrin α4 siRNA进入CD4 + T细胞后,能够通过抑制整合素的生成阻断T细胞归巢至炎症部位。
此外,为了探讨该组件实现长期治疗的可能性,研究团队优化了组件载体,利用AAV8-TBG(肝特异性表达的AAV亚型及肝特异性启动子)搭载核心元件,实现TNF-α siRNA、B7-1 siRNA 和integrin α4 siRNA 在肠炎动物体内的长期表达。在慢性结肠炎模型中,该AAV8-TBG系统能够实现一次注射,持续治疗并缓解症状。
这项研究是南京大学张辰宇团队近期发表的第三篇关于体内自组装siRNA的研究论文。
2021年3月29日,张辰宇/陈熹团队在 Cell Research 发表了题为:In vivo self-assembled small RNAs as a new generation of RNAi therapeutics 的封面论文【2】,首次提出并设计了一种可组合和可编程的基因环路,该环路能够重编程宿主肝脏,以指导siRNA在肝脏的自动合成和自组装进入外泌体,并通过外泌体的内分泌循环实现siRNA的体内递送,是这项技术的奠基性工作。
详情:

2021年12月,张辰宇/陈熹团队在 Brain 发表了题为:Therapeutic reversal of Huntington’s disease by in vivo self-assembled siRNAs 的封面论文【3】。通过构建靶向亨廷顿症致病基因mHTT的体内自组装siRNA,实现了对亨廷顿病动物模型的有效治疗。
详情:

而这项 Nature Communications 论文则建立了一种新型多靶点联合治疗方法,在结肠炎小鼠模型中诱导了多种siRNA的生成,以及自组装到外泌体中,实现了同时抑制多个免疫靶点,实现了对结肠炎的多基因联合治疗。
这项技术具有重要的理论意义和转化价值,它为结肠炎的联合治疗提供了可行且有前景的解决方案,同时也显示出了这一新型递送平台可在动态的体内环境中诱导可控的siRNA自组装和递送,并能够精确调控基因表达,从而使siRNA治疗免疫性疾病、癌症、代谢疾病、神经退行性疾病成为可能。
论文链接:
1.https://www.nature.com/articles/s41467-022-33436-0
2.https://www.nature.com/articles/s41422-021-00491-z
3.https://doi.org/10.1093/brain/awab354
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。




- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




