- +1
解读|肺癌“钻石”靶点第三代抑制剂国内获批,患者如何获益如何选?
“随着时代的不同,有些问题原来不重要的,变得越来越重要了。”广东省肺癌研究所名誉所长吴一龙教授所谈的是肺癌治疗的合理用药话题。
近日,吴一龙在接受澎湃新闻(www.thepaper.cn)等媒体采访时表示,以ALK阳性患者为例,“在十几年前,我们只有一个药,克唑替尼,那个时候我们需要谈合理用药吗?当然不需要,因为没得选择。但是到了今天,当我们有非常多药的时候就必须要来谈合理用药的问题了。”
ALK即间变性淋巴瘤激酶(Anaplastic Lymphoma Kinase,ALK),是一种受体酪氨酸激酶,与血液、间质和实体三大类型肿瘤相关。此前的研究显示,约3%-7%的非小细胞肺癌(NSCLC)患者体内肿瘤染色体EML4基因外显子与ALK基因外显子融合,形成EML4-ALK融合酪氨酸激酶,EML4-ALK融合变异体具有高度的致癌性,且ALK在多种肿瘤细胞中高表达。
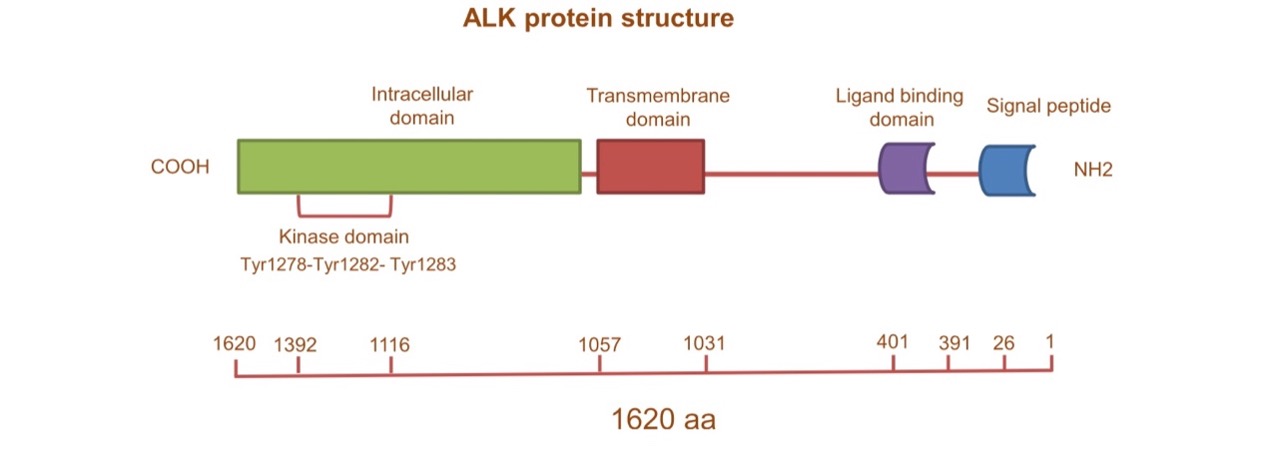
正因如此,ALK是一个极具吸引力的肺癌治疗靶点,也被称为肺癌的“钻石”靶点。“因为这个‘钻石’突变没有药的时候比其他的都恶性,但是有了药之后比其他的生存时间都要长。”吴一龙解释。
ALK阳性肺癌患者的“救星”于2011年问世。彼时,辉瑞公司(Pfizer)开发的第一代ALK抑制剂克唑替尼获美国食品和药品监督管理局(FDA)批准上市。7年之后,两次“升级”后的第三代ALK抑制剂也进入了市场。就在此前的4月底,辉瑞开发的全球首个第三代ALK抑制剂博瑞纳®(Lorbrena®,通用名:洛拉替尼片/Lorlatinib Tablets)获中国国家药品监督管理局批准,单药适用于间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。
“从科学性角度来讲,ALK抑制剂单药就已经可以显示非常好的效果。所以从治疗策略或者所有的指南、所有的证据也好,都会强调单药ALK抑制剂治疗ALK阳性患者。” 上海交通大学附属胸科医院、上海市肺部肿瘤临床医学中心主任陆舜教授在接受澎湃新闻(www.thepaper.cn)记者时如是表示。
第三代ALK抑制剂:无进展生存期已突破三年
在世界范围内,肺癌居恶性肿瘤死亡原因的首位。肺癌分为小细胞肺癌(约占所有肺癌的15%)和非小细胞肺癌。而在中国,肺癌也高居发病率和死亡率首位 ,其中ALK阳性晚期非小细胞肺癌患者平均年龄在52岁。
此外有数据显示:20-40%的ALK阳性晚期非小细胞肺癌患者在初诊时就已发生脑转移,且发生率随时间延长而升高,即使经过ALK抑制剂治疗,45-70%的患者也会出现脑部进展 ,对患者生存带来严峻挑战。
吴一龙认为,经过近二十年的探索,肺癌领域在两个科学观念的引导下产生了非常大的突破。
第一个就是循证医学,“循证医学的核心特点就是以临床试验为中心,以临床试验的数据来说话。所以,我们现在谈所有的治疗离不开数据,离不开临床试验。”第二则是精准医学,“精准医学跟循证医学不是矛盾的,而是相辅相成的。我们今天的精准医学核心是以分子生物学的改变来对肺癌进行仔细的分型,然后在分型的基础上指导我们的治疗,这叫做精准医学。”
上述提到的ALK分型,就是精准医学的一部分。ALK是一种受体酪氨酸激酶,属于胰岛素受体超家族,与白细胞酪氨酸激酶具有高度同源性。该基因位于人类染色体2p23段,编码1620个氨基酸的多肽,经过翻译后修饰,生成200- 220千道尔顿(kDa)的成熟ALK蛋白。ALK基因可激活多个细胞内信号通路,从而参与调节细胞生长、转化以及抗细胞凋亡的过程。
早在1994年,日本东京大学M Shiota等人发表论文报道,他们在间变性大细胞淋巴瘤AMS3细胞株中发现ALK融合基因。而到2007年,日本自治医科大学Manabu Soda等人在顶级学术期刊《自然》(Nature)发文,他们首次在日本的肺癌患者中发现ALK基因与EML4基因的融合,为晚期肿瘤的治疗提供了新的选择和方向。
辉瑞公司的克挫替尼拔得头筹。吴一龙提到,“克唑替尼当时给大家带来非常大的希望,因为用克唑替尼来治疗ALK融合,效果大大超过了过去唯一的治疗方案,也就是化疗,而毒副作用比起化疗大大减轻。”
然而,作为第一代ALK抑制剂,克挫替尼中位无疾病进展生存时间仅约11个月,“这个时候就产生一个问题,这就是我们称为医学上未被满足的(治疗需求)。为什么只有11个月?能不能更长?如果能更长的话,那这就是临床需要的。”
吴一龙表示,在克唑替尼之后更多的探索,就是希望能够把疾病控制住的时间拉得越长越好。第二代ALK抑制剂患者让患者能获得约34.8个月的无进展生存,“显然这是一个非常大的突破。”
目前,第三代ALK抑制剂也开始应用。辉瑞公司开发的洛拉替尼目前是全球唯一获批的三代ALK抑制剂,“首先它在化学结构上有一个比较独特的大环酰胺的结构,有了这个结构它的穿透力就会比较强,另外跟ALK的结合力也是比较强,在临床上显示比较好的效果。”陆舜解释道。
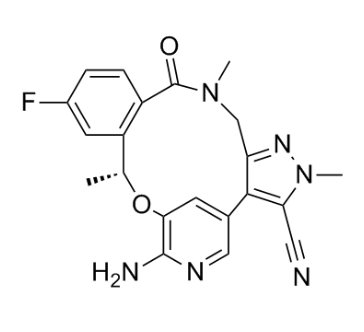
近期在美国癌症研究学会(AACR)公布的临床研究数据表明,洛拉替尼一线治疗ALK阳性非小细胞肺癌的无进展生存期(PFS)已突破三年,表现出前所未有的疾病无进展生存时间。“换另外一个角度来讲,洛拉替尼治疗之下患者的第三年的生存率可以达到63.5%,表现出了前所未有的疾病无进展生存时间。”吴一龙认为,这就是所谓临床未被满足的需求。
更为重要的是,洛拉替尼具还有着出色的血脑屏障穿透能力,无脑转移的患者接受其治疗能有效阻遏脑转移发生。而有脑转移的患者治疗后,颅内客观缓解率高达83.3%。
“这些数据得到了业界的高度关注,也为医生选择一线治疗方案提供了理论依据。”吴一龙表示。
陆舜也总结道,“这种效果可以提示说,一个药物控制就可以有非常长时间的生存,换句话说,把ALK阳性的病人真正意义上变成了一个慢性的疾病。”
新的探索:简化治疗、药物假期
随着洛拉替在国内的获批上市,中国ALK阳性非小细胞肺癌患者在临床用药上的可选择性进一步加大。
谈到实际临床上如何合理化选择用药方案,吴一龙提出四个原则,
一是,看药物疗效。一般的标准就是,现有的药物和过去的药物相比是否能够提高患者生存期4个月,如果能,就列入考虑范围,这也是合理用药最重要的维度。
二是,看药物副作用、安全性。聚焦患者是否可以接受药物的副作用,副作用是否可以处理。
三是,看是否需要长期用药。如果一个药物不用长期服用,用一段时间就可以控制病情,肯定比起长期用药要好得多。
四是,看费用的问题,包括医保覆盖、慈善补偿等措施。
吴一龙总结称,洛拉替尼在国内刚刚获批,目前还没有进入到医保,所以在目前的情况下,其个人认为,“如果从各项指标来讲,当然是推荐第三代,但是综合各种因素,现在基本是第二代、第三代并存。”
陆舜就这一问题表示,洛拉替尼在国内上市意味着,“中国ALK阳性的病人,不管是初治还是发生疾病进展的患者都可以用洛拉替尼,也都可以从洛拉替尼治疗中获益。”另一方面,“只要能够很好地解决支付性的问题,毫无疑问这个药物应该用在一线,因为这些病人获益更明显,所有的靶向药物治疗当中都证明了这一点。”
值得一提的是,随着近年来免疫治疗在癌症领域的异军突起,包括免疫疗法等在内的联合方案在临床上被不断探索,在ALK阳性患者身上也有着一些讨论。但吴一龙对澎湃新闻(www.thepaper.cn)记者表示,在其针对肺癌的治疗探索中,趋势是“化繁为简”。
吴一龙谈到学术界的两种治疗模式,“一种叫做强化治疗,通过很多手段把生存期延长到最高;另外一种是把治疗尽量简化,就是说在疗效相等或者相差不远的情况下,我们尽量地简化治疗。”
他认为,这两种治疗都有它存在的合理依据。然而,从个人角度来说,他更喜欢简化治疗。“因为治疗的手段越少、越单纯,病人的毒性会更低、耐受性会更好。”吴一龙从此前的研究联合治疗转变为现在的越来越简化,“能够用一个药的不用两个药,能够用两个药我不会用三个药,都是这样的原则。”
吴一龙提到,甚至现在还有一个非常主要的研究方向,即“药物假期”。“就是在探讨什么时候可以不用药,我们已经在做这样的事情。”
他认为这是在对肺癌深刻了解之后的必然趋势,“特别是当我们的病人生存越来越长的时候,简化治疗、减少毒性,这就是一个我们必须要面对的问题。”
就洛拉替尼来说,“在目前的情况下, ALK阳性患者第三年生存率可以达到63.5%,我觉得已经非常了不起。”
当然对于剩下的近三成的患者,吴一龙认为仍然需要去进一步探索原因,但并不是为了这部分患者就对所有患者都进行联合治疗,“这不符合精准治疗的方向。我们要探寻的原因是,哪些因素影响到了这个效果不好,对于存在这些因素的患者,来探讨联合治疗。”
然而,究竟采取何种策略的联合治疗,“这就需要我们做工作,这回到循证医学的精髓,我们要通过临床试验来证实加上另外一个药是不是好,这条路就更长了。”
吴一龙还着重指出一点,就当下大家最关心的问题,即ALK融合的病人能不能跟最热的免疫治疗联合起来?“到今天为止,我们获得的证据非常清楚地表明,ALK融合的病人用免疫治疗,效果不是很理想,毒副作用远远超过了我们可能得到的好处。”
陆舜也对澎湃新闻(www.thepaper.cn)记者谈到,“如果一个好的靶向治疗的药物单药就能显示非常卓越的效果,我们是不建议联合的,联合只会增加毒性。但是如果这个药物疗效不是太好,就有可能做一些联合,这是总体的思路。”
而他也同样信奉,“less is more,就是越少的药物实际上越能体现这个药物的效果。”陆舜明确提到,“我们是主张对ALK抑制剂单药用,而不太会主张加联合治疗。”





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




