- +1
不幸得了癌症,120万1针的CAR-T疗法能买回一条命?
原创 腾讯医典
“120万元打一针,就能让癌细胞消失”。
前不久,很多人被这个消息刷屏了。
新闻中的这种疗法就是一种CAR-T治疗。
2021年6月22日,中国批准上市了首个CAR-T细胞疗法药物(肿瘤免疫治疗的一种方法)。最近该注射液的官方定价发布了,正如之前猜想的——120万元一针。
按这个价格,说是“天价药”,一点也不过分。
这让很多人陷入思考:如果不幸得了癌症,CAR-T疗法需要120万,值不值?
如果是你,你会怎么选?
这不是一个简单的问题。
生命无价,但是不幸得病之后,治病却要花钱。
不同人对这个问题的答案不一样。
但在回答之前,明确这几个问题很关键。
CAR-T治疗究竟能做什么?对哪些肿瘤患者有效果?有哪些副作用?

如今癌症治疗进入精准医疗时代,CAR-T治疗目前为止是最有效的方法之一。
CAR-T治疗是一种免疫疗法。所谓免疫治疗,就是增加体内免疫细胞的杀伤力,免疫细胞装上定向导弹,直接瞄准肿瘤细胞,精准击杀[1]。
我们知道,肿瘤细胞是一种人体细胞的“叛徒”。是人体正常细胞经过一系列基因突变,变成不受控制、无限生长的变异细胞。不过,这还不是肿瘤细胞最厉害的超能力。
逃避免疫系统的“监视”,才是肿瘤细胞最厉害的能力之一。人的身体时时刻刻在产生这样的细胞,绝大多数被免疫系统追杀。癌细胞可以通过伪装和抑制免疫细胞功能,令自己逃脱免疫系统的追杀,堂而皇之地在免疫系统眼皮下生长繁殖。
免疫治疗就是专门针对这种超能力的。
这个过程是这样:
1. 医院采血,将免疫T细胞从血液中分离出来,剩余血液重新输回患者体内;
2. 将分离的T细胞送到实验室或工厂;
3. 修饰改造:通过基因工程,给T细胞装上特异性识别肿瘤细胞表面分子的“瞄准器”,修饰改造后的T体细胞被称为CAR-T细胞,具有超强的识别和杀伤肿瘤的功能;
4. 扩增:通过修饰改造的CAR-T细胞需在体外培养到一定数量,才能达到治疗要求,因此,需要将CAR-T细胞在体外培养进行大量扩增;
5. 回输:将CAR-T细胞注射到病人身体里,CAR-T细胞直接识别肿瘤细胞表面的抗原,从而杀伤肿瘤细胞。
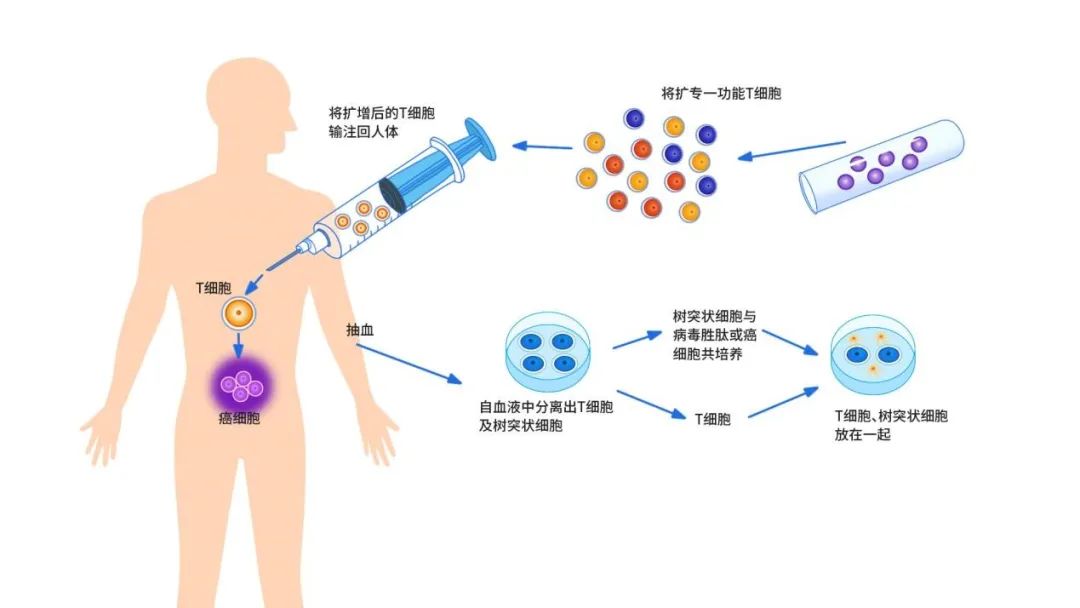
(点击查看大图)
治疗过程既简单又短暂,从手臂中抽出血液后,经过改造,又重新输送回体内。
这比化疗和放疗的周期更短,患者受到的伤害更少,CAR-T治疗通常只需静脉输注1~2次,无需反复给药。
这种人工改造后的免疫细胞,是一种打击癌症的“特种部队”,能够杀伤特定的肿瘤细胞。
还能够在人体内自我复制扩增,源源不断地补充“伤亡减员”,在患者体内长期驻扎、免疫监视。
这种疗法更精准,相比于传统的化疗药物产生的副作用,CAR-T细胞能够避免对正常细胞造成误杀,副作用较小。

免疫细胞治疗的效果虽好,但新闻中的宣传却夸大了。
总结下来就是,免疫细胞治疗有效,但适应证有限,不是对所有的癌症都适用。
CAR-T细胞治疗目前只在部分血液肿瘤有所突破,在患者人数占比更多的实体瘤领域,还有待进一步研究和优化[2]。
而根据2020年国际癌症研究机构的数据,中国癌症发病率前10的癌种,都是实体瘤:肺癌、乳腺癌、胃癌、结直肠癌、肝癌、食管癌、宫颈癌、甲状腺癌、子宫癌、前列腺癌[3],也就是说,大多数中国癌症患者,目前还用不了这种新治疗方法。
但对于血液肿瘤来说,以白血病、淋巴瘤为例,传统的一线治疗手段是化疗、放疗、靶向治疗等。
化疗有很多缺点。患者会出现诸多不良反应(如呕吐、脱发等),很痛苦。
在难治、复发类血液肿瘤的治疗领域,传统一线疗法复发率高。
根据世界卫生组织国际癌症研究机构发布的数据,2020年全世界血液肿瘤新发病例约128万,死亡病例数65万;
血液肿瘤一线治疗后复发率较高,例如:弥漫性大B细胞淋巴瘤患者,一线治疗缓解后,约30%~40%会出现耐药或复发[3]。
复发之后,意味着原先的疗法失效了,再次治疗难度更大,最终影响生存率。
相比之下,CAR-T疗法适应人群广泛,有可能会延长患者的生存时间。
已经有几例CAR-T细胞疗法的成功经验被报道出来了。
2019年7月,陈阿姨确诊弥漫性大B细胞淋巴瘤(DLBCL),经过治疗病情有所缓解,但2021年复发后疗效欠佳。
2021年6月22日,陈阿姨在上海交通大学医学院附属瑞金医院接受了阿基仑赛注射液(一种CATR-T疗法)治疗,经过两个月的治疗,陈阿姨被评估为“症状完全缓解”,身体状态也越来越好,获准出院[4]。
本次获批的CAR-T产品,根据2017年发布的临床试验结果:
1年随访结果:最佳总缓解率为82%,完全缓解率达到了54%。
2年随访结果:中位随访27.1个月,仍有39%的受试者持续缓解,其中37%的受试者持续完全缓解。
4年随访结果:中位随访时间51.1月,4年总生存率为44%,中位生存时间(50%的患者可以活过这个时间)达到25.8月[5]。
要知道,进入这个临床试验的患者,都是“复发或难治性”淋巴瘤患者,常规的放化疗很难取得这么好的疗效。
我国2018年新增癌症人数380万,血液瘤约占9.9%,其中急性淋巴细胞白血病中适合二线以下疗法的患者约20%,也就是大约7万名患者,可以从这种CAR-T细胞治疗中获益。
但CAR-T细胞治疗并不是完美的,目前是个体化疗法,生产工艺不成熟,成本高昂;而且治疗后仍有部分患者出现复发。
此外,CAR-T细胞治疗也有副作用。一项研究表明,几乎所有接受CD19靶向CAR-T 细胞治疗的患者都出现了不同程度的毒副作用,比如细胞因子释放综合征等,患者会出现发热,严重可导致全身炎症反应、低血压、缺氧和器官衰竭等[6]。

截至2022年1月,国内仅有2款CAR-T细胞药物获批上市,定价分别为120万和129万人民币。
目前,全球共有7款CAR-T细胞药物获批上市,获批的适应证也都局限在急性淋巴细胞白血病、多发性骨髓瘤、霍奇金淋巴瘤等血液肿瘤领域[7],这些疗法在中国,都是百万花费以上的。
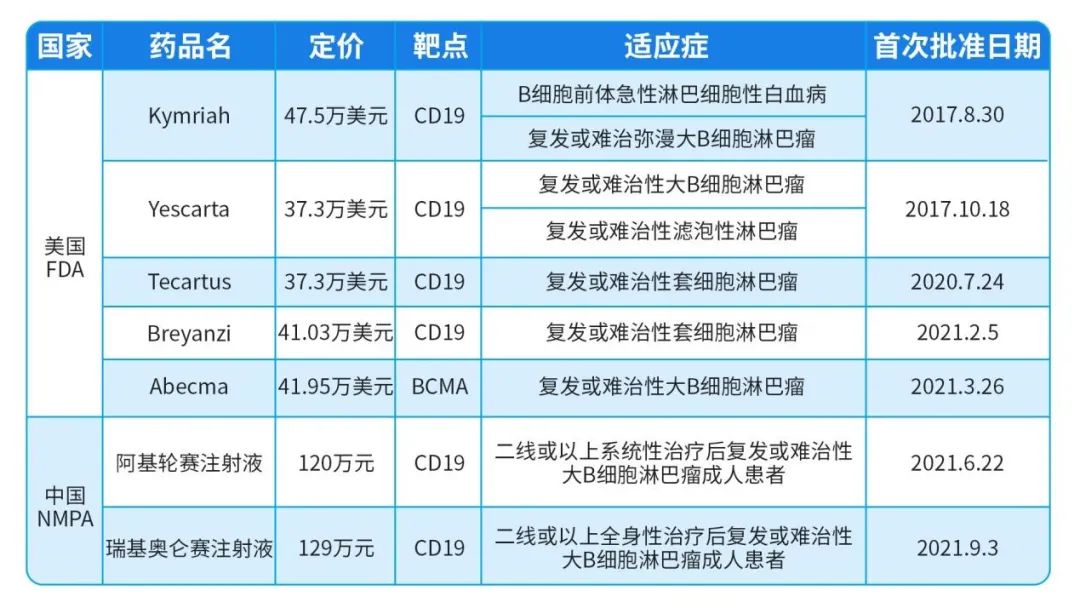
(点击查看大图)
都可谓“天价”。
CAR-T细胞治疗为什么这么贵?
CAR-T的高昂价格背后是一个复杂问题,涉及医学、药物经济学、经济学、医疗产业发展等多方面的。
第一,CAR-T治疗是需要个性化定制的,是个体化用药,无法实现规模化量产,每一批产品均耗费高昂成本、2~4周的培养制备周期。
第二,整个治疗过程很复杂,涉及的技术环节很多,质控要求严格,全球范围目前均未形成一个成熟、标准化的生产工艺流程,很多环节依赖人工操作,失败率较高。
第三,在产业方面,行业处于发展初期,原料、设备等产业链上下游资源体系尚不成熟,也导致了成本升高。
在药物研发的角度,在研制这个药物的过程中,药企付出了高昂的研发成本,获批适应证较少,对应的患者市场相对较为狭窄,药企需要合适的价格收回成本以及盈利。
如果强制性让厂家低价售卖,长此以往,药厂以及研究人员也不会再有动力去研究新技术,从长远来看这对患者并不是好事。
除此之外,还有医保、专利授权等等,很多因素都会影响药价。
未来,CAR-T细胞治疗的药价会下降吗?
我们相信,会的。
目前,我们已经看到多方的努力,比如药企给出的优惠方案、商业保险、越来越多CAR-T细胞治疗的药物出来,市场充分竞争会让药价下降。
复杂的世界里,很多时候没有一个简单的答案。
但是,我们要始终心怀希望,毕竟无数努力都在默默进行。
而对于大多数人来说,“不得癌症”依旧是最好的防癌方法。
审稿专家:崔伟
广东省人民医院肿瘤中心介入治疗科医学博士主治医师
参考文献
[1]Joseph Oved, David Barrett, David Teachey. Cellular therapy: Immune-related complications. Immunol Rev. 2019 Jul;290(1):114-126.
[2]Morello A, Sadelain M, et al. Mesothelin-Targeted CARs: Driving T Cells to Solid Tumors. Cancer Discov. 2016 Feb;6(2):133-46.
[3]https://www.bjcancer.org/Html/News/Articles/12768.html
[4]https://m.thepaper.cn/newsDetail_forward_14265156
[5]https://clinicaltrials.gov/ct2/results?cond=CAR-T
[6]朱婧涵,梁远征,王亮.CAR-T细胞治疗面临的挑战及解决思路[J].中国癌症防治杂志,2021,13(06):594-601.
[7]亿欧智库. 2021中国CAR-T行业研究报告.
https://www.iyiou.com/research/20211223951
作者:罗天明、张小乙
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




