- +1
古药新用:二千多年抗菌药硝酸银
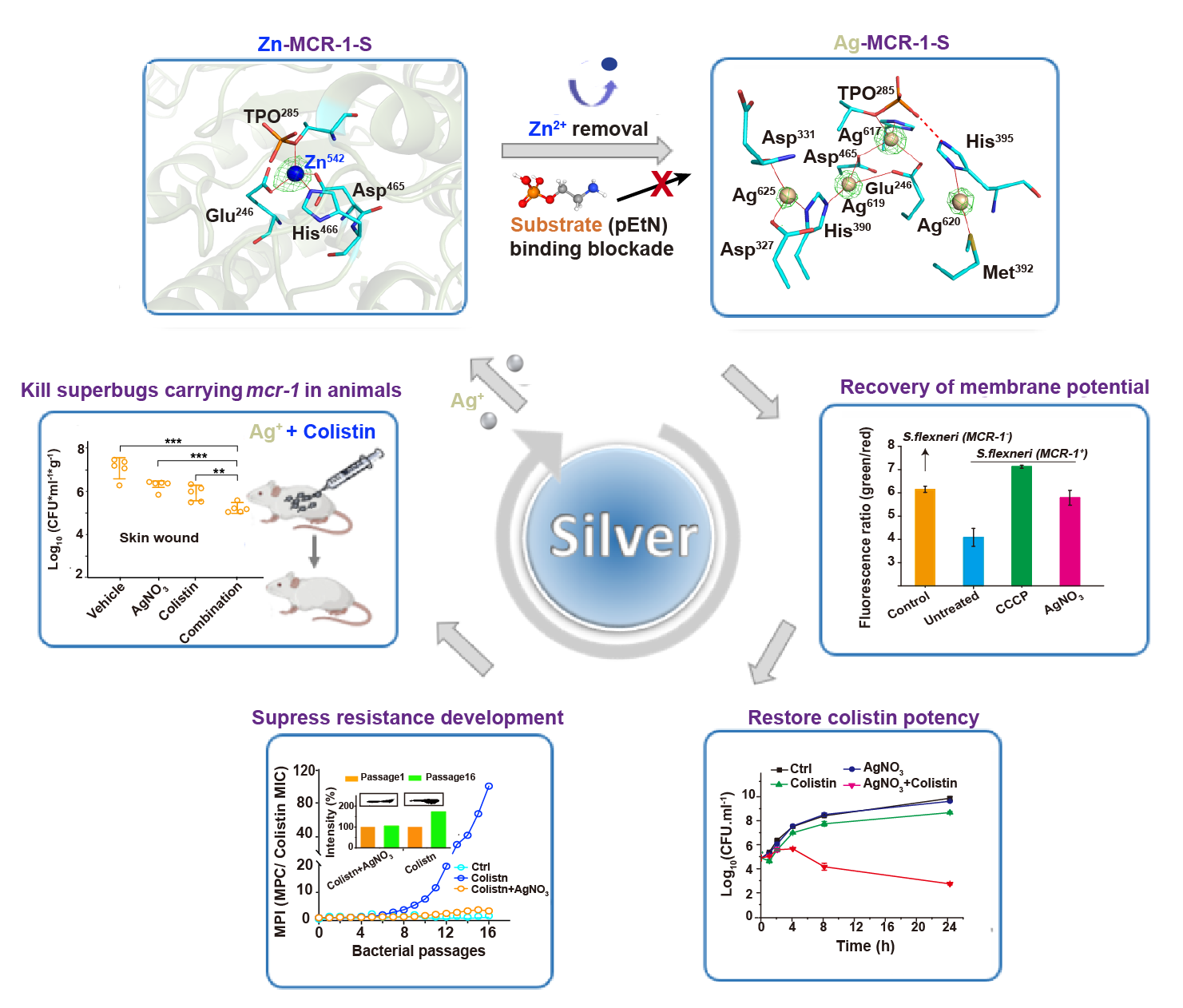
银可在体内外粘菌素对携带mcr基因的病原体重新敏感。 (左上)MCR-1-S酶活性位点口袋的卡通图,其中辅因子 Zn2+ 显示为蓝色球体。 (右上)位于Ag-MCR-1-S活性位点中的新型四核银核心的模拟图。图中Ag+ 显示为小麦色球体,它们通过配位键(红色实线)或氢键(红色虚线)桥接在一个狭窄的口袋中。 (右中) Ag+ 通过取代 MCR-1-S 中的 Zn2+ 并抑制底物 (磷酸乙醇胺,pEtN) 与MCR-1-S 酶的结合导致酶活性丧失,这可通过已被恢复的膜电位所反映出来。 (右下)用不同组合的药物处理携带有抗性基因mcr-1 的病原菌MCR-1-J53后,病菌的实时生长曲线。 (左中)使用携带有mcr-1的肺炎克雷伯菌 9607感染 Balb/c 小鼠皮肤。小鼠接受不同组合的药物治疗 7 天后,皮肤脓肿区域的细菌量。 (左下)单独用亚抑制浓度的多粘菌素或用多粘菌素和AgNO3 组合疗法对病菌MCR-1-J53进行连续16代的传代处理,病菌的耐药性发展曲线。内插图展示了在接受不同药物处理后,病菌中MCR-1 抗性蛋白酶的标准化表达水平。
(原新闻稿已于3月17日发布)
具有抗药性的超级细菌一直对人类健康构成重大威胁。目前,粘菌素(Colistin)被视为抗生素中的「最后一道防线」,可对抗沙门氏菌、绿脓杆菌、克雷伯氏肺炎菌、大肠杆菌、志贺氏菌和不动杆菌等具广泛耐药性的致命性细菌感染。然而,携带粘菌素抗性基因(mcr)的超级细菌于2015首次被发现,严重影响粘菌素的治疗功效。
针对此后抗生素时代的严峻临床挑战,科学家开始研究,利用复方抗生素和抗生素抗性消除剂(antibiotic-resistance breaker,ARB)联合疗法,透过激活具耐药性细菌重新对抗生素敏感并减低其抗药性,为治疗多重耐药细菌感染开辟出路。
香港大学(港大)化学系和微生物学系的研究团队,发现一种古抗菌药物 — 硝酸银 (AgNO3),可令这些耐药细菌对粘菌素重新敏感。硝酸银 (AgNO3) 抗菌药物已有超过二千年历史,以往多用作抑制外部感染,团队发现这药物可恢复粘菌素对一系列携带抗性基因的病原体的效力。
研究结果刚于国际科学期刊《美国国家科学院院刊》(Proceedings of the National Academy of Sciences of the United States of America, PNAS) 上发表。
研究团队由理学院化学系讲座教授、叶志成范港喜基金教授(生物无机化学)孙红哲教授,与李嘉诚医学院微生物学系、港大余家乐感染中心主任何柏良博士领导。
今次发现是一项有关抗菌素耐药性研究(注一)的延伸,团队于2020年曾发现抗风湿剂金诺芬可作为双重抑制剂,使多重耐药菌对粘菌素和β-内酰胺类抗生素恢复敏感性,该项目发现已于《自然通讯》发表。
「考虑到硝酸银作为古老的抗菌药物应用于外部感染的安全历史,我们认为它可以与金诺芬相互补充,用以治疗由携带粘菌素抗性基因的多重耐药超级细菌所引起的感染,为克服后抗生素时代的抗菌素耐药性危机带来新希望。」领导团队的孙红哲教授说。
研究背景
抗菌素耐药性是指当滥用或错用抗菌剂时,细菌会出现变异以逐渐适应抗菌剂,进而导致抗菌剂失去抑制和杀灭细菌的效力。抗菌素耐药性现已成为公共卫生最大的挑战之一。根据世界卫生组织的数据显示,2021年全球耐药菌感染的人数较上年增长9%;其工作报告亦指出,预计到了2050年,耐药菌总感染人数可能破千万,甚至将超过目前死于癌症的人数。
在目前疫情肆虐的特殊背景下,不当使用抗生素而导致抗菌素耐药性的问题有恶化趋势。香港卫生署曾指出,有研究发现高达71%的2019冠状病毒病患者曾接受抗生素治疗,而当中只有4%有受到细菌感染(注二)。
作为一种多黏菌素类多肽抗生素,粘菌素被认为是对抗广泛耐药革兰氏阴性菌感染(包括沙门氏菌、绿脓杆菌、克雷伯氏肺炎菌、大肠杆菌、志贺氏菌和不动杆菌等感染)的最后一道防线。不幸的是,科学家在 2015 年首次发现了可移动的粘菌素抗性基因1(mcr-1)。由于粘菌素抗性基因的快速变异,其他相关家族的抗性基因也陆续被发现,并发展出各自的亚型。这些可移动的耐药性基因进一步通过细菌菌株和物种间的水平基因转移迅速交叉传播,进而导致多种耐药超级细菌的出现。正如世界卫生组织(WHO)总干事谭德塞(Tedros Adhanom Ghebreyesus) 博士所言,更多的证据显示世界正迅速地失去这些至关重要的抗菌药物,情况令人担忧。事实上,亦有临床发现这些由「超级细菌」所引起的常见感染可能很快就会变得无药可治,这将严重危及公共卫生系统,使患者毫无治疗选择。
主要发现
研究发现,硝酸银中包含银纳米颗粒(Silver nanoparticles)在内的银 (Ag+),可以恢复粘菌素对携带抗性基因的细菌的能力,重新达致抗菌功效。团队透过X射线晶体学(利用X射线来研究晶体中电子密度的分布情况)观察到,银可通过取代抗性蛋白酶活性位点中的Zn2+(Zn2+正是促成抗药性的关键),以及在抗性蛋白酶MCR-1-S的活性位点中形成「四银簇(四核银核心)」,一个能有效抑制抗性蛋白酶活性的化学结构,最终可导致抗性蛋白酶失去功能。
研究表明,银能有效地减缓高水平耐药性的发展,并能够降低菌株的变异频率。而小鼠皮肤感染模型亦印证,由硝酸银和粘菌素组成的联合疗法,在缓解皮肤病变坏死和减少细菌载量方面的确非常有效。总而言之,联合治疗无论在体内及体外的效果皆良好,无疑为克服后抗生素时代的抗菌素耐药性危机带来新希望。
关于研究团队
该研究由港大化学系叶志成范港喜基金教授孙红哲所领导的团队进行,同属化学系的章琪博士及王润铭博士为本文的共同第一作者。其他参与这项研究的港大成员包括博士后研究员刘春娇博士(李嘉诚医学院微生物学系)、研究助理教授Mohamad Koohi-Moghadam(牙医学院)、博士后研究员王海波博士(理学院化学系)、港大余家乐感染中心主任(李嘉诚医学院微生物学系)何柏良博士和研究助理教授李洪艳博士(理学院化学系)。华东师范大学化学与分子工程系副教授汪旻稷博士也为研究作出了重要贡献。研究工作得到香港研究资助局、健康与医学研究基金和香港大学的支持。
关于孙红哲教授
孙红哲教授是港大叶志成范港喜基金教授(生物无机化学)及化学系讲座教授。他的研究重点包括金属蛋白、药物化学(抗菌剂的发现)和生物化学。孙教授在克服对超级细菌的抗菌素耐药性、开发抗冠状病毒药物和金属生物学等领域发表了一系列广受认可的工作。
更多有关孙教授的资料,可参看以下连结:https://www.bioinorg-chem.hku.hk/
参看研究论文,可登入此连结:https://www.pnas.org/doi/full/10.1073/pnas.2119417119
注一:(2020年新闻稿)港大发现抗风湿金属药物能复活已失效「最后防线」抗生素 有望解决多重耐药超级细菌感染的难题:
https://www.scifac.hku.hk/press/release/press-release-antirheumatic-metallodrug
注二:抗菌素耐药性 - 常見问题:
https://www.chp.gov.hk/files/pdf/amr_faqs_tc.pdf
(资料来源:卫生署卫生防护中心)
图片下载及说明:https://www.scifac.hku.hk/press
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




