- +1
【科学普及】CRISPR:重新设计生命
原创 李荣宇 细胞世界
基因支配着生命体的一生,但我们人类作为基因的最高智慧体,却在探索和学习中获得了改变基因的能力。
2020年的10月7日,诺贝尔化学奖授予两位对CRSIPR/Cas9基因编辑技术做出卓越贡献的女科学家——法国马克斯·普朗克生物感染研究所的微生物学家埃马纽埃尔·沙尔庞捷(Emmanuelle Charpentier)和美国加利福尼亚大学伯克利分校的化学家詹妮弗·杜德纳(Jennifer Doudna)。虽然CRISPR问世不足10年,但各界一致认为它必将对农业、医学和基础科研领域产生革命性影响,包括但不限于动植物的育种与优化、人类抵抗疾疾的方式以及生物研究模型的迅速构建。
01 什么是CRISPR
与大多数分子生物学研究的起源一样,CRISPR最先是上世纪90年代初在大肠杆菌中被偶然发现的。
CRISPR是Clustered Regularly Interspaced Short Palindromic Repeats的英文缩写,字面意思是“成簇的规律间隔的短回文重复序列”。尽管读起来既长且拗口,但这个名字包含了CRISPR作为一段DNA序列中的两个最重要特征性组分——重复序列与间隔序列。重复序列是长度为20-40bp(bp,即碱基对,是形成双链核酸以及编码遗传信息的基本单位)的短回文DNA片段,该片段一个接一个地重复排列,但两个重复序列之间都被间隔序列间隔开;间隔序列又被称为Spacer DNA,长度为20-70bp。科学家对CRISPR的Spacer DNA进行测序分析,发现不同位置的Spacer DNA序列差异明显,这意味着什么呢?
21世纪以来,基因测序和比对难度大大降低,研究者们得以将这些发现的Spacer DNA与其他物种中已经测序完成的DNA序列进行比对,他们惊讶地发现这些Spacer DNA竟然与病毒DNA——特别是噬菌体DNA完美吻合!此外,研究人员还在CRISPR基因的不远处鉴定出一系列与CRISPR相关的基因,并将其命名CRISPR-associated,简称Cas基因。Cas基因编码的蛋白被称为Cas蛋白,具有解旋酶的活性,可以将DNA链解旋,同时也具有核酸酶活性,可以切割DNA链。
结合以上线索,研究者们大胆地推测CRISPR可能是细菌的一个免疫系统,细菌通过CRISPR系统来抵抗敌人——噬菌体(可以理解为吃细菌的病毒)的入侵,这一推测也在后续实验中得到了证实。
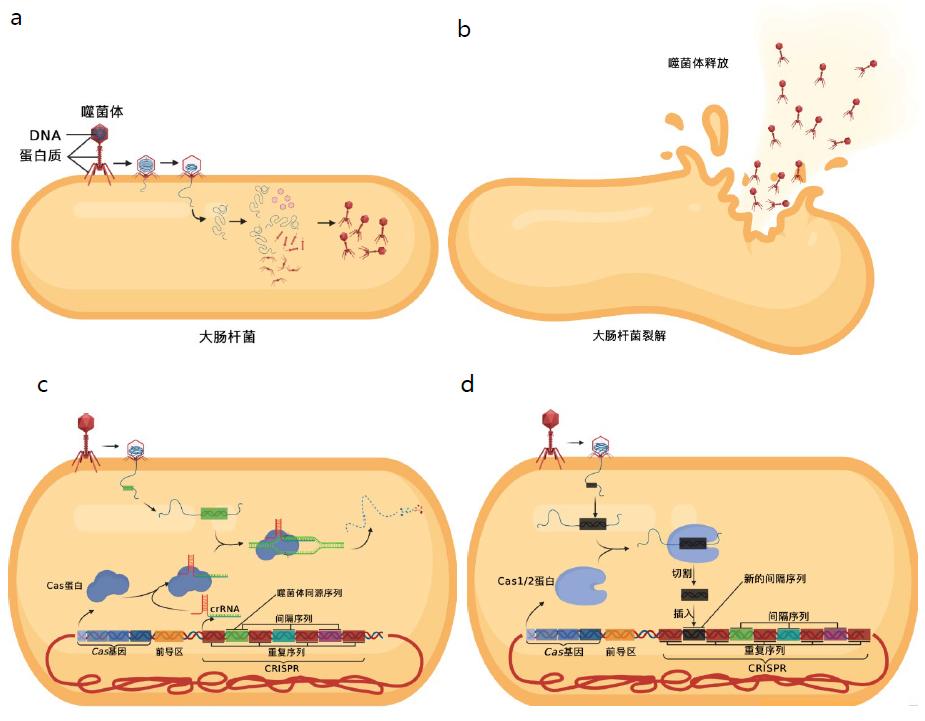

为了更好地理解,让我们来模拟噬菌体入侵大肠杆菌的过程(图1)。当噬菌体将病毒DNA注射到大肠杆菌中,将出现如下状况:
① 大肠杆菌没有类似CRISPR的免疫系统
一般情况下,噬菌体DNA将感染细菌细胞,并将自己的DNA嵌入到细菌基因组上,利用细菌宿主的基因表达系统复制出大量的噬菌体(图1a),并最终使细菌破裂,大量的噬菌体得以释放(图1b);
② 细菌中存在CRISPR系统(图1c)
这时细菌转录CRISPR形成CRISPR RNA(简称crRNA),特异性地与病毒DNA匹配;同时细菌表达Cas蛋白,并与CRISPR形成CRISPR复合体,将噬菌体注入的病毒DNA打断,将病毒感染的苗头掐灭。
多么奇妙的系统啊!但棘手的是,不是每种噬菌体DNA都会存在与之对应的Spacer DNA,如果恰好没有spacer DNA能与噬菌体DNA匹配,如图1d所示,细菌会产生一类新的蛋白——Cas1和Cas2蛋白,它可以与噬菌体注入的DNA结合,将其打断并将其一小段DNA复制并整合到CRISPR系统中,完成一个新的Spacer DNA的添加。
到这里,我们就可以回答CRISPR是什么了:它是一串间隔、重复、间隔、重复序列的组合,而且这些间隔序列实际上是过去所受感染的记录,以保证细菌不会再受到相同的感染。同时,CRISPR还具有在DNA中写入新的感染过程的能力。这与人类高水平的、通过抗体和免疫细胞实现的免疫系统的工作方式类似,因此可以将CRISPR系统看作是细菌的适应性免疫系统。
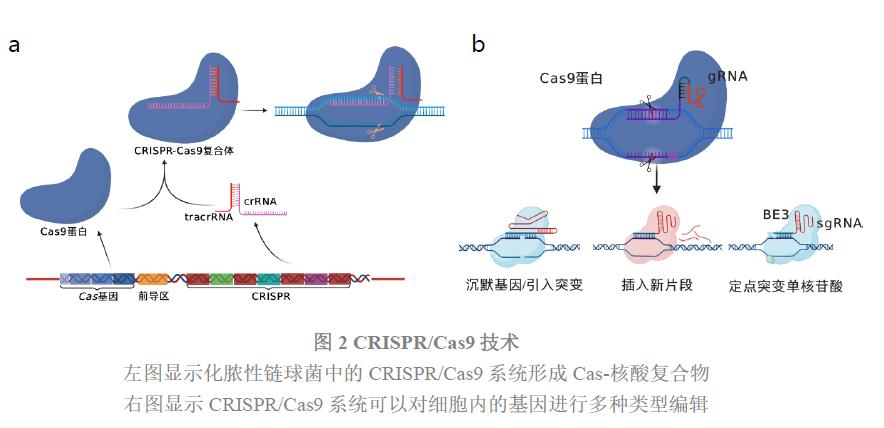
02 CRISPR/Cas9技术能量惊人
目前CRISPR系统中应用最广的是CRISPR/Cas9系统,它们是在文章开头所提到的两位诺奖得主的实验室中被发现的。埃马纽埃尔·沙尔庞捷研究的是化脓性链球菌中的Cas-CRISPR系统,有趣的是化脓性链球菌中只含有一个称为Cas9的Cas蛋白,但同时会转录两个RNA链——crRNA(识别匹配的DNA片段)和tracr RNA(与Cas9蛋白结合并将crRNA固定到正确位置),共同组成一个复合体用于切割DNA(图2a)。
詹妮弗·杜德纳在保留Cas9蛋白的基础上创制guide RNA以代替crRNA和tracr RNA(图2b),并将识别序列修改为靶向目标序列的RNA——猜猜当目标DNA被识别后会发生什么?
在Cas-核酸复合体与目标DNA相结合之后,Cas蛋白将对目标DNA进行定点切割,并因此打断该基因。尽管细胞会尝试将其修复,但在修复过程中会产生插入或缺失突变,从而达到沉默基因或达到引入突变的效果(图2b)。而当我们想插入一个新的片段,除了Cas9、guide RNA外,还需要在系统中添加想要引入的目标片段DNA,一共需要3个组分。打断DNA后,目标片段DNA将被细胞内固有的同源重组修复系统通过DNA置换的方式插入到基因组,从而实现插入新片段的目的(图2b)。
也就是说,我们在细胞中利用CRISPR系统可以随心所欲地使一个基因沉默,甚至将一个新的基因嵌入。
03 用好这把双刃剑
利用CRISPR/Cas9技术在基因组上进行任意的编辑和修改,这彻底改变了生命科学。
基因组编辑有许多好处。在农业方面,可以利用CRISPR系统加速动植物的育种进程,实现对优良性状基因的集合,也可以使一种物种获得其他物种的优良性状;我们还可以遴选出控制更优益性状的基因,使植物或动物更富有营养、产量更高、可以抵御更多疾病以及能在严酷的环境中生长。
对动物基因的编辑并不局限于养殖动物,还可以针对疾病传播的媒介生物,比如蚊子。来自伦敦帝国学院的Austin Burt教授和Andrea Crisanti教授目前正致力于利用CRISPR设计一种“男性偏向性畸变基因驱动器(SDGD)”,意在使X染色体在雄蚊产生精子的过程被切割。被切割后的X染色体无法正常遗传,因此能大大减少雌蚊对于疟疾的传播。
人们更期盼基因编辑能够拯救生命。2015年,身患白血病的一岁女婴蕾拉·理查德兹正面临死神的威胁。传统的化疗和骨髓移植均宣告失败,医生与她的父母背水一战,选择此前从未在人体上做过治疗的尖端技术——CAR-T疗法。被基因改造过的CAR-T细胞能够特异性识别并高效杀死肿瘤细胞,从而治愈白血病。我们不禁要追问:未来是否能使用这项技术改变致癌的变异或者激发抗癌的潜力,以真正地治愈癌症?
CRISPR技术也正在衍生出新的治疗艾滋病病毒(HIV)的疗法。
当然,要论CRISPR技术应用宝座上最夺目的明珠,当属对遗传病治疗的促进。此前人类面对刻在染色体上的致病基因束手无策,除了一小部分遗传性疾病可以通过药物来缓解痛苦外,绝大多数遗传病患者只能终生忍受痛苦。有了CRISPR技术,无论是对突变的治病基因进行定点修复还是使其沉默,抑或者将正常的基因插入缺失的位置,我们都可以像在word文档中进行删除、更改一样,对人类的生命密码——基因组DNA进行编辑修改。
此外,CRISPR在加速疫苗的研制,促进基础科研发展等方面也大有可为。
问题来了——这么好的技术,我们是否可以“随心所欲”地大用特用?
显然不能。方便且高效的基因组编辑技术会助长欲望的蔓延。举个例子,如果将CRISPR用于人类胚胎的改造,在胚胎孕育早期中去编辑改变人类的特征如眼睛的颜色甚至智力的高低等,这虽然对健康没有影响但无形中会助长“定制婴儿”的风气,使阶级垄断上升到基因水平。要知道改变婴儿的基因不仅会影响单一个体本身,也会影响他们的后代,从而对全人类的基因库造成威胁。如果不法分子利用基因组编辑来制备前所未有的更恶劣的病毒性疾病传播事件,后果更是不堪设想。因此,尽管基因编辑有许多好处,但仍需要接受道德、伦理和法律的约束。我们必须辩证规范地使用CRISPR技术,挖掘其潜能去解决世界性的难题,同时避免不良甚至有害应用。
作者简介:
李荣宇 军事科学院军事医学研究院,硕士研究生
原标题:《【科学普及】CRISPR:重新设计生命》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




