- +1
【学术前沿】JMCB | 孙少琛课题组揭示卵母细胞中LRRK2对微丝和线粒体功能的调控
以下文章来源于JMCB科学前沿 ,作者孙少琛课题组
JMCB科学前沿.
分享生命发现,走近科学前沿。学术期刊 Journal of Molecular Cell Biology (JMCB) 将助力更多优秀的科研成果在世界科学舞台精彩亮相!

关注我们,获取更多相关资讯
哺乳动物卵母细胞减数分裂成熟的典型特征之一是不均等分裂,产生一个大的卵母细胞和一个小极体,这对母源物质的保存起到重要作用,确保后期的受精和胚胎发育。卵母细胞减数分裂恢复从生发泡破裂开始,纺锤体在卵母细胞中央形成,随后纺锤体迁移到皮层区域,染色体分离后发生胞质分裂,排出第一极体。微丝骨架在中期纺锤体迁移过程中发挥重要作用;除此之外,微丝还参与卵母细胞中细胞器(如线粒体)的分布和功能调节,进而影响卵母细胞的发育潜能和受精后的胚胎命运。
近日,南京农业大学动物科技学院孙少琛课题组在Journal of Molecular Cell Biology (JMCB) 在线发表了题为“LRRK2 regulates actin assembly for spindle migration and mitochondrial function in mouse oocyte meiosis”的研究成果,该研究发现LRRK2是调控哺乳动物卵母细胞微丝介导的纺锤体迁移及线粒体功能的重要因子。
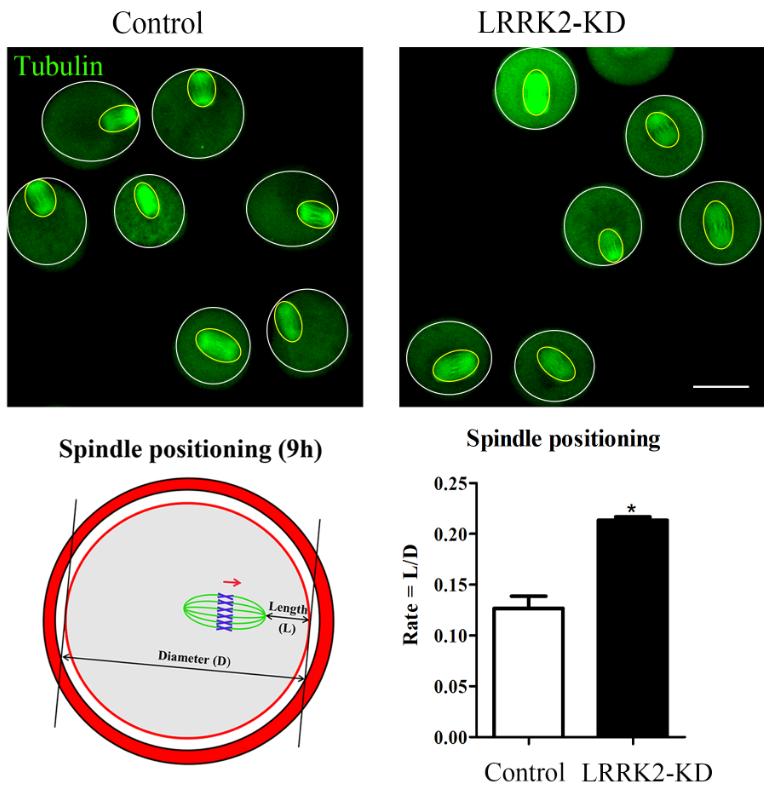
LRRK2敲低后影响卵母细胞纺锤体的迁移过程
孙少琛课题组长期从事卵母细胞微丝骨架的分子调控研究,在前期工作中报道了微丝成核因子Formin家族及Arp2/3复合物参与微丝介导的纺锤体迁移。而LRRK2是一种具有GTP酶和激酶双重活性的蛋白,在有丝分裂中参与细胞骨架动力学、细胞器功能、囊泡运输和自噬等多种生命过程的调节。该研究发现在小鼠卵母细胞成熟过程中LRRK2主要分布在纺锤体外围。LRRK2缺失造成卵母细胞极体排出失败或大极体的出现,这主要是通过影响胞质微丝的组装,进而影响纺锤体迁移和胞质分裂造成的。质谱分析和免疫共沉淀筛选发现LRRK2与ROCK-cofilin信号通路因子与微丝成束因子fascin互作,进而调控胞质微丝的组装。此外,LRRK2缺失导致卵母细胞中纺锤体外围聚集的线粒体减少,线粒体拷贝数下降,ATP产量下降,同时氧化应激水平升高,表明LRRK2可能通过微丝进一步参与线粒体功能调节。
综上所述,LRRK2在卵母细胞中通过调控ROCK、fascin参与微丝的组装,进而影响减数分裂纺锤体的迁移及线粒体功能,该研究为卵母细胞微丝骨架调控的分子机制提供了新见解。
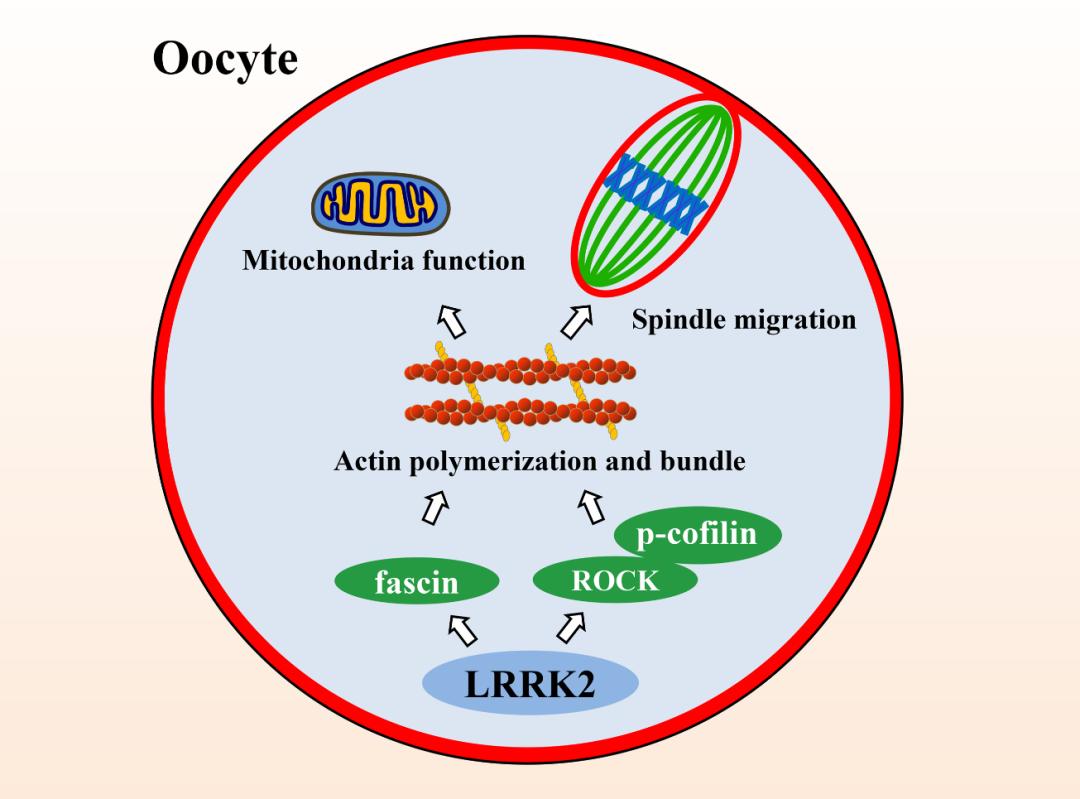
LRRK2在卵母细胞减数分裂成熟中的作用模式图
作者简介
孙少琛,南京农业大学动物科技学院教授、博士生导师,国家优秀青年基金获得者。主要研究方向为卵母细胞成熟的环境影响及分子调控,在Development等期刊发表论文120余篇。
博士研究生潘振楠为本论文的第一作者,孙少琛教授为本论文的通讯作者。该工作受到国家重点研发计划项目、国家自然科学基金的经费资助。
关于JMCB
Journal of Molecular Cell Biology (JMCB) 创刊于2009年10月,由中国科学院主管,由中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)和中国细胞生物学学会共同主办,与牛津大学出版社 (Oxford University Press,OUP) 开展版权合作,为完全开放获取期刊,聚焦分子细胞生物学前沿进展及相关多学科交叉研究,2020年度影响因子为6.216,5年影响因子为6.688,预测2021年度影响因子将继续稳定上升。
来源:JMCB科学前沿
原标题:《【学术前沿】JMCB | 孙少琛课题组揭示卵母细胞中LRRK2对微丝和线粒体功能的调控》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




