- +1
中国的新冠病毒特效药来了,这对我们意味着什么?
原创 白宁 品玩
作者|白宁
邮箱|baining@pingwest.com
12月8日,新冠单克隆中和抗体安巴韦单抗/罗米司韦单抗联合疗法(此前称BRII-196/BRII-198联合疗法)获得中国药品监督管理局的应急批准上市,用于治疗新冠病毒。
这是国内首个获监管机构批准上市的单抗药物,也是中国首个全自主研发的抗新冠病毒特效药,由清华大学与深圳市第三人民医院及腾盛博药合作研发而成。
消息一出,瞬时点燃了网络平台,如今,当子弹飞了足够长的时间,诸多针对性研究和讨论部分尘埃落定之后,我们或许可以更全面地了解这款药。
突破
首当其冲的,自然是“0”的突破。
在此之前,根据国家卫生健康委办公厅于2021年4月14日公布的最新版《新型冠状病毒肺炎诊疗方案(试行第八版 修订版)》,新冠肺炎患者在医院使用的抗病毒治疗药物是在临床观察研究中可能具有一定效果的治疗药物,诊疗方案特别标注目前对这些药物的态度是“试用”,需要“在临床应用中进一步评价疗效”:
1、α—干扰素:成人每次500万U或相当剂量,加入灭菌注射用水2ml,每日2次,雾化吸入,疗程不超过10天;
2、利巴韦林:建议与干扰素(剂量同上)或洛匹那韦/利托那韦(成人200mg/50mg/粒,每次2粒,每日2次)联合应用,成人500mg/次,每日2至3次静脉输注,疗程不超过10天;
3、磷酸氯喹:用于18~65岁成人。体重大于50kg者,每次500mg,每日2次,疗程7天;体重小于50kg者,第1、2天每次500mg,每日2次,第3~7天每次500mg,每日1次;
4、阿比多尔:成人200mg,每日3次,疗程不超过10天。
而根据安巴韦单抗/罗米司韦单抗联合疗法药物(以下简称“安/罗联合疗法”)的研发责任人,清华大学医学院教授、全球健康与传染病研究中心主任张林琦介绍,安/罗联合疗法药物通过静脉注射的方式进入患者身体,只需要40分钟,便可在患者体内产生抗体,“马上起效”。这与上述的各种“试用”药物的疗效堪称天差地别。
安/罗联合疗法针对的患者是新型冠状病毒检测结果为阳性,同时伴有进展为重型COVID-19危险因素的成人和青少年(≥12岁,体重≥40 kg)患者。另外,虽然主要作用以治疗为主,但因为抗体在体内可存留9~12个月,对预防感染也有一定作用。

在央视“对话”栏目的采访中,钟南山说:“这款药不但对重症病人有效果,使用了以后还有比较高的抗体,对有免疫缺陷的病人,有预防作用。”
安/罗联合疗法中起作用的是中和抗体。所谓中和抗体,就是可以中和病毒的活性抗体。新冠病毒想要侵入人体,需要利用自身表面的刺突蛋白与细胞结合,就像“小偷偷开房门时使用的钥匙”。中和抗体可以提前与病毒刺突蛋白的某个片段作用,从而阻断这种结合,让病毒撬“门”失败。
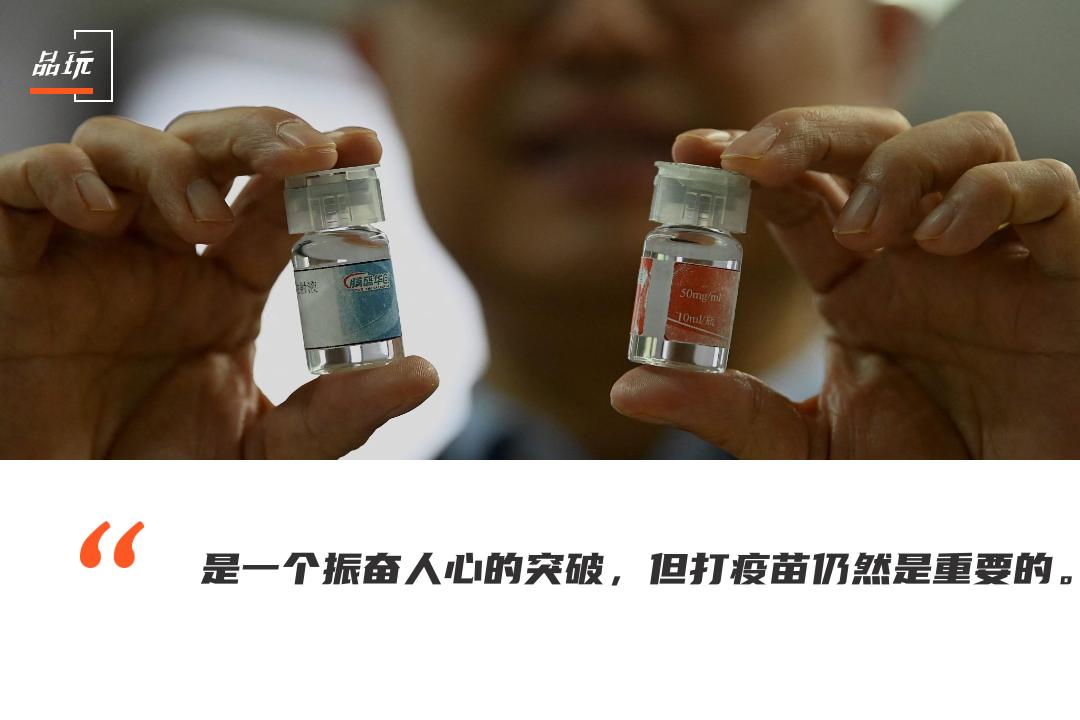
从这款中和抗体的命名——安巴韦单抗/罗米司韦单抗联合疗法——可以得知,这款药物使用了两个新冠病毒抗体,即安巴韦单抗和罗米司韦单抗,作为一个组合。
在中和抗体型药物研发领域,选择组合抗体是一种常见的策略。因为单个中和抗体的靶点针对性太强(靶点即药物与机体生物的结合部位),万一病毒变异,靶点失效,很容易导致药物失效,联合型的抗体相当于双重保障。目前,美国食品药品监督管理局(FDA)紧急授权的中和抗体药物中,联合型抗体有3种,分别为礼来LY-CoV016/LY-CoV555、再生元(Regeneron)REGN10933/REGN10987和阿斯利康AZD8895/AZD1061。

张林琦展示安巴韦单抗(蓝色药瓶)和罗米司韦单抗(红色药瓶)
安/罗联合疗法所用的抗体BRII-196、BRII-198是从206对抗体中精心挑选出来的,可以结合在新冠病毒刺突蛋白的受体结合区的不同表位。其中,BRII-196与新冠病毒刺突蛋白结合的部位属于高度保守区域,可以降低产生突变与逃逸的概率,另一个抗体BRII-198和新冠病毒刺突蛋白结合的部位避开了和BRII-196结合点重叠的区域,在另一个表位。这一组合能够很好的对体内的新冠病毒进行抑制,确保其不会与人体细胞相结合,从而使得患者的情况可以得到明显好转。
根据张林琦介绍,这样的联合会有组合拳的效果,即便病毒发生了变异,导致一个抗体失效,还有另一个抗体保底,所以依然可以有效应对。
12月5日,腾盛博药发布了ACTIV-2研究3期临床试验分析的基于患者总人数的关键性数据分析结果。数据来源于美国国立卫生研究院(NIH),安/罗联合疗法的二期和三期临床试验的流程设计和执行均由此机构主导。整个研究在全球多个临床试验中心开展,包括美国、巴西、南非、墨西哥、阿根廷和菲律宾,研究包含了2021年1月至7月全球SARS-CoV-2 变异株快速出现期入组的847例入组患者,依据严格的随机、双盲、安慰剂对照的国际标准进行。在此期间,腾盛博药只负责提供试验所需药物。
根据公布出来的结果,可以得到以下信息:
与安慰剂相比,安/罗联合疗法将临床进展为重度疾病高风险的COVID-19门诊患者的住院和死亡风险降低80%,具有统计学显著意义。
治疗组在28天内无患者死亡,而安慰剂组有9例患者死亡。
安全性方面,与安慰剂组相比,安/罗联合疗法治疗组的3级或以上不良事件较少,且未发现与药物相关的严重不良事件或输液反应。
在目前已获得官方许可的四款中和抗体联合疗法中,这是三期临床表现最好的数据。
再生元(Regeneron)REGN10933/REGN10987:2020年9月29日再生元公布了第一阶段275人的临床数据,并在10月28日公布了另外524人的临床数据。除此研究外,再生元还在开展多项临床研究。总体临床数据显示,与安慰剂相比,两个剂量REGN-COV2(2.4g和8g)都可更快缓解患者临床症状,降低门诊患者就医次数(包括住院、急诊等)。REGN-COV2可以将门诊患者就医次数降低57%(2.8% vs 6.5%),可以将具有一个或多个风险因素(包括年龄>50岁、BMI>30、心血管疾病、代谢疾病、肺部疾病、慢性肝病、慢性肾病、免疫低下)的高风险患者的就医次数降低72%。
礼来LY-CoV016/LY-CoV555:2021年1月26日,礼来公司在其官网宣布,礼来中和抗体bamlanivimab(LY-CoV555)和etesevimab(LY-CoV016)联合疗法可将COVID-19住院和死亡的风险降低70%,达到了III期BLAZE-1临床试验的主要研究终点。
阿斯利康AZD8895/AZD1061:2021年10月公布的III期临床试验结果显示,与安慰剂相比,轻度非住院患者通过肌肉注射600毫克剂量AZD7442,发生重症或死亡的风险降低50%;在对出现症状五天内接受治疗的参与者进行的预先分析结果显示,与安慰剂相比,AZD7442将发生重症或死亡的风险降低67%。
当然,这些数据中不论降低了80%还是70%,还都只是在临床试验中得出的结果,在真正投入市场之后,随着临床数据的增加,数据还会发生变化,增高或降低都有可能。
突变毒株的考验
随着新冠病毒的突变,无论是哪种类型的抗体,都将面临病毒免疫逃逸的风险。因为中和抗体识别的位点都只是刺突蛋白上极小的一个片段。如果病毒在这个位点上发生了突变,那么针对这个位点作用的中和抗体疗效就会受影响,中和效率会下降,乃至完全丧失中和能力。于是,重新测试抗体的抗病毒性也就成了必选项。
检验病毒突变对现有抗体药物或疫苗影响的一种重要手段是病毒实验。
今年11月以来,变异株Omicron出现。它被认为是目前最强的变异毒株,其刺突蛋白产生了32处突变。这么多的突变很有可能影响中和抗体识别的位点,进而威胁单克隆抗体药物的有效性。
12月23日,北京大学谢晓亮研究组在《Nature》上发表论文《Omicron escapes the majority of existing SARS-CoV-2 neutralizing antibodies》,检测了Omicron的突变对9种获得监管部门授权紧急使用的抗体药物的影响。
实验表明,针对Omicron,礼来、再生元、阿斯利康的联合单抗都分别呈现出不同程度的失效,只有Vir-7831与DXP-604能抑制Omicron突变株。其中,Vir-7831所在位点属于保守位点,而DXP-604则是由国内药企丹序生物与北大谢晓亮团队共同研发的单抗药物,目前正在国内开展二期临床试验。
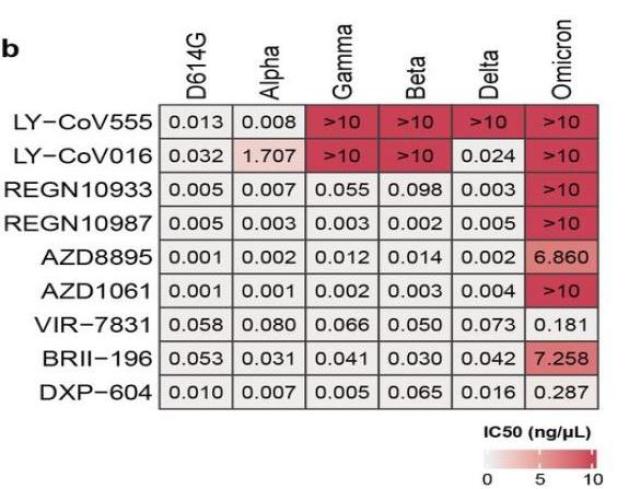
北大团队检测了九种单克隆抗体药中和不同新冠病毒突变株的效力。研究人员从新冠康复者以及疫苗接种者体内提取血清,观察不同稀释倍数的血清阻断真病毒或人工构建的假病毒感染细胞的能力。如果一个突变株需要更多的血清来中和,那么就意味着对于这个突变株,血清里的中和抗体能力下降了。
此外,论文显示腾盛博药获批联合疗法中的抗体BRII-196对Omicron失活,但未显示另一个抗体BRII-198的结果。
同一天,发表在《Nature》上的另一篇论文《Striking antibody evasion manifested by the Omicron variant of SARS-CoV-2》显示,针对Omicron突变株的中和实验中,全球有代表性的19个中和抗体里仅有BRII-198仍显示有效。论文由华裔病毒学家、哥伦比亚大学医学院教授何大一团队撰写,文中补充,由于Omicron还有一些具有更多突变的分支,抗体是否仍有效需进一步检测。
另外,清华大学实验室近期也针对Omicron突变株做了中和实验,结果显示BRII-196中和Omicron的效果的确下降明显,但BRII-198仍然保持活性,中和效果甚至相比其他突变毒株略有上升。
不过,不论安/罗联合疗法的中和抗体在体外实验中验证有效还是无效,结果都仅供参考,因为这些实验都不是在人体上进行。张林琦说,“金标准一定是临床上的,我们需要更多流行病的数据、更多当地临床一线医生的研究结果,才能知道病毒的致死率和传播率到底怎么样,逃逸能力有多强。对于整个科学界都是这样,不到临床,很难下结论。”
疫苗还需要么
随着国内外多款新冠治疗药物的出现,开始有人宣称,人们不需要疫苗了。和现实状况相比,这实在是一个很大的误解。
以中和抗体为例,虽然抗体药物通过改造可以在人体内保持较长的活性,但是每出现一个新变异株都需要重新测定活性。而且Omicron已经证明,因为单抗药物的靶向性很强,虽然通过混合使用可以扩大作用的范围,但如果病毒的变异性过强,病毒逃逸的可能性依然很大。
根据张林琦的介绍,中和抗体药物的生产周期需要4到5个月。因为抗体是活细胞在自然生长过程中经过发酵产出的,在此基础上,再经过提纯、过滤等一系列工艺流程,才能得到药物,而且产能还极其有限。
又因为成本高昂,所以单抗药物售价也颇高。目前国外同类药物的价格是2100美金/针,这还是购买量达几百万份的政府采购价。国内价格虽然可能比国外低,也依然会远远高于疫苗。
而依照目前的病毒变异情况,随着对病毒和中和抗体的熟悉,虽然在实验室里挑选中和抗体的整个研发流程会被缩短,但是规模化生产阶段所需的时间是无法大规模缩短的,所以病毒变异的速度很可能比药物上市研发速度的更快。相比之下,接种疫苗可以产生很多不同的抗体,即便一部分抗体可能因为病毒突变失活,但一般仍会保留一些有效的抗体。
所以即便中和抗体药物让我们在对抗新冠肺炎的过程中拥有了更多的主动权,在现实中,依然不能放弃疫苗,需要坚持预防为主,治疗药物为辅的双线并行。过去的经验也告诉我们,在抵抗传染性疾病上,前期的预防永远是第一位的。
*参考资料:
Omicron突变株横空出世,新冠抗体药物扛得住吗?
《新型冠状病毒肺炎诊疗方案(试行第八版 修订版)》
《Striking antibody evasion manifested by the Omicron variant of SARS-CoV-2》
《Omicron escapes the majority of existing SARS-CoV-2 neutralizing antibodies》
《对话》 20211218 新冠特效药的速度与激情
《面对面》 20211219

· 文章版权归品玩所有,未经授权不得转载。
原标题:《中国的新冠病毒特效药来了,这对我们意味着什么?》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




