- +1
非酒精性脂肪肝全基因组Meta分析
原创 Cell Press CellPress细胞科学
 医学
医学Medicine
2021年11月3日,加拿大拉瓦尔大学Benoit J. Arsenault课题组在Cell Press细胞出版社期刊Cell Reports Medicine上发表了一篇题为“Electronic health record-based genome-wide meta-analysis provides insights on the genetic architecture of non-alcoholic fatty liver disease”的研究型论文,基于电子病历记录的全基因组Meta分析鉴定出5个非酒精性脂肪肝的遗传位点。
摘要
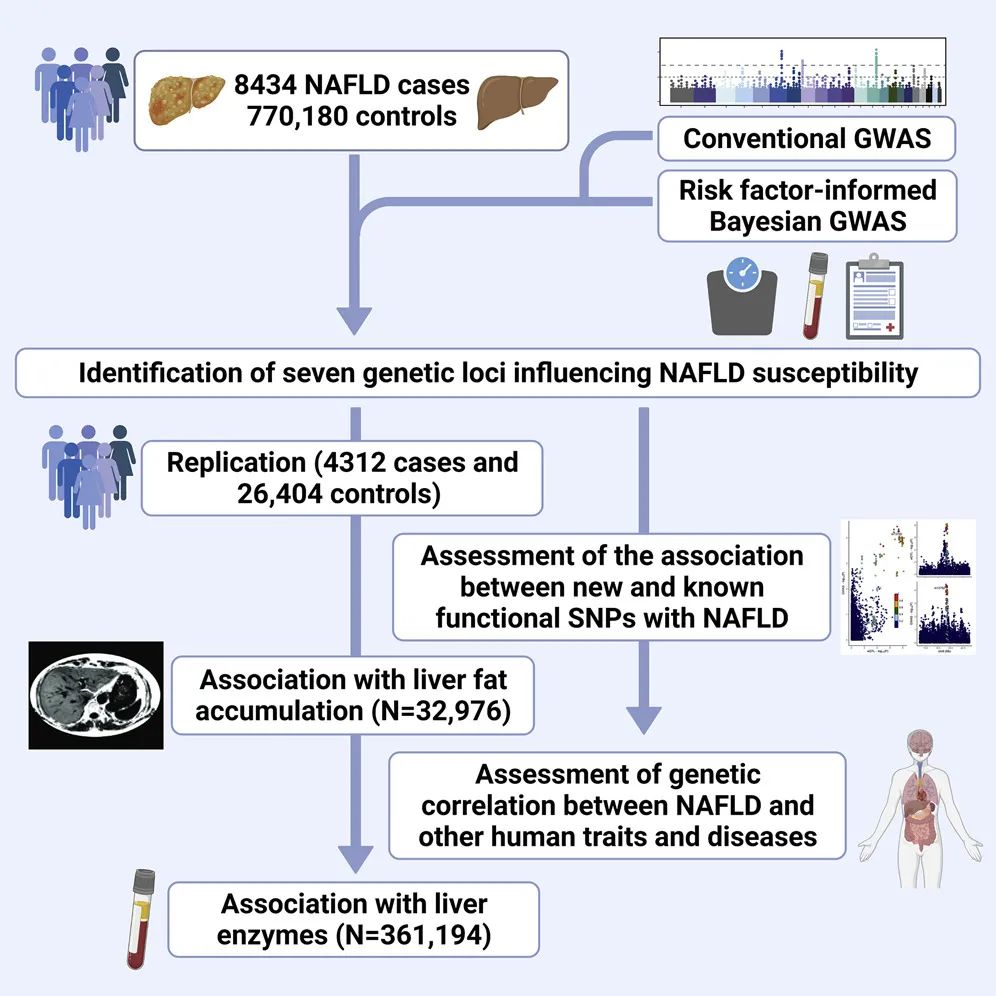
非酒精性脂肪肝(NAFLD)是一种与多种慢性疾病相关的复杂疾病。本研究旨在确定与NAFLD相关的遗传变异,并评估其功能后果。我们对四个包含电子病历记录的具有欧洲血统的NAFLD患者队列进行了全基因组Meta分析(包括8,434例病例和770,180例对照)。我们确定了五个潜在的NAFLD易感基因座,分别位于GCKR、TR1B1、MAU2/TM6SF2、APOE和PNPLA3处或附近。我们还报告了脂肪组织中LPL低表达对NAFLD易感性的潜在因果效应,以及FTO基因型对NAFLD的影响。本研究观察到NAFLD与心脏代谢性疾病及其危险因素(如身体脂肪积累/分布、脂蛋白-脂质水平、胰岛素抵抗和冠状动脉疾病)之间的正向遗传相关性,还发现了NAFLD与父母寿命、社会经济地位,以及乙酰乙酸乙酯水平的负向遗传相关性。总的来说,该项大型GWAS Meta分析揭示了对NAFLD遗传结构的深入了解。
 引言
引言非酒精性脂肪肝(NAFLD)是最普遍的慢性肝病之一[1-2]。最近的研究估计,全世界约25%的成年人可能患有NAFLD[3-4]。根据预测,该疾病到2030年将成为西方国家最常见的肝移植指征[5]。NAFLD是一种进行性肝脏疾病,对其他几种慢性疾病都有潜在影响,例如心血管疾病(CVD)(NAFLD患者死亡的主要原因)[6-9]、2型糖尿病(T2D)[10-11]、血脂异常[12],以及其他肝外表现,包括慢性肾脏疾病[13]和胃肠道肿瘤等[14]。
为了更充分地了解NAFLD这类复杂疾病的病因,并开发可以帮助该疾病患者延长生命、活得更健康的疗法,我们需要更深入地探究NAFLD的遗传结构。持续进行的全基因组关联研究(GWAS)已经发现了与肝脏脂肪堆积[15-16]、肝脏酶水平[17]和不同形式的肝脏疾病相关的遗传变异[18-19],但只有少数几项小型GWAS试图确定与NAFLD临床诊断相关的遗传变异。例如,针对电子病历记录和基因组学(eMERGE)网络的GWAS纳入了1,106例NAFLD病例和8,571例对照,但只确定了一个NAFLD的易感基因座——PNPLA3;英国生物库(UK Biobank)的NAFLD GWAS 纳入了1,664例NAFLD病例和40,005例对照,但只确定了两个与NAFLD呈强相关的区域——PNPLA3和PBX4/TM6SF2。FinnGen队列(包含651例非酒精性脂肪肝病例和176,248例对照)的4号数据库分析也证明了,PNPLA3和PBX4/TM6SF2两个基因座的遗传变异与NAFLD具有关联性。
在此,我们提出了一项基于电子病历记录(EHR)的GWAS Meta分析结果,以确定与NAFLD相关的遗传变异。该分析包括多个GWAS汇总统计——eMERGE和FinnGen队列、英国生物库的最新NAFLD GWAS(2,558例病例和395,241例对照),以及爱沙尼亚生物库(Estonian Biobank)的最新GWAS(4,119例病例和190,120例对照)——总计8,434例NAFLD病例和770,180例对照。
结果
确定与非酒精性脂肪肝相关的遗传变异
为了确定与NAFLD相关的遗传变异,我们首先利用英国生物库和爱沙尼亚生物库的数据开展了两项新的GWAS,并对四个队列(英国生物库、爱沙尼亚生物库、eMERGE和FinnGen队列)进行了Meta分析。这些队列共包括8,434例均通过电子病历记录确定的NAFLD病例,以及770,180例对照。总的来说,通过组合传统的GWAS和揭示危险因素的GWAS,我们的分析确定了可能影响NAFLD易感性的七个基因座,包括位于PNPLA3、PBX4/TM6SF2、GCKR、TR1B1、MAU2/TM6SF2、APOE和PNPLA3处或附近的遗传变异。
NAFLD相关变异与NAFLD相关表型的关系
我们通过分析另一个队列(麻省总医院布里格姆生物库)的数据,探究了上述遗传变异的影响,以及与NAFLD相关的表型,例如英国生物库数据所揭示的肝脏脂肪堆积和肝酶水平等。我们发现,七个SNPs的影响方向与GWAS Meta分析中观察到的一致。在麻省总医院布里格姆生物库中进行的分析显示,除了FTO和LPL位点的变异之外,上述其他SNPs都与NAFLD显著相关。而且,七个SNPs对肝脏脂肪堆积的影响方向与在GWAS Meta分析中观察到的一致,除了LPL基因座的变异之外,其他SNPs都与肝脏脂肪堆积存在显著关联。最后,我们探究了NAFLD相关的七个变异与肝酶ALT(丙氨酸氨基转移酶)、AST(天冬氨酸氨基转移酶)、GGT(γ-谷氨酰转移酶)和ALP(碱性磷酸酶)之间的关联性。结果表明,除了FTO和GCKR的变异与ALT水平无关,APOE的变异与AST水平无关,PNPLA3的变异与GGT水平无关之外,其他所有变异都与肝酶呈正相关关系。GCKR、LPL、TRIB1和APOE的变异与ALP水平呈正相关,MAU2/TM6SF2和PNPLA3的变体与ALP水平呈负相关。总的来说,这一分析结果表明,NAFLD相关的七个变异与NAFLD相关的性状存在关联,例如肝脏脂肪堆积和/或肝酶水平等。
NAFLD与人类代谢和表型性状的关系
我们对NAFLD与在LD Hub数据库中描述的240个人类性状进行了跨性状的遗传相关性分析。LD Hub包含对数百个人类性状的公开GWAS的汇总统计,可用于评估这些性状之间的连锁不平衡(LD)得分回归。本研究的结果显示,NAFLD与心脏代谢性状和疾病(例如肥胖、胰岛素抵抗、甘油三酯水平、冠状动脉疾病、2型糖尿病)之间存在高水平的遗传相关性,并与父母寿命、教育水平和乙酰乙酸乙酯水平存在负向的遗传相关性。
讨论
我们利用英国生物库和爱沙尼亚生物库的数据,进行了两项关于NAFLD的全基因组关联研究(GWAS),并将这些结果与两项公开的NAFLD GWAS(分别来自eMERGE网络和FinnGen队列)的结果相结合。本项GWAS Meta分析包括8,434例通过电子病历记录(EHRs)确定的NAFLD病例和770,180例对照,因而是目前最大的NAFLD临床诊断全基因组分析。结合揭示危险因素(risk factors-informed)的贝叶斯GWAS(bGWAS),本研究确定了两个已知的NAFLD易感基因座——TM6SF2和PNPLA3,以及五个潜在的新候选基因区域,这些发现能为基于EHRs(GCKR、TRIB1、LPL、FTO、APOE)的NAFLD临床诊断提供帮助。
我们的常规GWAS分析(根据BMI调整或不进行调整)报告指出,GCKR、TRIB1、MAU2/TM6SF2、APOE和PNPLA3位点的变异可能与NAFLD有关。既往研究发现这些基因座的遗传变异与一些肝脏表型有关[20-23],我们的GWAS Meta分析揭示了与NAFLD遗传结构相关的重要信息。利用bGWAS,我们的研究证实了已知的NAFLD相关遗传变异,并确定了新的潜在NAFLD基因座(LPL和FTO),这些基因座可能通过间接影响NAFLD的危险因素(BMI和甘油三酯)而与NAFLD相关。
最近的一篇预印本文章发现,FTO位点的某个变异是导致高ALT水平的易感位点[24],尽管研究者对FTO位点变异的生物学相关性仍有争议,但FTO是一个特征明显的肥胖症遗传位点[25]。在调整BMI后,FTO位点变异与NAFLD的关联不再显著,说明了该变异对NAFLD的影响取决于其对体重的作用。
尽管在主要分析中GCKR位点的变异与NAFLD无关,但bGWAS分析和根据BMI调整的常规GWAS发现,GCKR是NAFLD的一个易感位点。也有其他研究报告了GCKR位点的变异与肝脏脂肪堆积[26]和肝脏酶水平[27]的关联。这一分析表明,GCKR位点的遗传变异可能参与调节与肥胖和/或甘油三酯水平升高相关的NAFLD风险。编码脂蛋白脂肪酶(LPL)的基因——LPL位点的变异可能也发挥了相似的作用。在本研究中,我们发现皮下脂肪组织中LPL的基因预测表达与NAFLD之间存在潜在的因果关系。
既往研究表明,NAFLD可能与心血管疾病(CVD)或2型糖尿病(T2D)等慢性疾病有关,或可预测其风险。我们的遗传相关性分析显示了NAFLD与这些疾病及其危险因素(如肥胖和胰岛素抵抗)的关联。我们还报告了NAFLD与酮体乙酰乙酸、父母寿命之间的负相关关系,这表明NAFLD可能是影响人类寿命的一个重要因素。NAFLD的治愈是否会影响这些性状和结果仍有待确定。有趣的是,结合其他研究,我们的分析表明,针对LPL合成与代谢途径的疗法或能预防NAFLD及其他疾病,例如高脂血症和冠状动脉疾病,且不会增加其他人类疾病的患病风险。目前已有许多针对LPL途径的治疗药物处于研发过程中,包括血管生成素样蛋白-3(ANGPTL3)抑制剂[28]、胰高血糖素样肽-1(GLP-1)受体激动剂[29]和葡萄糖依赖性胰岛素样肽(GIP)/GLP-1双受体激动剂[30]。
审校:虞莎 Cell Reports Medicine 科学编辑
相关论文信息
论文原文刊载于CellPress细胞出版社期刊Cell Reports Medicine上,点击“阅读原文”查看论文
▌论文标题:
Electronic health record-based genome-wide meta-analysis provides insights on the genetic architecture of non-alcoholic fatty liver disease
▌论文网址:
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(21)00299-8#%20
▌DOI:
https://doi.org/10.1016/j.xcrm.2021.100437
本文参考文献
[1] Sumida, Y. & Yoneda, M. Current and future pharmacological therapies for NAFLD/NASH. Journal of gastroenterology 53, 362-376 (2018).
[2] Stefan, N., Häring, H.-U. & Cusi, K. Non-alcoholic fatty liver disease: causes, diagnosis, cardiometabolic consequences, and treatment strategies. The lancet Diabetes & endocrinology 7, 313-324 (2019).
[3] Younossi, Z. M. et al. Global epidemiology of nonalcoholic fatty liver disease—meta-analytic assessment of prevalence, incidence, and outcomes. Hepatology 64, 73-84 (2016).
[4] Eguchi, Y. et al. Prevalence and associated metabolic factors of nonalcoholic fatty liver disease in the general population from 2009 to 2010 in Japan: a multicenter large retrospective study. Journal of gastroenterology 47, 586-595 (2012).
[5] Pais, R. et al. NAFLD and liver transplantation: current burden and expected challenges. Journal of hepatology 65, 1245-1257 (2016).
[6] Yoshitaka, H. et al. Nonoverweight nonalcoholic fatty liver disease and incident cardiovascular disease: a post hoc analysis of a cohort study. Medicine 96 (2017).
[7] Brouwers, M. C., Simons, N., Stehouwer, C. D. & Isaacs, A. Non-Alcoholic fatty liver disease and cardiovascular disease: assessing the evidence for causality. Diabetologia, 1- 8 (2020).
[8] Kotronen, A. & Yki-Järvinen, H. Fatty liver: a novel component of the metabolic syndrome. Arteriosclerosis, thrombosis, and vascular biology 28, 27-38 (2008).
[9] Targher, G., Day, C. P. & Bonora, E. Risk of cardiovascular disease in patients with nonalcoholic fatty liver disease. New England Journal of Medicine 363, 1341-1350 (2010).
[10] Anstee, Q. M., Targher, G. & Day, C. P. Progression of NAFLD to diabetes mellitus, cardiovascular disease or cirrhosis. Nature reviews Gastroenterology & hepatology 10, 330 (2013).
[11] Lonardo, A., Ballestri, S., Marchesini, G., Angulo, P. & Loria, P. Nonalcoholic fatty liver disease: a precursor of the metabolic syndrome. Digestive and Liver disease 47, 181-190 (2015).
[12] Neuschwander-Tetri, B. A. et al. Clinical, laboratory and histological associations in adults with nonalcoholic fatty liver disease. Hepatology 52, 913-924 (2010).
[13] Kaps, L. et al. Non-alcoholic fatty liver disease increases the risk of incident chronic kidney disease. United European Gastroenterology Journal, 2050640620944098 (2020).
[14] Armstrong, M. J., Adams, L. A., Canbay, A. & Syn, W. K. Extrahepatic complications of nonalcoholic fatty liver disease. Hepatology 59, 1174-1197 (2014).
[15] Speliotes, E. K. et al. Genome-wide association analysis identifies variants associated with nonalcoholic fatty liver disease that have distinct effects on metabolic traits. PLoS Genet 7, e1001324 (2011).
[16] Parisinos, C. A. et al. Genome-wide and Mendelian randomisation studies of liver MRI yield insights into the pathogenesis of steatohepatitis. Journal of hepatology 73, 241-251 (2020).
[17] Chambers, J. C. et al. Genome-wide association study identifies loci influencing concentrations of liver enzymes in plasma. Nature genetics 43, 1131-1138 (2011).
[18] Emdin, C. A. et al. A missense variant in Mitochondrial Amidoxime Reducing Component 1 gene and protection against liver disease. PLoS genetics 16, e1008629 (2020).
[19] Anstee, Q. M. et al. Genome-wide association study of non-alcoholic fatty liver and steatohepatitis in a histologically characterised cohort☆. Journal of hepatology 73, 505- 515 (2020).
[20] Emdin, C. A. et al. A missense variant in Mitochondrial Amidoxime Reducing Component 1 gene and protection against liver disease. PLoS genetics 16, e1008629 (2020).
[21] Romeo, S. et al. Genetic variation in PNPLA3 confers susceptibility to nonalcoholic fatty liver disease. Nature genetics 40, 1461-1465 (2008).
[22] Kozlitina, J. et al. Exome-wide association study identifies a TM6SF2 variant that confers susceptibility to nonalcoholic fatty liver disease. Nature genetics 46, 352-356 (2014).
[23] Parisinos, C. A. et al. Genome-wide and Mendelian randomisation studies of liver MRI yield insights into the pathogenesis of steatohepatitis. Journal of Hepatology (2020).
[24] Vujkovic, M. et al. A genome-wide association study for nonalcoholic fatty liver disease identifies novel genetic loci and trait-relevant candidate genes in the Million Veteran Program. medRxiv, 2020.2012. 2026.20248491 (2021).
[25] Scuteri, A. et al. Genome-wide association scan shows genetic variants in the FTO gene are associated with obesity-related traits. PLoS Genet 3, e115 (2007).
[26] Speliotes, E. K. et al. Genome-wide association analysis identifies variants associated with nonalcoholic fatty liver disease that have distinct effects on metabolic traits. PLoS Genet 7, e1001324 (2011).
[27] Chambers, J. C. et al. Genome-wide association study identifies loci influencing concentrations of liver enzymes in plasma. Nature genetics 43, 1131-1138 (2011).
[28] Gaudet, D. et al. Vupanorsen, an N-acetyl galactosamine-conjugated antisense drug to ANGPTL3 mRNA, lowers triglycerides and atherogenic lipoproteins in patients with diabetes, hepatic steatosis, and hypertriglyceridaemia. European heart journal 41, 3936-3945 (2020).
[29] Vergès, B. et al. Liraglutide Increases the Catabolism of Apolipoprotein B100– Containing Lipoproteins in Patients With Type 2 Diabetes and Reduces Proprotein Convertase Subtilisin/Kexin Type 9 Expression. Diabetes Care (2021).
[30] Wilson, J. M. et al. The dual glucose‐ dependent insulinotropic peptide and glucagon-like peptide-1 receptor agonist, tirzepatide, improves lipoprotein biomarkers associated with insulin resistance and cardiovascular risk in patients with type 2 diabetes. Diabetes, Obesity and Metabolism 22, 2451-2459 (2020).
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2026 上海东方报业有限公司




