- +1
照束光便可降血糖?华东师大开发光遗传工具可或控制血糖稳态
利用一束光来治疗疾病?通过光照实现降血糖?
2021年10月4日,生物技术领域顶级期刊《Nature Biotechnology》在线发表了来自华东师范大学生命科学学院、上海市调控生物学重点实验室、华东师范大学医学合成生物学研究中心叶海峰研究团队的成果“A small and highly sensitive red/far-red light-mediated optogenetic switch for multiple applications in mammals”。
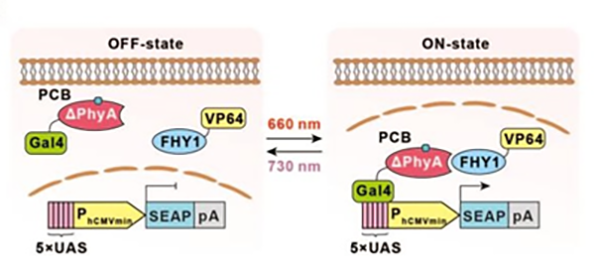
REDMAP系统原理
该研究开发了一个模块小、灵敏度高、可逆性良好的光遗传学工具,命名为REDMAP。研究人员将装载REDMAP系统的工程化细胞移植至小鼠、大鼠和兔的皮下后,可以通过光来精准控制小鼠和大鼠体内胰岛素的表达,成功实现了对糖尿病小鼠和大鼠血糖稳态的控制。无需每天定时服用药物或注射胰岛素,只需要每天光照几分钟即可达到显著降血糖的效果。
据叶海峰团队介绍,课题组将目光放在了来自植物拟南芥的光敏蛋白PhyA(phytochrome A)上,在红光照射下,该蛋白能和其伴侣蛋白FHY1(far-red elongated hypocotyl 1)形成二聚体,并在远红光照射下解离。根据这一特点,研究人员构建了基于PhyA-FHY1的转录激活系统。研究人员将PhyA与GAL4的DNA结合域融合表达,将FHY1和转录激活因子VP64融合表达。红光刺激下,PhyA-GAL4和FHY1-VP64结合形成复合体并招募RNA聚合酶,从而启动下游基因的表达。但起初,使用完整的PhyA并不能激活下游基因的表达。随后,研究人员对其进行了工程改造,通过优化激活子和伴侣蛋白,最终得到了一个模块小且高度灵敏地响应红光的光遗传学工具,并将其命名为REDMAP。
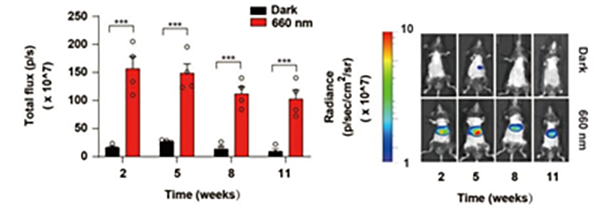
REDMAP介导的小鼠体内长期基因控制
利用光来控制细胞信号通路可以为基础研究提供便捷可控的研究方法。因此,叶海峰课题组将ΔPhyA定位到细胞膜上,将FHY1和SOS蛋白的激活域SOScat进行融合表达,通过红光照射来控制SOScat的细胞定位,从而实现了Ras/MAPK信号通路的激活和去激活,成功构建了REDMAPSOS-Ras工具。此外,研究人员还构建了REDMAPCas工具,将REDMAP系统与基因编辑工具CRISPR-dCas9结合在一起,实现了对哺乳动物细胞、小鼠肝脏及肌肉内源基因转录的高效调控。
接着,研究人员探究了REDMAP系统在基因治疗领域的能力。由于截短的ΔPhyA蛋白具有较小的尺寸,可以利用腺相关病毒包装。因此,研究人员将REDMAP包装至腺相关病毒(AAV2/8)中并将其注射至小鼠体内,实现了长达三个月以上的光控基因表达。
治疗蛋白的精准控制对疾病的治疗具有重要意义。研究人员将装载REDMAP系统的工程化细胞移植至小鼠、大鼠和兔的皮下,探究其光响应能力。结果显示,短时间的光照(1-5分钟)即可诱导报告基因的高效表达。接着,研究人员通过光来精准的控制小鼠和大鼠体内胰岛素的表达,成功实现了对糖尿病小鼠和大鼠血糖稳态的控制。无需每天定时服用药物或注射胰岛素,只需要每天光照几分钟即可达到显著降血糖的效果,这充分表明了REDMAP系统在精准可控的细胞治疗领域具有极高的应用潜能。
总之,该研究开发了一个模块小、灵敏度高、可逆性良好的光遗传学工具,为基础医学和转化医学研究,尤其是精准可控的基因治疗和细胞治疗领域提供了强有力的新型控制系统。
据悉,2019级博士生周阳和2020级博士生孔德强为共同第一作者,叶海峰研究员为论文的通讯作者。该研究受到了国家重点研发计划“合成生物学”重点专项、国家自然科学基金、上海市科委合成生物学重大项目的资助。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




