- +1
【科技前沿】鲁伯埙/丁澦团队合作开发靶向自噬的降脂化合物(LD-ATTEC)
许多疾病由特定的生物大分子积累引起,而特异性降解这些致病分子可以从根本上干预或治疗疾病,具有重要的科学及临床价值,给生物医药领域带来革命性进展。近年主要由美国科学家原创发展的PROTAC(PROteolysis TArgeting Chimera)等靶向降解技术是医药产业界的热点(Nat Chem Bio观点丨蛋白质靶向降解PROTAC疗法的研究进展),可特异靶向降解致病蛋白,但对于非蛋白类的生物大分子,如脂类、核酸和衰老的细胞器等的降解无能为力。
2021年7月8日,复旦大学生命科学学院鲁伯埙与丁澦课题组合作在Cell Research杂志上发表文章 Degradation of lipid droplets by chimeric autophagy-tethering compounds,首次实现了非蛋白类生物大分子的靶向降解,从而实现了靶向降解技术从蛋白向非蛋白物质的突破。

该目标的实现基于复旦大学鲁伯埙/费义艳/丁澦团队于2019年发表的原创技术ATTEC(AuTophagy-TEthering Compounds,详见BioArt报道:Nature突破丨复旦鲁伯埙/丁澦/费义艳团队合作研发亨廷顿病潜在新药——“明辨忠奸”的小分子胶水 )。该研究证明了可利用筛选得到的“小分子胶水”将目标蛋白绑定至自噬小体进行降解。该研究发表于Nature,并入选了Nature评选的年度十大杰出科技论文。然而,ATTEC这一概念是否可以拓展至非蛋白生物分子,以及是否可以利用组装拼接设计ATTEC以省去繁琐的大规模筛选步骤,仍然未知。在本次发表于Cell Research的研究中,研究团队证明,ATTEC技术不仅可降解蛋白质,还可通过靶向自噬-溶酶体途径降解包括脂类的非蛋白质类生物大分子,且ATTEC技术也可采取拼接的双功能化合物设计策略(图1),从而规避费时费力的大规模筛选。
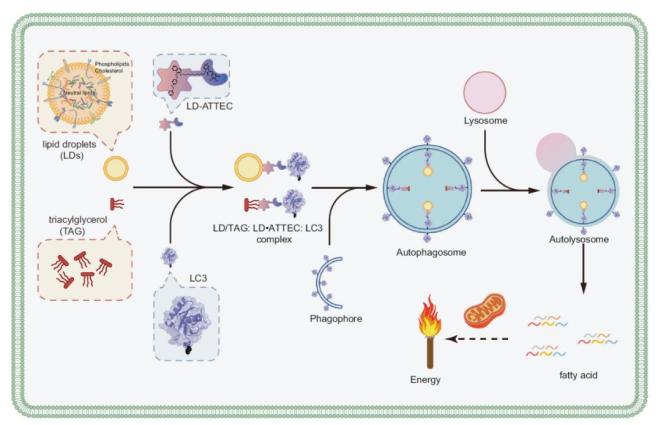
图1 LD-ATTEC化合物一端与脂滴(LDs)或甘油三酯(TAG)结合,另一端与自噬小体特征蛋白LC3结合,形成三元复合物,将脂滴和甘油三酯通过自噬-溶酶体选择性降解
项目团队以脂滴,这一细胞内储存脂肪的细胞器为降解目标设计ATTEC化合物(LD-ATTEC)。脂滴的过分储积可能与多种疾病相关,比如肥胖、非酒精性脂肪肝、神经退行等。因此脂滴的降解可能对相关疾病产生有益效果,而LD-ATTEC也可以作为工具化合物研究脂滴与这些疾病的因果关联。
团队首先设计了4个LD-ATTEC化合物,分别以之前报道的LC3结合小分子GW和DP作为靶向自噬小体的矛头,以Sudan III和Sudan IV作为靶向脂滴的矛头,通过短链连接以上配体,合成了LD-ATTEC C1-C4四个双功能分子(图2)。
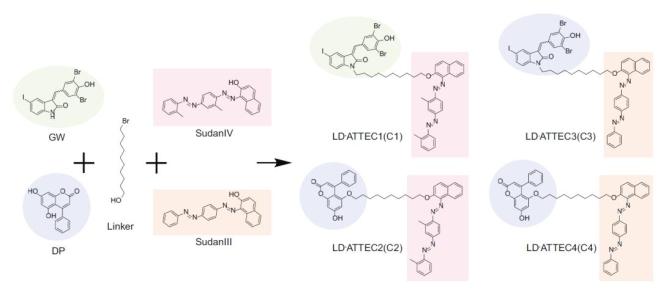
图2 设计合成4个LD-ATTECs(C1-C4)化合物的思路
首先在油酸诱导的MEF细胞模型上验证了相关化合物的效果,5-15μM的C1或C2化合物处理24小时后,可基本完全降解脂滴。该降解作用依赖于自噬,用Atg5敲除(导致LC3无法脂化,抑制自噬)的细胞系进行对照实验,观察不到降解效果。在SH-SY5Y细胞上可观察到类似结果,因此,该作用机制可能是普遍的。通过饥饿诱导或氯化铵处理增强或抑制细胞整体自噬水平仅仅微弱改变了脂滴的水平,说明LD-ATTEC靶向降解可能比整体改变自噬水平具有更高的效率。
为了证明LD-ATTEC化合物的有效性,团队又利用3T3-L1分化的脂肪细胞进行了内源脂滴的降解实验,观察到了类似的降解效果。同样,自噬抑制剂氯化铵或Atg5敲低可抑制LD-ATTEC化合物的效果。仅含有单个靶向自噬小体或脂滴的矛头没有降解脂滴的效果,说明必须是双功能分子才能特异靶向自噬降解脂滴。
随后,研究团队通过一系列实验证明了LD-ATTEC仅特异将脂滴靶向自噬小体,并不影响细胞整体的自噬水平。通过MST及改进的ELISA实验,证明了LD-ATTEC化合物在体外实验可同时结合LC3和甘油三酯。通过共定位实验,证明LD-ATTEC化合物提高了共定位比例。
为了进一步证明LD-ATTEC将脂滴靶向自噬小体而非直接通过靶向溶酶体进行降解,团队进一步在敲除了LC3的293T细胞验证了相关化合物的效果,证明缺失LC3可阻断化合物的降解效果。另外,团队在MEF细胞实验证明LD-ATTEC化合物并不影响自噬小体和溶酶体的数量。通过pH敏感的mRFP-GFP-LC3(溶酶体的低pH将会使得绿色荧光蛋白变性而不显色)系统,团队验证了LD-ATTEC不干扰自噬小体和溶酶体的融合过程。
为了证明LD-ATTEC特异降解中性脂滴而不影响细胞膜的完整性和功能,团队通过脂组学分析,发现LD-ATTEC主要降解了中性脂类,而很少影响构成细胞膜带电荷的极性脂类。
研究团队最后通过小鼠动物实验验证了LD-ATTEC化合物的实际降解效果。在db/db和NASH(非酒精性脂肪肝病)两个动物模型上,C3和C4均显示了良好的降脂效果。
本项研究从概念上证明了组装拼接型ATTEC可将非蛋白类生物物质直接特异性靶向至自噬-溶酶体途径降解,首次实现了非蛋白类物质的靶向降解技术,并证明了组装接型ATTEC概念,为新药研发开拓了一条可能的原创路径。而所发现的LD-ATTEC化合物则可能为脂滴研究或脂滴相关疾病的干预提供重要工具或潜在药物。
复旦大学青年副研究员付玉华为本文第一作者,负责了大部分实验。博士生陈宁谢、王紫英及Plymouth大学的罗寿青教授也参与了本项研究,鲁伯埙和丁澦为该论文的通讯作者。
原文链接:
https://www.nature.com/articles/s41422-021-00532-7
本文转载自公众号“BioArt”(BioGossip)
中国生物物理学会官方订阅号,为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科技前沿】鲁伯埙/丁澦团队合作开发靶向自噬的降脂化合物(LD-ATTEC)》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2025 上海东方报业有限公司




