- +1
【学术前沿】Cell突破 | 迈出人-猴嵌合体第一步!季维智/牛昱宇/谭韬/吴军等合作揭示异种细胞…
全球每年大概有200万人亟待器官移植拯救生命,但器官来源主要依靠捐献,缺口巨大,根据《中国器官移植发展报告(2019)》,我国2019年公民逝世后器官捐献 仅5,818 例,很多病人特别是年轻病人在等待中去世,十分令人痛惜。现在主要的解决途径有三条:异种器官移植(Xenotransplantation)【1】;异种嵌合 (interspecies chimaeras)【2】;类器官(organoid)【3】及3D打印 (3D bio-printing)【4】等。但不同策略存在不同的问题,例如异种器官移植存在免疫排斥及伦理问题,解决的方法之一是敲除引起超急性排斥反应抗原,比如α-1,3-半乳糖转移酶 (α-1,3-galactosyltransferase,αGT)【5】。类器官及3D打印的方法可能存在器官功能不全,不能形成完美的可移植器官。虽然异种嵌合也存在着嵌合效率低下等问题,但可能是将来会产生突破的一个方向。近来大动物中的异种嵌合取得了一些列的突破性进展, 例如Juan Carlos Izpisúa Belmonte和吴军等人实现了人干细胞在猪早期胚胎中的嵌合【6】。中国科学院中国科学院动物研究所和中国科学院干细胞与再生医学创新研究院周琪院士、李伟和海棠课题组的团队首次拿到了食蟹猴-猪嵌合体(详见BioArt报道:特别关注 | 周琪/李伟/海棠合作团队首次获得猴-猪嵌合活体)【7】。这些研究为下一步嵌合体的研究带来了新的方向,比如异种之间进化差异在嵌合体中如何互相影响,细胞之间互做、通讯及竞争关系等等。
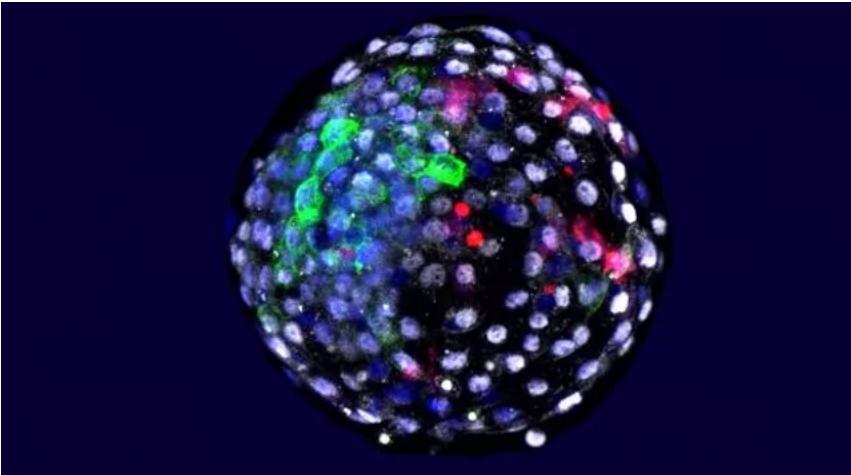
运用荧光染色标记,研究人员能够观察到早期胚胎发育中不同物种来源的细胞。Credit: 季维智, 昆明理工大学
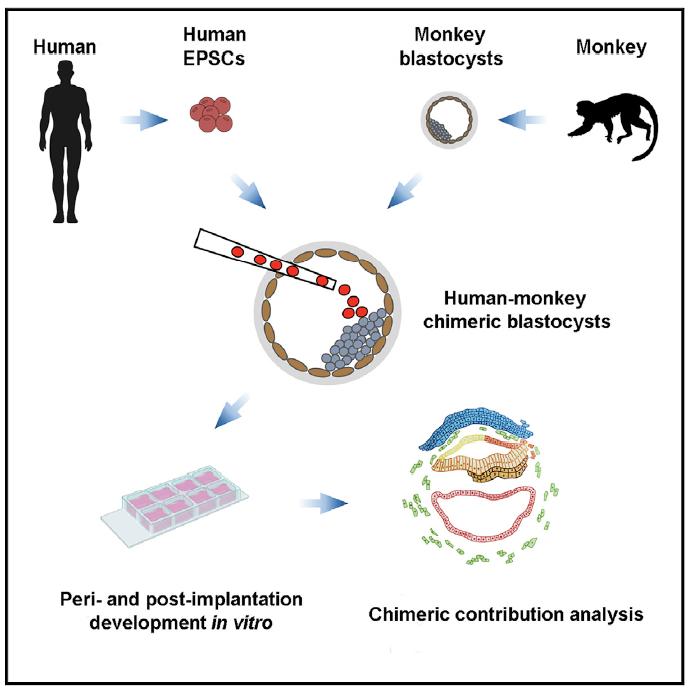
要回答这些科学问题,最好在一些与人比较接近的物种,比如非人灵长类动物中开展异种嵌合体研究来回答,以避免太多的干扰因素。2021年4月15日,昆明理工大学灵长类转化医学研究院和省部共建非人灵长类生物医学国家重点实验室季维智、牛昱宇、谭韬、代绍兴课题组(谭韬课题组博士生张又月、牛昱宇课题组博士生司晨洋、代绍兴为共同一作)与美国索尔克研究所Juan Carlos Izpisúa Belmonte和吴军(现任职德克萨斯大学西南医学中心)在Cell杂志上发表了题为Chimeric contribution of human extended pluripotent stem cells to monkey embryos ex vivo的文章。研究人员结合团队之前建立的猴胚胎体外培养系统,评估了人扩展多能性干细胞(hEPS)【8】在食蟹猴中的嵌合能力。

在该研究中,作者们发现hEPS可以嵌合进入食蟹猴胚胎,随着胚胎发育,hEPS同时可以伴随进入原肠运动,表达中、内胚层的marker基因。令人意外的是,hEPS细胞很难在食蟹猴胚胎中分化为滋养层细胞,而较容易分化为上胚层(epiblast,EPI)细胞,这一发现与hEPS细胞人鼠嵌合体实验存在一定的差异。通过进一步结合单细胞RNA测序等技术的研究,作者惊讶的发现hEPS细胞随着发育的进行,从表达特征上逐渐与受体食蟹猴胚胎细胞变得相似,反之亦然。于是作者怀疑受体胚胎提供了环境,通过细胞互做来引导了这一过程。通过细胞互作分析,作者不仅发现人猴在诸如EPI细胞之间存在的特异的互做关系,例如FGF5-FGFR4。同时受体猴胚胎细胞本身之间的细胞或者也增强了,主要涉及PI3K-Akt和MAPK等信号家族。更为有意思的是,通过分析,作者发现hEPS在嵌合体胚胎中的发育进程显著慢于正常发育的人和食蟹猴胚胎。同样可能与PI3K-Akt 和MAPK信号通路的改变有密切关系。
此项研究走出了人-非人灵长类异种嵌合研究的第一步,回答了异种嵌合细胞如何互做及发育程序差异如何调节等基础科学问题,为解决异种嵌合效率低下等问题提供新的思路,但对其深入理解以及后续探索还有很多未完成的部分,值得进一步研究。
原文链接:
https://www.cell.com/cell/fulltext/S0092-8674(21)00305-6?utm_source=EA
参考文献
1. Ekser, B., Ezzelarab, M., Hara, H., van der Windt, D.J., Wijkstrom, M., Bottino, R., Trucco, M., and Cooper, D.K. (2012). Clinical xenotransplantation: the next medical revolution? Lancet 379, 672-683.
2. Wu, J., Greely, H.T., Jaenisch, R., Nakauchi, H., Rossant, J., and Belmonte, J.C. (2016). Stem cells and interspecies chimaeras. Nature 540, 51-59.
3. Schutgens, F., and Clevers, H. (2020). Human Organoids: Tools for Understanding Biology and Treating Diseases. Annu Rev Pathol 15, 211-234.
4. Vijayavenkataraman, S., Yan, W.C., Lu, W.F., Wang, C.H., and Fuh, J.Y.H. (2018). 3D bioprinting of tissues and organs for regenerative medicine. Adv Drug Deliv Rev 132, 296-332.
5. Lai, L., Kolber-Simonds, D., Park, K.W., Cheong, H.T., Greenstein, J.L., Im, G.S., Samuel, M., Bonk, A., Rieke, A., Day, B.N., et al. (2002). Production of alpha-1,3-galactosyltransferase knockout pigs by nuclear transfer cloning. Science 295, 1089-1092.
6. Wu, J., Platero-Luengo, A., Sakurai, M., Sugawara, A., Gil, M.A., Yamauchi, T., Suzuki, K., Bogliotti, Y.S., Cuello, C., Morales Valencia, M., et al. (2017). Interspecies Chimerism with Mammalian Pluripotent Stem Cells. Cell 168, 473-486 e415.
7. Fu, R., Yu, D., Ren, J., Li, C., Wang, J., Feng, G., Wang, X., Wan, H., Li, T., Wang, L., et al. (2020). Domesticated cynomolgus monkey embryonic stem cells allow the generation of neonatal interspecies chimeric pigs. Protein Cell 11, 97-107.
8. Yang, Y., Liu, B., Xu, J., Wang, J., Wu, J., Shi, C., Xu, Y., Dong, J., Wang, C., Lai, W., et al. (2017). Derivation of Pluripotent Stem Cells with In Vivo Embryonic and Extraembryonic Potency. Cell 169, 243-257 e225.
来源:BioArt
原标题:《【学术前沿】Cell突破 | 迈出人-猴嵌合体第一步!季维智/牛昱宇/谭韬/吴军等合作揭示异种细胞的嵌合能力》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。




- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




