- +1
史料|中国第一位化学博士赵承嘏的博士论文
以下文章来源于BioArt ,作者赵承嘏

高屋建瓴,提供专家点评,引导学术争论,展现学术批评;诚心实意,关注科研生态,推广科研经验,倡导师生交流。
本文得到BioArt授权,并由中国化学会整理编辑存档

Tsan Quo Chou(1885-1966)
(药物化学家)
赵承嘏(1885—1966),男,江苏江阴人。中国植物化学和现代药物研究的开拓者和奠基人,原国立北平研究院药物研究所创始人,中国科学院上海药物研究所首任所长。首批中国科学院数理化学部学部委员。
1914年,赵承嘏获瑞士日内瓦大学博士学位,是我国第一位化学博士,之后留校任教两年,成为在欧洲大学讲授科学(Science)课程的第一位中国人。
2015年,赵承嘏先生诞辰130周年,中国科学院上海药物所专门组织团队进行“赵承嘏学术思想和科学精神的研究”,经由日内瓦大学的档案馆, 获得了赵承嘏先生的博士论文复印件,由中科院上海药物所李序文研究员翻译,柳红研究员校对,蒋华良院士撰文导读。
赵承嘏先生是我国第一个从事有机合成和天然产物全合成工作的科学家。这篇博士论文无论是对现代科学研究,还是对研究现代中国科技的发展历史,均具有重要的参考和史料价值。
导读
赵承嘏(1885—1966),男,江苏江阴人。1910年获曼彻斯特大学硕士学位, 1914年获瑞士日内瓦大学博士学位。中国用现代科学技术研究和开发中草药的先驱者,中国科学院上海药物研究所创始人、第一任所长,1955年当选中国科学院学部委员(现称院士)。关于赵承嘏先生的生平、求学经历和学术贡献,我们已经在《中国现代药物研究的开拓者—赵承嘏先生》一文中作了详细介绍(见《中国科学:生命科学(中文版)》2016, 46: 1)。今天,借赵承嘏先生博士论文(中文版)发布之际,谈一些感想。
赵先生105年前即在日内瓦大学获得博士学位,是我国第一位化学博士,为我国的药学事业和天然产物的发展作出了奠基性和开创性贡献。赵先生回国后在南京高等师范学校(南京大学前身)、协和医学院、国立北平研究院药物研究和中国科学院上海药物研究所工作期间,独自开展研究工作,直到去世当天的上午还亲自在实验室做实验。他平时几乎不与他人交流自己的留学经历,他的博士论文到底做了什么研究一直是个谜。2015年,赵先生诞辰130周年,上海药物所专门组织团队进行“赵承嘏学术思想和科学精神的研究”,我任研究组组长,请上海药物所毕业生、当时在日内瓦大学留学的周率真查阅了日内瓦大学的档案馆, 获得了赵承嘏先生的博士论文复印件,终于知道赵先生博士研究工作是天然产物紫堇碱(即延胡素甲素)的全合成,这样算来,赵先生是我国第一个从事有机合成和天然产物全合成工作的科学家。
赵先生的博士论文是用法文写的,我不懂法语,专门请我所留法回国工作的李序文博士翻译了赵先生的博士论文,并请精通有机合成的药物化学家柳红研究员作了校对。读完赵先生的博士论文,我感慨万千,心情久久不能平静,为赵先生深厚的有机合成功底、创新的研究思路和精巧的合成设计方法所折服。这篇博士论文无论是对现代科学研究,还是对研究现代中国科技的发展历史,均具有重要的参考价值。我当即与科学出版社联系,希望在获得日内瓦大学版权授权的情况下出版赵先生的博士论文,并以此为契机,相继出版对我国科技事业发展作出重大贡献的老一辈科学家(例如两弹一星功臣)的博士论文,以对我辈和更年轻科技工作者有所启示。科学出版社编辑说,赵先生的博士论文“太薄”(法语印刷版仅54页9600多字,中文翻译稿也只有13000多字),达不到出版的要求。无奈之余,我请BioArt发布这篇“薄薄的”中国第一位化学博士的博士论文。
赵先生的博士论文虽然很薄,但内涵丰富。赵先生的导师为著名有机化学家Amé Pictet,1911年Pictet与学生Theodor Spengler发展了β-芳基乙胺在酸性条件下与羰基化合物(如醛)缩合再环化为1,2,3,4-四氢异喹啉的反应,这是有机化学领域著名的人名反应—Pictet-Spengler反应(简称PS反应)(Ber. Dtsch. Chem. Ges. 1911, 44, 2030),至今依然被广泛应用于药物和天然产物合成。赵先生1912年跟随Pictet攻读博士学位期间,就用PS反应首次完成了天然产物紫堇碱的全合成,说明他善于将他人最新研究成果应用于自己了研究中。大家可以从他的博士论文中看到,赵先生科研思路缜密,将各种问题分析透彻后,再下手进行试验研究。
赵先生博士论文研究工作具有独创性。PS反应发现后,首先想到的应用是合成著名天然产物小檗碱及其衍生物四氢小檗碱(坎那定)。紫堇碱即是赵先生回国在协和医学院和国立北平药物研究所工作期间从中药延胡索中提取得到的天然产物延胡索甲素,与小檗碱的结构很类似(赵先生的博士论文中也提到了)。1911年,Pictet和他另一位学生Gams确实应用PS反应合成了小檗碱和四氢小檗碱(Ber. Dtsch. Chem. Ges. 1911, 44, 2480),赵先生在英国曼彻斯特大学留学时的导师William Henry Perkin, Jr和师弟Robert Robinson(1947年获得诺贝尔化学奖)曾在一篇综述(J. Chem. Soc., Trans. 1912, 101:262)中称赞这是一个brilliant合成方法。1929年,杜克大学Johannes S. Buck和Rose M. Davis发现Perkin和Robinson合成方法最终没有得到小檗碱和四氢小檗碱(J. Am. Chem. Soc. 1930, 52:660)。赵先生在博士论文中提到了Perkin和Robinson合成小檗碱和四氢小檗碱的合成方法,但没有照搬他们的合成方法,而是改变了反应试剂(如将甲醛改为乙醛)和反应条件。后来证明赵先生的合成方法是正确的,不仅获得了紫堇碱的目标化合物,而且确定了天然紫堇碱的正确结构(在此之前紫堇碱的结构有争议),或许他才是实现小檗碱类天然产物全合成的第一人。此外,赵先生在合成紫堇碱过程中,也进行了四氢罂粟碱与甲缩醛的缩合反应,获得去甲基-克拉立定,与时任日内瓦大学诊疗实验室主任A. Mayou的学生M. A. T. Aftandilian合作,测定了去甲基-克拉立定在青蛙、豚鼠和兔子上的生理活性。这或许为赵先生后来去法国罗克药厂工作以及回国后毕生从事天然药物研究奠定了基础。
1928年赵先生在协和医学院和国立北京研究院药物所工作期间,开展中药延胡索的植物化学研究,并企图从中发现镇痛药物,陆续提取出13种延胡索素, 用“甲、乙、丙、丁、戊、己、庚、庚……”来表示,其中延胡索甲素即为其博士论文合成的紫堇碱,1947年,赵先生在总结国立北平研究院药物研究所近10年工作时,专门提及延胡索庚素和辛素上海有机所黄鸣龙先生在德国留学时也分离到。1920年代,由于化学分析技术的缺乏,根本没有波普解析和核磁共振技术帮助解析结构,天然产物结构鉴定是非常困难的事情,有时需要全合成或合成模型化合物来解决这一问题。赵先生研究了延胡索和其他几十种药用植物的天然产物,我一直不理解他是如何解决天然物结构解析的,读了他的博士论文,终于明白,深厚的有机合成功底是他解决这一问题的法宝。
最后,我想说的是,上世纪初到1940年代,我国在欧美留学的学生数量不多,但大多数学业精湛,具有家国情怀,学成归国后,不计个人得失,为中国的科技事业发展作出了重要贡献。另一方面,1920年代之前,科学的中心在欧洲,博士生培养的模式也值得我们借鉴,注重科学问题的解决,而非一味追求论文的发表。博士论文也不像现在这样追求“厚度”,而是注重科学的深度和内涵。例如,赵先生合成紫堇碱的PS反应,目前依然应用于有机合成、特别是药物合成,连目前药物研究最前沿的技术之一DNA编码库的合成也经常使用PS反应。PS反应机制的研究也有新的发展,中国科学院上海有机化学研究所的游书力研究员和郑超副研究员团队综合利用理论计算和实验研究的方法提出了关于Pictet–Spengler反应的统一机理,拓展了PS反应的应用范围。
蒋华良(中国科学院上海药物研究所)
2019年12月13日
论文原文

博士论文
日内瓦大学科学学院自然科学专业
赵承嘏
江阴(中国)
科学硕士(曼彻斯特)
日内瓦
J. Studer 印刷厂,Plainpalais圆形广场3号
1914
科学学院在A. Pictet 教授的预先申请下授权进行该论文打印,并对该提案无任何异议。
日内瓦,1914年5月3日
院长:
C. E. GUYE.
致 Amé Pictet教授
以崇高的敬意和无比感激
本论文工作是在A. Pictet教授的指导下,于日内瓦大学有机和无机化学实验室完成的。
在这里,我要特别感谢A. Pictet教授对我的关心和照顾,以及他在本工作开展伊始到最终完成的过程中给我提出的所有宝贵意见。
前言
───
紫堇碱,分子式C22H27NO4, 于1826年由WACKENRODER【1】从紫堇属植物Corydalis Cava(紫堇科)的根中发现,是该植物中最主要的生物碱。紫堇碱的化学结构已经被大批科学家研究过,其中首先要提到的是E. SCHMIDT和他的学生们,包括DOBBIE,LAUDER,以及最新的学生GADAMER。这些研究者的工作为该生物碱的结构组成提供了一个近乎完美的概念。他们认为紫堇碱的结构和坎那定(四氢小檗碱)很接近。紫堇碱的骨架形成过程与坎那定相似,都是由两分子的异喹啉通过缩合的方式而共用一个氮原子和一个碳原子:
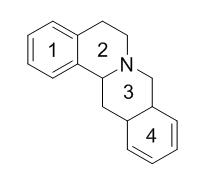


最终的结构可能只能通过合成的方法来确定。
首次尝试运用该方法是在1913年,MM. PICTET和MALINOWSKI【2】希望通过缩醛和四氢罂粟碱在盐酸的作用下缩合得到外消旋的紫堇碱。
这一尝试是基于PICTET 和SPENGLER【3】,以及PICTET和GAMS【4】的前期实验而开展的。
下面我们简单回顾一下这些前期的工作。
1911年,PICTET 和SPENGLER发现,当将苯乙胺的盐酸盐和甲缩醛以及过量的中等浓度的盐酸在水浴加热时,可以得到产量可观的四氢异喹啉盐酸盐。在这个反应中,盐酸首先皂化甲缩醛得到甲醛的水合物(甲二醇),并立即与苯乙胺反应;得到的产物进而进行环化并脱去两分子。



我们也可以用类似的反应来合成紫堇碱。通过用乙缩醛替换甲缩醛,同时将其作用于我们需要得到的四氢罂粟碱(III),假设该缩合反应也在2号位,那么如下图结构式IV所示的产物便可以得到,该结构也是我们认为的紫堇碱的可能结构之一。

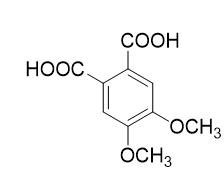
实际上,紫堇碱的合成就像天然的紫堇碱形成一样,是通过间-半蒎酸以及少量邻-半蒎酸的氧化得到。因此它拥有如下图所示的结构V。与之前的情况相反,在这里缩合反应在6位进行,方程式如下:

在这些条件中,还有两种方法是可以尝试的。可以从四氢罂粟碱出发,通过限制环化反应在2位进行来合成紫堇碱。我将一一列举这两种方法:
I. 假设甲缩醛倾向于进行2位的缩合反应,那么我们期望将其作用于四氢罂粟碱时可以得到去甲基-紫堇碱(结构VI)。在这种情况下,将仅有一个甲基的引入来获得紫堇碱。而鉴于FBEUND和BECK【5】在小檗碱系列化合物的合成方法,引入该甲基应该是可行的(见下文)。


在A. PICTET教授的指导下,我逐一进行了上述研究;我所获得的成果便是该论文所要达到的目标。在接下来的实验部分详述这些成果之前,我想先从理论上进行分析。
第一个方法:首先包括进行四氢罂粟碱和甲缩醛的缩合反应以及鉴定产物的结构。刚开始我是参照PYMAN【6】的方法通过将罂粟碱在锡和盐酸的作用下来制备四氢罂粟碱(盐酸盐的形式)。后来我从巴塞尔的《化学工业公司》免费获得了非常纯的四氢罂粟碱。
在PICTET和SPENGLER以及PICTET和MALINOWSKI所建立的反应条件下,我们的盐酸盐与甲缩醛的缩合反应能够非常容易完成。反应的产率甚至比上述学者的还要高;有些反应产率甚至达到了90%。产物(亚甲基-四氢罂粟碱)是一个无色的碱,熔点为157-158℃,分子式为C21H25NO4。
这个碱跟坎那定和紫堇碱的性质非常相似。尤其是将其与碘置于醇溶液加热时,它会去掉一个质子并在两者之间相互转化。与后两个生物碱类似,在一个脱氢季碱的氢碘化合物中,这些盐是黄色的并完全可以确定是罂粟碱和脱氢紫堇碱的盐的类似物。这一事实表明它们结构组成的类似以及由于与甲缩醛进行缩合反应而最终导致第四个母核的关环。
最后仅需要鉴定的是缩合反应到底是发生在2位还是6位。
亚甲基-四氢罂粟碱与浓硫酸加热生成了棕红色的溶液。这个颜色与生成紫堇碱的反应颜色完全一致,而当PICTET和MALINOWSKI所获得的克拉立定在同样的条件下是绿色的。
乍一看,这个反应似乎告诉我得到的是去甲基-紫堇碱,而且其与甲缩醛的缩合反应也很好的进行了,正如我预期的一样可以认为坎纳定的合成在2位进行。然而,我通过将该化合物进行氧化反应打消了最初的这个看法。
我用了一定量的高锰酸钾来做该氧化反应,并运用了DOBBIE和LAUDER【7】氧化紫堇碱的相同反应条件。在这个反应中,我得到了一个酸,并很容易鉴定为间-半蒎酸,然而在仔细寻找后我没有发现任何邻-半蒎酸的踪迹。因此,这似乎表明母核4中甲氧基的位置和克拉立定中的一样,因此其结构式如下图中数字VII所示。
然而,我并不想只依靠这唯一的证据。事实上,这两个间- 和邻-半蒎酸的性质极其相似,因此想要鉴别和分离它们是很棘手的,而且我也没有一个绝对可靠的方法。因此,我希望用其他转化方法来构建我的化合物的组成,即甲基化反应。通过在特定的位置引入一个甲基,我应该要么得到紫堇碱,要么得到克拉立定这两个很容易区别的碱,所以这个证据也不是我想找的绝对证据。
我的这个甲基化反应是建立在M. FREUND 和 H. BECK【8】的工作基础上的。他们从罂粟碱的盐和有机镁化物的反应中获得了脱氢罂粟碱的衍生物。例如,与甲基镁的碘化物反应进行的方程式如下:

因此,我将我的脱氢碱的氢碘化物通过将碘甲烷与镁加热进行了格氏反应,并且在没有进一步研究其产物的情况下,用碘将其氧化了。我同样获得了一个碱,而这些盐也被发现和脱氢克拉立定的盐是一样的,而与脱氢紫堇碱不一样。
这表明甲氧基在我的脱氢碱中的位置和在克拉立定中是一样的。这一证据加上已经完成的氧化反应表明亚甲基-四氢-罂粟碱不是去甲基-克拉立定,而是去甲-紫堇碱,其化学结构式如下:

这两个反应不同的原因不在于醛的性质不同,而是在于参与反应的碱。我认为这是一个非常奇怪的现象,因为我们惊奇的发现用两个CH3O基团来取代一个CH2O2基团能够指引该反应生成一个如此截然不同的新的取代物。
因此,通过上面提到的第一个方法来进行紫堇碱的合成最终发现是不可行的。
第二个方法:如上所述,第二种方法是我们必须设计一个合成紫堇碱的路线,包括不是将乙酸醛作用于四氢罂粟碱,而是与它的衍生物在6位反应。缩合反应因此不会在2位进行,最后在消除取代原子或基团的基础上,我们应该能够得到紫堇碱的两个结构式中的一个。唯一的条件是,这个取代基应该容易被消除。在满足该条件的取代基上,我们首先考虑引入的基团是NO2和NH2。
因此我的任务是准备硝基和氨基分别取代的四氢罂粟碱,结构式如下:
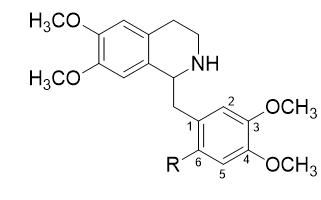
接下来在将四氢罂粟碱与硝酸反应时,虽然有一定的难度,我还是能够制备单硝基取代衍生物。硝基的取代位置能够通过还原该产物得到确定;因为我获得的氨基-四氢罂粟碱与之前的一样。因此,对四氢罂粟碱的硝化与对罂粟碱的硝化反应位置相同,而我的硝化衍生物正是想要的6-硝基-四氢罂粟碱。接下来我将这两个衍生物分别与乙缩醛进行了缩合反应。
硝基-四氢罂粟碱在所有条件都不发生缩合反应。这是一个在其他类似情况基础上【10】的有关硝基对环化反应负面影响的新的实例。
除了已经拥有一个次级碱外,氨基-四氢罂粟碱总是形成了一个有初级碱特征的碱,从而证明了与乙缩醛的反应仅仅在NH基团上进行。因此,毫无疑问环化反应会形成一个酰胺紫堇碱。然而,消除该产物的氨基对我来说曾是一项几乎无法实现的任务。
实验部分
───

参照PYMAN【11】的条件来制备该碱的盐酸盐:
10 g 罂粟碱
40 mL 浓盐酸
40 mL 乙醇
20 g 锡粒
以上样品置于圆底烧瓶中并在水浴加热回流5小时,然后我们再加入40 mL浓盐酸和5 g锡粒, 并再次加热反应5小时。接下来蒸干乙醇,并将浓缩的酸溶液用足够量的水稀释到氯锡酸盐完全沉淀为止。
该盐脱水后,再用一点冷水清洗,然后重新溶解于大概300 mL沸水中。在该溶液中通入一定量的硫化氢,然后沉淀,并用热水清洗沉积的硫化锡沉淀,最后在溶液中加入碳酸钠使游离碱沉淀下来。这个碱我们是通过在乙醚中反复搅拌,并加入稀盐酸而提取出来的。通过蒸发掉盐酸溶液,我们最终获得了四氢罂粟碱的盐酸盐,并可以在乙醇中重结晶;它结出的是无色晶体,熔点为217℃。
四氢罂粟碱与甲缩醛的缩合反应
─去甲基-克拉立定

经浓缩第一次沉淀的滤液,我们首先获得了同一个盐的第二次结晶,接着我们又获得了少量的另外一个熔点为268℃的盐酸盐,其结构没有得到进一步的研究。
去甲基-克拉立定,C21H25NO4。─ 去甲基-克拉立定盐酸盐的水溶液通过添加碳酸钠生成了大量游离碱的白色沉淀。我们再将该沉淀溶于尽量少的乙醇中,并通过加入水直到其持续浑浊为止来达到纯化的目的。通过冷却得到该碱的微小片状的无色晶体。三次结晶后,其熔点稳定在157-158℃。产率为80%。
元素分析

苦味酸盐 ─ 通过将苦味酸的的醇溶液和该碱(或者其盐酸盐)混合得到。它在醇中以黄色细针状结晶,并在空气中变成红色;该盐难溶于水,熔点 138 ℃。
氯铂酸盐 ─ 通过将氯化铂的水溶液加入该盐酸盐的水溶液中使其沉淀得到氯铂酸盐。通过在其乙醇溶液中加入盐酸使其重结晶,我们得到了橙色棱状晶体,几乎不溶于水。熔点在变黑情况下达到了231 ℃。
氯汞酸盐 ─ 通过在其盐酸盐的水溶液中加入氯化汞形成黄色沉淀。熔点为158℃。
去甲基-克拉立定的生理学性质
日内瓦大学诊疗实验室主任A. MAYOR教授和他的助手B. WIKI博士非常希望测试一下去甲基-克拉立定对动物机体的作用。他们将该研究的部分实验交给了其学生,M. A. T. AFTANDILIAN, 该学生的博士论文题目就是:亚甲基-四氢罂粟碱的药效研究【12】。(日内瓦1914)
我仅在这里转述一下该工作的结论(这些实验是在盐酸盐上做的)。
1 ° 毒性剂量:

a) 青蛙:抑郁状态,然后有麻醉特征,紧接着出现破伤风样抽搐的过激反射状态;接下来反射状态消失且呼吸停止(假死特征);最后,逐步恢复到正常状态。
b) 豚鼠:躁动现象,无目的乱跑,全身发抖,甚至有抽搐状态;接着出现阶段性或大或小的抑郁症状,并有轻度短暂的嗜睡现象;最后,持续长时间的疯狂撕咬[l4] 症状。
c) 兔子:一段时间的亢奋状态,震颤,随后经历非常严重的麻醉阶段并伴有反应灵敏度下降,以及中枢麻痹;在恢复正常之前,兔子经历了第二阶段的亢奋状态,但是强度较弱。如果剂量非常大的话,它会一上来就发生惊厥;然后,在解毒阶段,该动物会经历一段时间的麻醉状态。
d) 狗(小剂量):具有明显的麻醉现象以及一定程度的肌肉僵硬。
3 ° 致死剂量:
青蛙,停止心跳;
温血动物,停止呼吸。如果剂量过大,呼吸停止之前还有惊厥的危机;接着伴随着肺水肿的现象。
4 ° 亚甲基-四氢罂粟碱首先加速呼吸,然后呼吸会变浅:在麻醉期间,呼吸声很大,呼吸缓慢,甚至是周期性的呼吸。
5 ° 小剂量(1千克兔子给药几毫克)时,该生物碱是强心剂,能够轻微增加血压和加速脉搏。相反,大剂量时,它能降低血压并减慢脉搏。血压的降低主要时是该生物碱对血管运动中枢的影响造成的。心跳一直在持续,需要用到3倍于致呼吸停止的量来使心跳停止。
6 ° 亚甲基-四氢罂粟碱对迷走神经的心脏纤维的活动没有影响。
去甲基-克拉立定的分解反应试验
去甲基-克拉立定这一分子含有一个不对称碳原子;通过合成得到该碱也因此应该是一个外消旋体,而它也应该可以通过其两个旋光对映体与一个活性酸结合而得到分离。
我仅尝试了一次这种方法,而结果是阴性的。我选择了光学活性的溴代樟脑磺酸。我将几当量的水加入该酸和去甲基-克拉立定的混合物中并水浴加热,直到反应物溶解为止,冷却后得到第一个盐。将母液浓缩后加入浓的海盐溶液后,第二个盐得到了沉积。这两种盐分别在热水中重结晶了多次,之后其碱被提取出来;这两个碱的氯仿溶液通过旋光仪测定发现均没有光学活性。
高锰酸钾氧化去甲基-克拉立定
对于该氧化反应,我参照了DOBBLE和LAUDER【13】对于天然的紫堇碱的氧化以及PICTET和MALINOWSKI【14】对克拉立定的氧化。反应步骤如下:
2 g 去甲基-克拉立定以悬浊液形式溶于500 mL水中;该混合物置于一个大的圆底蒸发皿中,用明火加热到沸点左右并不断采用机械搅拌。接着将其通过一个带阀门的漏斗慢慢加入溶于700 mL冷水的7 g高锰酸钾溶液中。这一操作持续近一个小时。然后少量的乙醇加入该溶液中还原过量的高锰酸钾,过滤,并多次重复在水中煮沸锰沉淀,最后将所有的溶液合并,在水浴中蒸发至干燥。
蒸干的残余物中加入热的乙醇来溶解其中的有机盐,并除去大量不溶的碳酸钾。该醇溶液再次蒸干,并重新溶解于大约100 mL水中,然后小心的加入稀硫酸中和。刚开始有一些树脂类的杂质沉淀下来,我们用玻璃棒将其取出。继续加入稀硫酸直至溶液呈极弱的酸性,然后蒸干并用乙醇提取残留物。
该含有由氧化所产生自由酸的醇溶液再次蒸干。接着将其溶于水中,加入氨水,并使其在大约300 mL沸水中呈悬浊液,再通入硫化氢使其分解。溶液过滤并浓缩。在浓缩过程中相继得到两种晶状沉淀,接着将溶液蒸干。
前两个沉淀的晶体呈淡黄色,熔点在169 ℃左右(邻半蒎酸的熔点为160-161℃,间半蒎酸的熔点为174-175℃)。
我们知道这两种半蒎酸的性质很相似,因此要想区别它们非常困难。它们的衍生物也一样;仅有的一个能区分的例外是由GOLDSCHMIDT【15】报道的;那就是它们的乙酰胺,这两种酰胺可以通过在它们的酸中加入乙胺水溶液并在明火中加热得到。邻半蒎酸的乙酰胺(I)通过该法制备得到,其沸点为96-98℃,易溶于醇;而间半蒎酸的乙酰胺(II)熔点为227 ℃,且极难溶于醇,即使是加热情况下。

在该物质中加入少量30%的乙胺水溶液,然后在水浴中蒸干。白色的晶状残留溶于氯仿中,并转移到一个试管中小火加热。氯仿首先蒸干,然后残留的固体分解释放出气体并升华成漂亮的黄色晶体到试管内壁上。试管中所有的物质接下来重新溶于热的甲醇中。通过再冷却析出熔点为224-225℃细小的无色晶体,其难溶于乙醇,也因此具有间半蒎酸乙酰胺的性质。
将该晶体的母液浓缩后产生了第二次沉积下来的晶体,并被鉴定为第一次的晶体,因为两者具有相同的熔点。
最后的甲醇母液蒸干后,剩余一点残留物,其与前面晶体的熔点也很接近。
我当时在所有的组分都找不到一点邻半蒎酸乙酰胺的踪迹,因此,我觉得可以确定这最后几步操作只能产生间半蒎酸乙酰胺,而由此证明间半蒎酸是去甲基-克拉立定氧化的唯一产物。最后的结论便是,与克拉立定中类似,最后的四个甲氧基对称分布在两个苯环的母核中,这两个母核氧化都得到同样的二甲氧基邻苯二甲酸。

脱氢-去甲基-克拉立定

我的操作步骤跟上述三种情况完全一致【16】:
0.2 g 去甲基-克拉立定
0.4 g 碘
7 mL 乙醇
置于密封试管中并在水浴加热2小时。通过冷却得到氢碘盐酸和新生成碱的高碘化物的混合物,其难溶于醇。试管打开后,其内容物首先与浓的碳酸氢钠水溶液一起加热,然后再与硫酸溶液加热。过量的碘被消除掉,而脱氢-去甲基克拉立定的氢碘酸盐通过再次冷却得到亮黄色的沉淀。该沉淀过滤后在40%乙酸中重结晶。产物具有绝对的纯度,产率近乎理论值。
脱氢-去甲基克拉立定的氢碘酸盐呈细针状黄色结晶,熔点为252.5℃。该化合物几乎不溶于水,极易溶于稀乙酸中,极难溶于醇(与脱氢-克拉立定的氢碘酸盐不同,后者易溶于醇)。
元素分析

脱氢-去甲基克拉立定的硝酸盐。该化合物是通过氢碘酸盐和硝酸银的复分解反应得到的。其在水中长出黄色棱状晶体,熔点为261 ℃。
元素分析

自由碱。由于是季铵盐,脱氢-去甲基克拉立定的盐既不能被氨水也不能被碱金属的碳酸盐分解。而在苛性碱的作用下,他会发生进一步的转化,这一点我待会会提到。在所有情况下,它们的表现完全与小檗碱、脱氢紫堇碱以及脱氢克拉立定一致。
通过将新沉淀出的氧化银作用于盐酸盐的溶液中,我可以制备得到脱氢-去甲基克拉立定的水溶液。

接下来的两个组合更加稳定,即脱氢-去甲基克拉立定与氯仿或丙酮的组合物,也就是小檗碱所得到化合物的类似物。
脱氢-去甲基克拉立定与氯仿的组合
大约0.1 g 脱氢-去甲基克拉立定的硝酸盐与2 mL氯仿置于试管中。然后加入足够量的20%苛性钾溶液并剧烈搅动几分钟直至完全溶解。接下来将试管中的物质倒入圆底皿中并水浴加热蒸发掉多余的氯仿。冷却后就得到了二者组合的晶体;将其过滤并水洗,最后用干燥器干燥。我们通过将其在氯仿中得到新的晶体的方法来最终纯化该产物。其为黄色针状,细短晶体,熔点为215℃
脱氢-去甲基克拉立定与丙酮的组合
该产物的获得与上述完全一致,只是将氯仿用丙酮替代。通过在丙酮里结晶,最终获得了深黄色聚集且呈星状的晶体,熔点为150 ℃。
氢氧化钾对脱氢-去甲基克拉立定的作用
氧化-脱氢-去甲基克拉立定
J. GADAMER【17】在1905年实验发现,当小檗碱的盐与苛性碱一起加热时,其会转化成两个新的形态,方程式如下:
2 C20H19NO5(小檗碱)+H2O = C20H19NO4 + C20H17NO5 +2 H2O
C20H19NO4是一个三级碱;Gadamer 将其命名为脱氢小檗碱;C20H17NO5被鉴定为氧化小檗碱,因为PERKIN【18】曾用高锰酸钾氧化小檗碱得到过该化合物。
Gadamer对该反应机理的解释是假定小檗碱以醛(I)的形式出发, 然后在强碱的影响下经历Cannizarro歧化反应,接着通过水解而分解得到一分子醇(II)和一分子相应的酸(III)。这两个产物都不稳定,都失去了一分子水,前者得到脱氢小檗碱(IV),一个三级碱;而后者得到氧化小檗碱(V),一个中性化合物:


氧化-脱氢-去甲基-克拉立定(结构式VIII)
上述碱的碱性滤液是完全澄清的;它很可能含有酸VII的钾盐。如果我们将其在水浴情况下浓缩的话,它会很快形成沉淀;如果我们将其酸化或蒸干也会得到同样的结果。所有获得的部分都不溶于水和碱性溶液,并且都包含同样的酸VII的内酸酐,即氧化-脱氢-去甲基-克拉立定。仔细用水清洗,然后在苯或二甲苯中重结晶,其形成了黄色细棱状晶体,熔点为190℃。它与氧化小檗碱的相似关系使其具有如下性质:
在热的醇、苯以及二甲苯中能够适当溶解,在热的乙酸中易于溶解,而在乙酸酐中更加易于溶解;它几乎不溶于水、石油醚以及盐酸。而50%的热硫酸可以较难的溶解该化合物;如果我们在该溶液中加入一滴硝酸的话,它会变成紫色。该反应与生成氧化小檗碱的反应完全一致,唯一不同的是在加入水之后该反应的颜色消失了。
元素分析


C21H21NO5(COCH3): C = 67.48%
H =5.62%
然而,没有深入的研究很难最终确定该衍生物的组成。
格氏试剂作用于脱氢-去甲基-克拉立定
FREUND和H. BECK【19】发现将小檗碱的盐与有机镁试剂反应会得到二氢小檗碱的衍生物。例如,与甲基碘化镁反应方程式如下:


3 g 碘化钾
50 mL 干燥的乙醚
混合在一个小烧瓶里并接上冷凝回流管。该反应在常温下已经开始,我们最后水浴加热了一小会,然后等到所有的镁都溶解之后,我们将该溶液加入另一个含有0.5 g碘化脱氢-去甲基-克拉立定和20毫升干燥乙醚的烧瓶中。我们将其加热回流一天。加入几滴吡啶会使反应更容易进行。我们然后在反应中加入水并搅拌,使得新的碱能够游离出来,接着用乙醚萃取。乙醚相加入稀盐酸并搅拌,接着蒸干。残留物在40%的盐酸中重结晶,其熔点为120 ℃并确定是碱IX的盐酸盐。
该碱本身在甲醇中很难结晶。它呈黄色,熔点大约为180℃。
很遗憾的是,上述两个产物(盐酸盐和游离碱)的产率都非常低,所以我无法完整研究这类化合物,也无法进行分析。为了确定他们的性质,我必须局限于将其在一定量的碘和乙醇中氧化。也因此我得到了一些更容易纯化和表征的物质,并发现它们与Pictet和Malinowski的脱氢-克拉立定的盐是一致的。于是我得到了关于去甲基-克拉立定组成的新的证据。
下方的图表给出了这几个碱的氢碘酸盐和苦味酸盐熔点的测试对照。


HESSE【20】已经完成过罂粟碱的硝化。该学者获得了一个单硝化的衍生物,熔点为185℃;他没有鉴定出硝基所在的位置。这个问题仅在1904年由R. PSCHORR【21】得到了确定,其展示了硝化罂粟碱的如下信息:
1. 通过高锰酸钾的氧化得到6-硝化藜芦酸(I),熔点为188-190℃,且其组成之前已经由他自己鉴定了【22】;
2. 通过将苛性碱作用于其碘化钾获得6-硝基-高藜芦醚(II),熔点为118℃,且其组成之前已经由H. COUSIN鉴定【23】。

将20毫升密度为1.40的硝酸通过在冰和盐浴里冷却至0-5℃,在持续搅拌下,我们加入3 g研细的罂粟碱的粉末,然后我们将所有的反应物倒入冰水中。硝化罂粟碱的硝酸盐沉淀下来呈橙黄色晶体。我们将其过滤分离,水洗,然后在水浴加热的情况下加入稀释的氨水使其分解。再次过滤,用水和少量醇来洗涤游离碱,并在乙酸乙酯中重结晶得到产物,熔点为185℃。
硝化罂粟碱的还原
氨基-四氢罂粟碱

从氯化锡的滤液中还获得了少量的盐酸盐(伴随一些其他的还原产物),如果我们将其蒸干,并重新溶于约1升的沸水中,然后和上面一样通过硫化氢得到分解,再将产物通过锡和盐酸可进行新的还原反应。
氨基-四氢罂粟碱在空气中快速变色并非常不稳定。

将0.2 g 四氢罂粟碱的盐酸盐溶于2毫升冰粗醋酸中;然后用冰将其彻底冷却,接着一次性加入1毫升密度为1.40的硝酸和1毫升冰醋酸的混合物,并剧烈搅拌,反应溶液的颜色逐渐变成越来越深的红色。在颜色彻底变深之前,我们在反应溶液中加入几片冰并搅拌来终止硝化反应。获得的硝化四氢罂粟碱的硝酸盐呈大片状。该化合物纯度一般,或多或少有一些更进一步的硝化反应或氧化反应的副产物,我们可以将其在水中结晶来纯化,或者将其转化成盐酸盐更好。因此,我们将该化合物的硝酸盐与20%碳酸钠水溶液在水浴中加热,生成的游离碱快速过滤,用少量水清洗,然后溶于必需量的3%热醋酸中。冷却后,其产生白色针状盐酸盐。我们将其在水中进行进一步的重结晶来纯化该产物,彻底去除了所有其他的副产物。其熔点为228 ℃。该化合物不含结晶水,也几乎不溶于浓盐酸。
分析

这一一致性源于硝化-四氢罂粟碱的组成,上述化合物中硝基的位置与硝化罂粟碱本身的硝基位置是一样的。而我们对罂粟碱和四氢罂粟碱的硝化反应中,两种情况下,都是藜芦醇核心6位氢原子被硝基取代了。
硝化-四氢罂粟碱是一个次级碱,接下来我们展示其两个容易转化的衍生物:
亚硝基-硝化-四氢罂粟碱

乙酰基-硝化-四氢罂粟碱

分析

1 g硝化-四氢罂粟碱的盐酸盐与10毫升浓盐酸和20毫升水混合与烧瓶中并水浴加热回流。然后逐量加入大大过量的乙缩醛并加热回流2 h。混合物变成浅褐色,但仍有盐没有完全溶解。通过冷却后该盐再次几乎完全沉积。它的所有性质,尤其是与亚硝酸钠反应产生亚硝酸胺,表明该盐是没有转化的硝化-四氢罂粟碱的盐酸盐。
在过滤完该盐的滤液中仅有少量有机物质。在其中加入氨水,我们仅仅获得了硝化-四氢罂粟碱的沉淀。
因此该盐并没有与乙缩醛发生缩合反应。我做了很多其他的尝试,包括能做到最好的各种经验条件(优化盐酸的浓度、加热的时间等等),在乙酸介质中反应,甚至在氢氧化钠的碱性条件,结果都是阴性的。因此提出如下的结论:硝基的存在与已知的其他情况一样,使得分子不能发生新的环化反应。
氨基-四氢罂粟碱与乙缩醛的缩合反应
这个反应也和之前的反应条件类似,即将1 g氨基-四氢罂粟碱的盐酸盐与2毫升浓盐酸和5毫升水置于烧瓶中水浴加热回流。然后在半小时内缓慢加入2 g乙缩醛,反应溶液的颜色慢慢加深。冷却后,没有任何产物沉积。于是加水稀释该溶液,并加入碳酸钠使得该碱得到沉淀并用乙醚萃取。乙醚相接着用硫酸钠干燥,然后通入干燥的氯化氢气体使其产生黄色沉淀并过滤。但是该化合物在湿空气中易潮解,因此难以保存。我无法获得它的理想状态来进行化学分析。该物质极有可能是氨基-紫堇碱的盐酸盐。

通过与碳酸碱的作用,该盐酸盐形成了一个非常不稳定的碱。
由于该碱以及其盐酸盐没有给出什么优越的性质,我不得不放弃对它的深入研究,而且没有没有其它方法来消除氨基并由此可能得到紫堇碱。
我按照FRIEDLANDER【24】的方法在水溶液中进行了该盐酸盐的重氮化反应,并将产物倒入含有氯化锡的冷苏打水溶液中。接着将其加热到接近沸点,我仅仅发现了非常少的氮气释放出来。冷却后,其沉积出少量的碱性物质,但是树脂粘稠状,因此无法通过结晶来纯化该物质。在这种情况下,我无法成功分离到一个确定的物质来与紫堇碱做比较。
UNI-GE SCIEN
1071590179
制版人:小娴子
注释详细
[1]Berzelius Tabresbericht I, 220 (1826)
[2]Berichte, 46, 2688.
[3]Berichte, 44, 2030.
[4]Berichte, 44, 2480.
[5]Berichte, 37, 4673. (1905)
[6] Journ.Chem. Soc. 95, 1614.
[7] Journ.Chem. Soc. 65, 57 (1894); 67, 17 (1895).
[8]Berichte, 37, 4673. (1905)
[9]Berichte 37, 1932 (1904)
[10]详见Kay 和Pictet. J. Chem. Soc.
[11] J.Chem. Soc. 95. 1614.
[12]亚甲基-四氢罂粟碱这个名字实际是在其结构及与克拉立定的关系确定前就已经取的。
[13] Chem.Soc. 65. 57 (1894); 67, 17 (1895).
[14]Berichte 46, 2695 (1913).
[15]Monatshefte 9 762 (1888).
[16] E.Schmidt, Archiv. der Pharm. 232, 144(1894). Zigenbein,Archiv. der Pharm. 234, 505 (1896). Pictet&Malinowski, Berichte 46, 2694 (1913).
[17]Archiv. Der. Pharm. 243, 34 (1905).
[18] J.Chem. Soc. 57, 1085 (1890).
[19]Berichte 37, 4673 (1905).
[20] Hesse.Annalen Suppl., 8, 202.
[21]Pschorr. Berichte 37, 1932 (1904).
[22]Pschorr. Berichte 327, 3405 (1900).
[23]Cousin. Ann. Ch. Phys. (7) 13, 545(1898).
[24]Berichte 22, 587.
中国化学会
Chemsoc
原标题:《史料|中国第一位化学博士赵承嘏的博士论文》
本文为澎湃号作者或机构在澎湃新闻上传并发布,仅代表该作者或机构观点,不代表澎湃新闻的观点或立场,澎湃新闻仅提供信息发布平台。申请澎湃号请用电脑访问http://renzheng.thepaper.cn。





- 报料热线: 021-962866
- 报料邮箱: news@thepaper.cn
互联网新闻信息服务许可证:31120170006
增值电信业务经营许可证:沪B2-2017116
© 2014-2024 上海东方报业有限公司




